🎧 I farta? Lytt til podcast om signalsubstanser under!
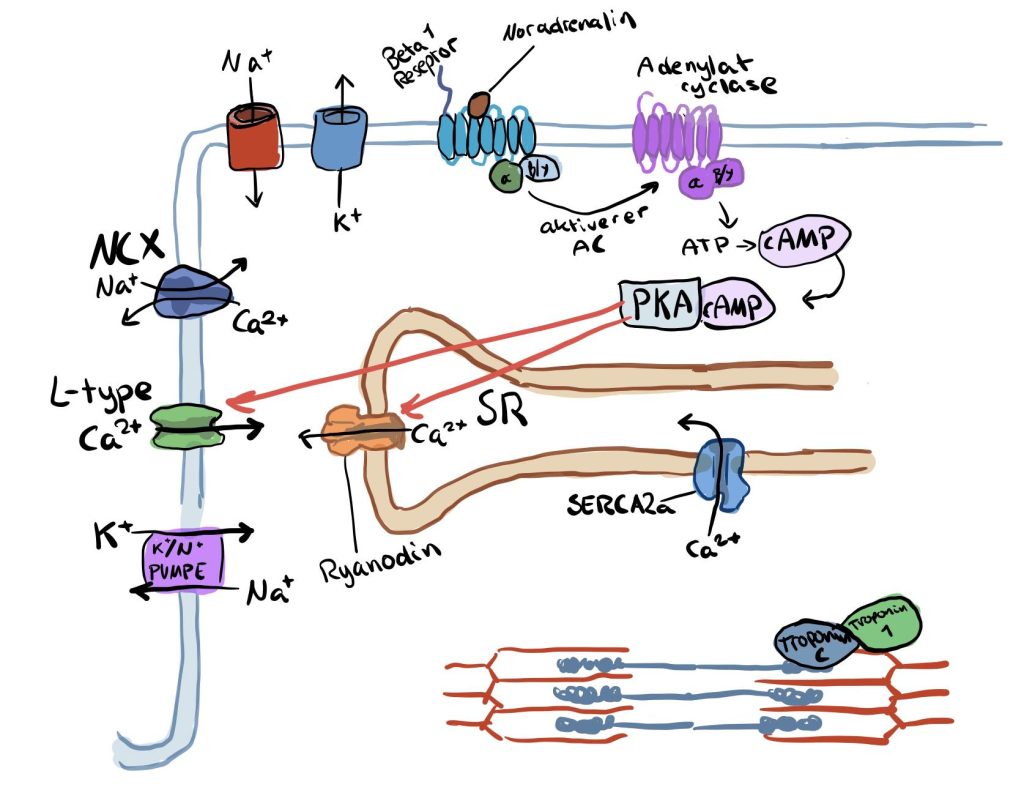
Signalsubstanser i hjertet
Hjertet slår av seg selv, rytmisk og presist, takket være spesialiserte pacemakerceller som spontant genererer elektriske signaler. Men selv om hjertet er selvgående, er det langt fra autonomt i praksis. Kroppen trenger et system som kan justere både rytmen og kraften i hvert hjerteslag – og dette styres i stor grad av signalsubstanser, altså kjemiske budbringere som overfører informasjon mellom nerveceller og hjertemuskelceller.
Det autonome nervesystemet – med sine sympatiske og parasympatiske grener – er den viktigste leverandøren av slike signaler.
Når du trener, får feber eller blir redd, øker den sympatiske aktiviteten og hjertet slår raskere og kraftigere. Når du hviler, senker vagusnerven pulsen og sparer energi. Dette skjer ikke ved magi, men ved hjelp av spesifikke reseptorer, signalveier og intracellulære mekanismer – som alle jobber for å tilpasse hjertets aktivitet til kroppens behov i sanntid.
På denne siden går vi gjennom hvordan disse signalsubstansene virker på hjertet – fra reseptorer og intracellulære effekter, til hvordan ulike stimuli (som stress, sykdom eller trening) påvirker samspillet mellom nervesystemet og hjertemuskelen.
Regulering av hjertets frekvens og kontraktilitet
Sympatikus (fight-or-flight)
Sympatikus øker hjertets aktivitet for å møte kroppens behov under stress, fysisk aktivitet eller fare. Dette er en evolusjonært bevart respons som forbereder kroppen på handling.
Når vi får en sympatisk respons, som ved akutt stress eller trening, vil noradrenalin (NE) frigjøres fra sympatiske nerveender (i hjertet, spesielt i sinusknuten). Noradrenalin binder seg til β₁-adrenerge reseptorer på overflaten av pacemakerceller i sinusknuten. β₁-reseptoren er koblet til et Gs-protein (stimulerende G-protein). Når denne aktiveres, vil adenylyl(adenylat) cylase bli aktiv. Og da bør du huske hva som skjer:
- Adenylat syklase omdanner ATP til cAMP, en viktig second messenger.
- Økt cAMP aktiverer PKA (protein kinase A), som fosforylerer flere proteiner. Akkurat denne signalveien ser vi i flere situasjoner, så den er grei å huske at et et slags “mellomledd” i signalveien.
Men derifra vil PKA komme inn å fosforylere flere proteiner, derav funny channels og L-type kalsiumkanaler. Disse er veldig viktige i sinusknuten! Så nå blir disse fosforylert og hav skjer da?
HCN-kanaler («funny channels»): Disse kanalene tillater Na⁺ og K⁺ å lekke inn i cellen under hvile. PKA-fosforylering gjør at de åpner raskere og oftere, noe som gjør at mer natrium og kalium strømmer inn og dette fremskynder spontan depolarisering.
L-type Ca²⁺-kanaler: Fosforylering øker Ca²⁺-innstrømningen i depolariseringsfasen → Aksjonspotensialer genereres raskere.
Så hele signalveien fra Noradrenalin til fosforylering av disse to viktige kanalene, leder da til at vi får flere aksjonspotensialer. Og det betyr jo selvsagt: hjertet banker fortere.
🧠Repetisjon:
Hva er HCN (funny) kanaler? Etter hvert hjerteslag faller membranpotensialet i pacemakercellen (spesielt i sinusknuten) til rundt -60 til -70 mV. Dette er ganske negativt – og det er akkurat da funny channels våkner til liv. De åpner når membranpotensialet er blitt «for negativt» (hyperpolarisert).
De slipper inn Na⁺ (og litt K⁺) → dette øker membranpotensialet gradvis (gjør det mer positivt igjen).
Det kalles spontan depolarisering, og det er det som gjør pacemakerceller selvgående.
Så de hjelper altså til å gjøre cellen litt mer positiv før andre kanaler tar over og depolariserer cellen.
Poenget: Funny channels sørger for at membranpotensialet aldri blir for negativt for lenge. De starter neste depolarisering så fort hjertet er klart for det, og sørger for at det kommer et nytt slag i tide
Økt kontraktilitet via β₁-adrenerge reseptorer – mer kalsium = sterkere hjerteslag
Når det sympatiske nervesystemet aktiveres – for eksempel ved fysisk aktivitet, stress eller fare – trenger kroppen mer blod til musklene og hjernen. Da holder det ikke bare at hjertet slår raskere. Det må også slå kraftigere. Dette kalles økt kontraktilitet, eller positiv inotropi, og det skjer via en presis kjemisk signalvei som starter med β₁-adrenerge reseptorer.
Disse reseptorene sitter på overflaten av hjertemuskelcellene (kardiomyocytter). Når noradrenalin (eller adrenalin) binder seg til β₁-reseptoren, aktiveres et signalprotein inne i cellen som setter i gang en kaskade av hendelser. Denne kaskaden fører til at det blir mer kalsium (Ca²⁺) tilgjengelig inne i cellen – og det er nettopp dette som gir den kraftigere kontraksjonen.
La oss se nærmere på de tre viktigste mekanismene som forklarer hvordan sympatisk stimulering øker intracellulært kalsium og dermed kontraktiliteten:
1. L-type Ca²⁺-kanaler fosforyleres og slipper inn mer kalsium
Etter aktivering av β₁-reseptoren blir PKA (proteinkinase A) aktivert.
PKA fosforylerer L-type kalsiumkanaler i cellemembranen, som dermed blir mer følsomme og åpner lettere og lenger enn vanlig. Resultatet er at mer Ca²⁺ strømmer inn i cellen fra ekstracellulærvæsken under hvert aksjonspotensial.
2. Ryanodinreseptorene (RyR2) aktiveres og frigjør lagret kalsium fra SR
Det kalsiumet som kommer inn via L-type-kanalene fungerer som en slags «tennplugg» – det aktiverer ryanodinreseptorer (RyR2) på sarkoplasmatisk retikulum (SR). Dette fører til en eksplosiv frigjøring av store mengder kalsium som allerede var lagret i SR, gjennom en prosess kalt kalsiumindusert kalsiumfrigjøring (CICR).
3. Flere Ca²⁺ → Flere kryssbroer → Kraftigere kontraksjon
Men hvorfor gir mer kalsium en sterkere kontraksjon?
Fordi Ca²⁺ binder til troponin C, som gjør at tropomyosin flytter seg og avslører bindingssetene på aktin.
Nå kan myosin gripe tak i aktin – og jo mer kalsium som er tilgjengelig, desto flere kryssbroer dannes mellom myosin og aktin.
Tenk på det som flere «hender» som drar i et tau: flere hender = sterkere drag. Dette gir en kraftigere og mer effektiv kontraksjon av hjertemuskelen.
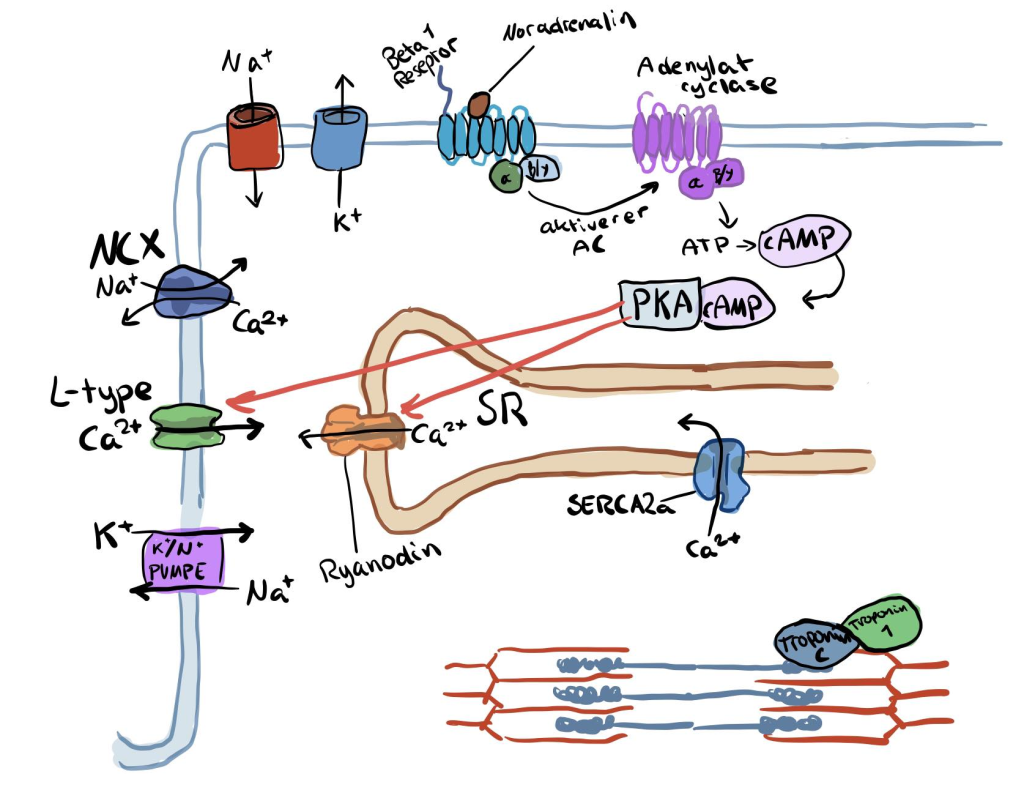
α₁-adrenerge reseptorer
Når vi snakker om sympatisk stimulering av hjertet, handler det aller meste om β₁-adrenerge reseptorer – de som øker hjertefrekvens og kontraktilitet dramatisk når det trengs.
Men de er ikke alene. I bakgrunnen finnes en annen type reseptor, nemlig α₁-adrenerge reseptorer, som spiller en mer subtil, men viktig rolle.
Disse reseptorene sitter også på hjertemuskelcellens membran, og de aktiveres først og fremst av noradrenalin – det samme signalstoffet som virker på β₁.
Forskjellen ligger i hvordan de virker inni cellen, og hvilke intracellulære signalveier de setter i gang.
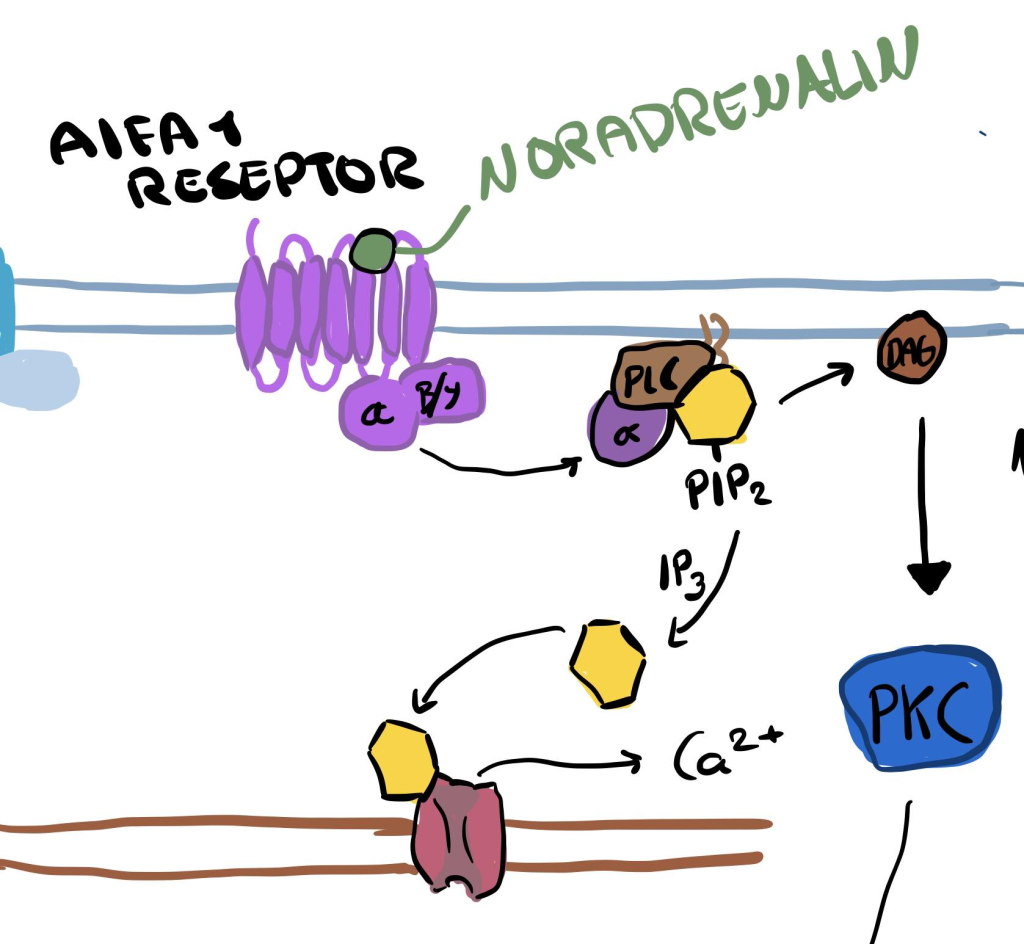
En annen signalvei: Gq og fosfolipase C
Mens β₁-reseptorer aktiverer Gs-proteiner og øker cAMP, går α₁-reseptorer en annen vei.
De aktiverer et annet G-protein kalt Gq, som i sin tur aktiverer fosfolipase C (PLC).
Når PLC aktiveres, spalter det en lipid i cellemembranen (PIP₂) til to viktige signalmolekyler:
- IP₃ (inositoltrifosfat)
- DAG (diacylglyserol)
IP₃ → Øker intracellulært kalsium
IP₃ diffunderer raskt gjennom cytosol og binder seg til egne reseptorer på sarkoplasmatisk retikulum (SR) – og det fører til frigjøring av lagret Ca²⁺ fra SR, uavhengig av L-type Ca²⁺-kanalene. Resultatet er mer kalsium i cytosol → økt kontraktilitet.
DAG → Aktiverer PKC og modulerer kontraksjonsapparatet
DAG aktiverer enzymet proteinkinase C (PKC), som fosforylerer ulike proteiner i kontraksjonsapparatet. Dette kan blant annet påvirke følsomheten for kalsium og modulere hvor kraftig hver Ca²⁺-bølge faktisk påvirker aktin og myosin.
Denne signalveien er ikke like rask eller dominerende som β₁-veien, men den er viktig i langsom finjustering av kontraktiliteten, og særlig i langvarig sympatisk stimulering – som ved hjertesvikt, hypertrofi eller stressrespons over tid.
Noen studier tyder også på at α₁-reseptorer kan bidra til å beskytte hjertemuskelen mot overstimulering og apoptose – altså celledød – ved å gi en mer «modulert» form for kalsiumsignalering.
Hva gjør PKC, og hvorfor er det viktig for hjertets kontraksjon?
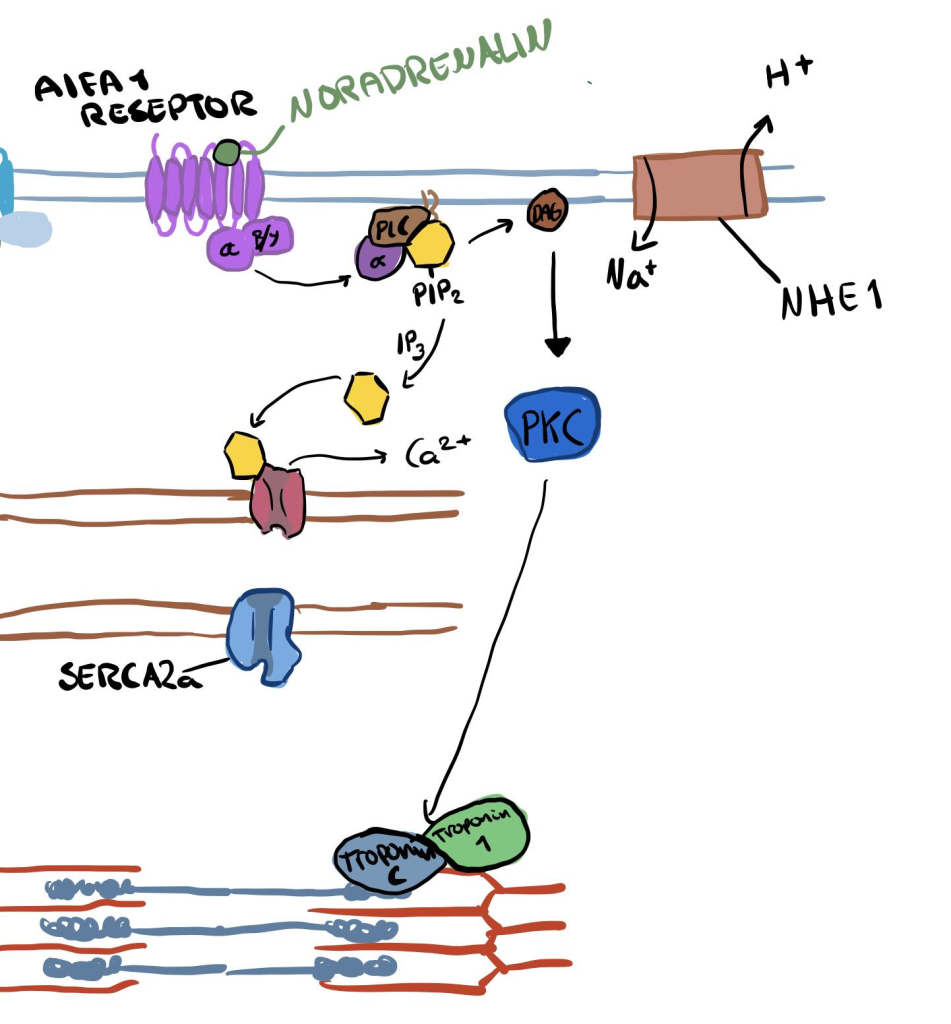
Hva gjør PKC – og hvorfor betyr det noe for hjertets kontraksjon?
I hjertemuskelcellene er det ikke bare mengden kalsium som bestemmer hvor kraftig en kontraksjon blir. Det handler også om hvordan cellen reagerer på kalsium – altså kalsiumfølsomhet. Her spiller PKC (proteinkinase C) en sentral rolle.
PKC aktiveres som en del av signalveien som starter med α₁-adrenerge reseptorer, og fungerer som en slags “modulator” av kontraktilitet – ikke ved å oversvømme cellen med kalsium, men ved å gjøre hjertet mer følsomt for det kalsiumet som allerede er der. Dette er spesielt viktig i situasjoner der β₁-responsen er nedsatt, for eksempel ved langvarig stress, hypertrofi eller hjertesvikt.
La oss se nærmere på de to hovedmåtene PKC bidrar på:
PKC fosforylerer myosin light chain 2 (MLC-2)
MLC-2 er en del av det kontraktile apparatet i hjertemuskelcellen, og har en viktig rolle i hvordan myosin-hodene binder til aktinfilamentene under kontraksjon.
Når PKC fosforylerer MLC-2, skjer det en interessant ting:
Myofilamentene blir mer følsomme for kalsium.
Det betyr at selv med et moderat kalsiumnivå i cytosol, kan cellen likevel utvikle en kraftig kontraksjon. Det er som om troponin- og myosin-systemet skrur opp volumet på kalsiumsignalet. Myofilamentene – og gir dermed kraftigere kontraksjon uten nødvendigvis å øke hjertefrekvensen.
PKC aktiverer Na⁺/H⁺-utveksleren (NHE1)
Den andre effekten av PKC skjer indirekte gjennom cellens pH-regulering.
Når PKC aktiveres, stimuleres Na⁺/H⁺-utveksleren, også kalt NHE1.
Denne transportøren bytter H⁺ ut og Na⁺ inn i cellen. Resultatet er at det blir mindre surt inne i cellen – altså en økning i intracellulær pH.
Og hvorfor er det viktig?
Kalsium binder seg sterkere til troponin C når pH er høy.
Med andre ord: selv om mengden kalsium er den samme, så blir effekten større når pH øker. Dette er nok en måte hjertet kan “få mer ut av” hver Ca²⁺-bølge, og bidra til en kraftigere sammentrekning under krevende forhold.
Så tenk gjennom det: Hvorfor øker det ikke hjertefrekvensen når det utløser mer kalsium? Vel, fordi reseptorene er plassert på myocyttene, ikke i ledningssystemet (sinus og AV). Dermed påvirker det ikke frekvensen i lik grad.
Økt relaksasjonshastighet (lusitropi):
Lusitropi beskriver hjertets evne til å slappe av mellom hvert slag. Dette er avgjørende for at hjertet skal kunne fylle seg effektivt med blod før neste kontraksjon. Når hjertet slår raskt, for eksempel under fysisk aktivitet eller stress, er det spesielt viktig at det også rekker å slappe ordentlig av mellom slagene – ellers blir fyllingen dårlig, og hjertets pumpeevne reduseres.
Under sympatisk stimulering, når noradrenalin binder seg til β₁-adrenerge reseptorer på hjertemuskelcellene, aktiveres enzymet PKA (protein kinase A).
PKA har flere mål i cellen, og en av de viktigste for lusitropi er proteinet fosfolamban. Fosfolamban fungerer som en brems på SERCA2a-pumpen – pumpen som fjerner kalsium fra cytoplasma og sender det tilbake inn i sarkoplasmatisk retikulum, hjertemuskelcellens indre kalsiumlager. Når PKA fosforylerer fosfolamban, oppheves denne bremsen.
Resultatet er at SERCA2a jobber raskere og mer effektivt, slik at kalsiumnivået inne i cellen synker raskere etter en kontraksjon.
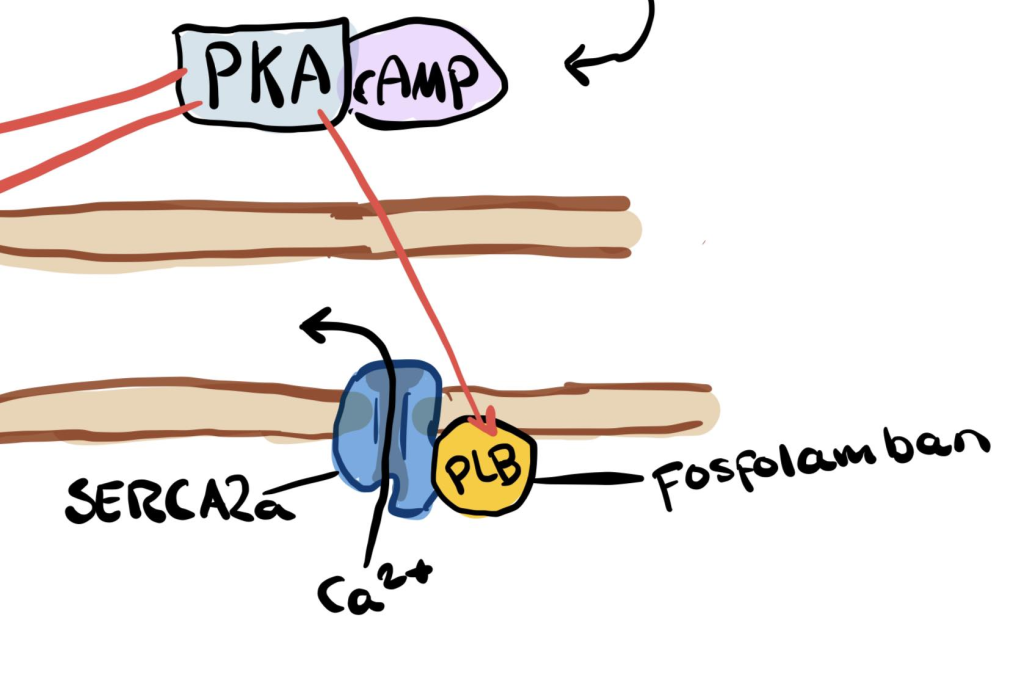
I tillegg påvirker PKA et annet nøkkelprotein, nemlig troponin I. Når troponin I fosforyleres, reduseres dets affinitet for kalsium, noe som gjør at kalsium slipper løs fra troponin C tidligere. Dette bidrar til at kontraksjonsprosessen avsluttes raskere, og at muskelfiberen går tilbake til avslappet tilstand.
Til sammen fører disse mekanismene til at hjertet kan slappe av raskere og mer effektivt etter hvert slag.
Resultat av sympatisk stimulering – hva skjer med hjertet?
Når det sympatiske nervesystemet aktiveres – som ved stress eller fysisk aktivitet – tilpasses hjertet for å kunne levere mer blod og oksygen til kroppen. Dette skjer gjennom en kombinert økning i hjertefrekvens (HR) og slagvolum (SV), som sammen gir økt minuttvolum (cardiac output, CO = HR × SV).
I tillegg blir hjertets arbeid mer effektivt koordinert: kontraksjonen blir kraftigere, og relaksasjonen skjer raskere, slik at hjertet både tømmer og fylles bedre – selv når det slår raskt.
Dette gir økt tilførsel av oksygen og næringsstoffer til vevene, noe som er helt avgjørende under fysisk belastning.
Men denne tilpasningen har også en pris: hjertet bruker mer ATP og har et høyere oksygenforbruk, noe som øker den metabolske belastningen – spesielt viktig å huske ved hjertesykdom.
Parasympatikus (rest-and-digest)
Parasympatikus dominerer når kroppen er i hvile, og bidrar til å senke hjertets aktivitet for å spare energi og fremme restitusjon. Det parasympatiske signalet kommer via vagusnerven, som frigjør acetylkolin (ACh).
ACh virker hovedsakelig på sinusknuten og AV-knuten, der det binder seg til M2-muskarinreseptorer. Disse reseptorene er koblet til inhibitoriske G-proteiner (Gi), som hemmer enzymet adenylat syklase. Da forstår vi kjapt at det fører til redusert produksjon av cAMP, noe som gir motsatt effekt av sympatikus:
-Funny channels (HCN) aktiveres tregere → lavere hjertefrekvens –Kalsiumkanaler åpnes saktere → redusert ledning og impulsdannelse Mindre kalsium inn i cellen, betyr mindre kalsiumfrigjøring fra ryanodinreseptorer. Resultatet er langsommere hjerterytme og redusert overledning gjennom AV-knuten
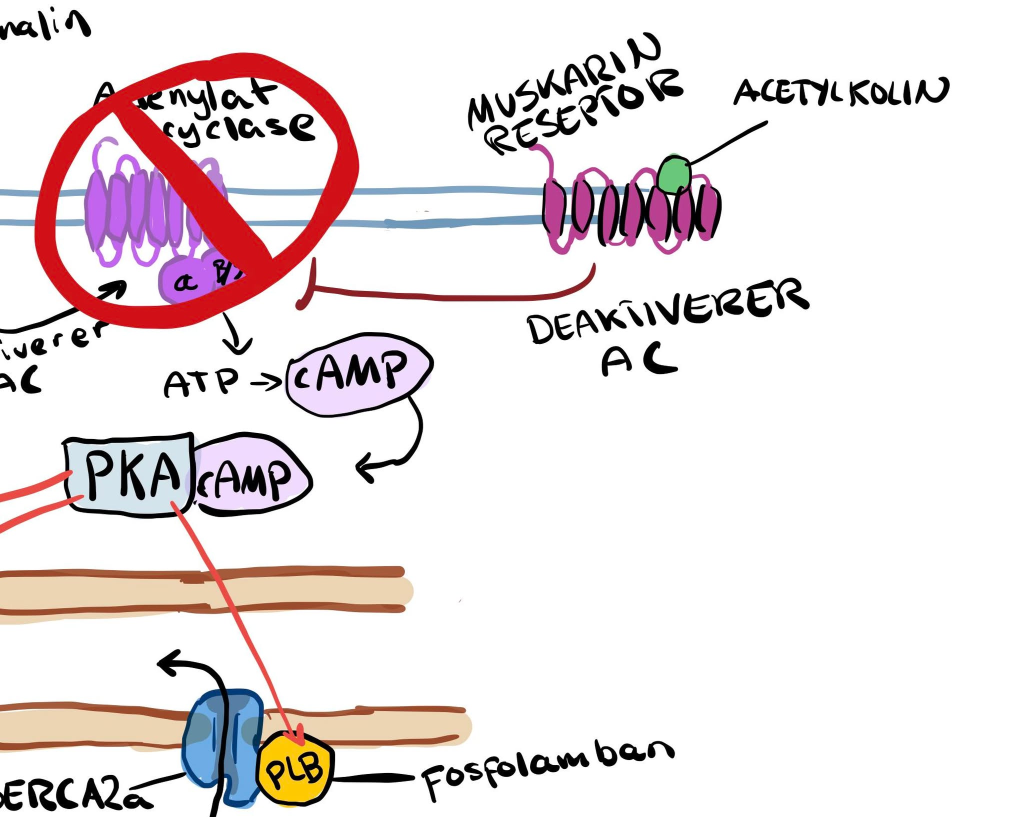
Har derimot en minimal effekt på kontraktilitet
Parasympatisk innervasjon er hovedsakelig begrenset til atriene og ledningssystemet. Ventriklene har lite til ingen direkte parasympatisk påvirkning. Derfor har parasympatikus svært liten effekt på slagkraften i hjertet (kontraktiliteten).
Dette er sannsynligvis en evolusjonært bevart sikkerhetsmekanisme: Selv når hjertet slår langsomt i hvile, beholdes en viss slagkraft slik at blodsirkulasjonen opprettholdes til vitale organer.
Parasympatikus bidrar til å skåne hjertet i hvile ved å redusere hjertefrekvens og energiforbruk. Dette sparer ATP og oksygen, reduserer metabolsk stress, og har en beskyttende effekt mot arytmier. Samlet sett støtter det restaurering og vedlikehold av hjertehelse, og er særlig viktig for kroppens restitusjon og langsiktige balanse.
🫀 Kardiovaskulær regulering og respons
Sentral regulering av det kardiovaskulære systemet
Hjernen spiller en aktiv rolle i å tilpasse hjerte og blodårer til kroppens behov. Denne styringen skjer både bevisst og ubevisst, gjennom samspill mellom høyere hjerneområder og autonome sentre i hjernestammen.
Central command – hjernens overordnede styring
Når vi forbereder oss på bevegelse – enten vi faktisk beveger oss eller bare tenker på det – aktiveres motorisk cortex og andre høyere hjerneområder. Disse områdene sender signaler til det kardiovaskulære kontrollsenteret i hjernestammen, spesielt til en struktur som kalles ventrolateral medulla (VLM).
VLM fungerer som en dirigent for hjerte og blodårer:
– Den øker sympatisk nerveaktivitet, som får hjertet til å slå raskere og blodårene til å trekke seg sammen.
– Samtidig reduseres parasympatisk aktivitet via signaler til nucleus ambiguus, som normalt bremser hjertet.
– I tillegg kan VLM stimulere binyrene til å slippe ut stresshormoner som adrenalin, som forsterker den sympatiske effekten.
Reflekser og automatisk regulering
Kroppen har innebygde systemer som kontinuerlig overvåker og justerer blodtrykk, blodvolum og hjerteaktivitet – uten at vi tenker over det.
Barorefleksen – kroppens blodtrykksvakt: Baroreseptorer er spesialiserte strekkfølsomme sanseceller som finnes i aortabuen og carotis sinus. De registrerer hvor mye blod som presser på arterieveggen – altså blodtrykket.
Når blodtrykket øker, strekkes veggene mer, og baroreseptorene fyrer hyppigere. → Dette fører til økt parasympatisk og redusert sympatisk aktivitet. Hjertet roer seg, blodårene slapper av, og blodtrykket synker.
Når blodtrykket faller, reduseres fyringen. → Dette gir økt sympatikus og mindre parasympatikus, som øker hjertefrekvens, kontraktilitet og karsammentrekning – for å heve blodtrykket igjen.
Barorefleksen er kroppens raske og presise system for å holde blodtrykket stabilt fra sekund til sekund.
Kardiopulmonære reflekser – volumregulering
I tillegg til trykkfølsomme baroreseptorer, finnes det lavtrykksreseptorer i områder som hjertevegg, lungevener og de store venene. Disse registrerer endringer i blodvolum og venetrykk – altså hvor mye blod som er på vei tilbake til hjertet.
Når blodvolumet er høyt, påvirker disse reseptorene viktige systemer:
- De hemmer ADH (antidiuretisk hormon) fra hypofysen, slik at nyrene skiller ut mer vann.
- De hemmer sympatikus til nyrene, noe som øker filtrasjonen.
- De kan også påvirke renin-angiotensin-aldosteron-systemet, som er sentralt for langtidsregulering av blodtrykk og væskebalanse.
Dette systemet virker tregere enn barorefleksen, men er avgjørende for volumkontroll over tid.
Exercise pressor reflex – når musklene ber om mer blod
Når du beveger deg, skjer det ikke bare bevisst aktivering fra hjernen. Skjelettmuskulaturen selv sender også signaler om at den trenger mer blod. Dette skjer gjennom to typer reseptorer:
Mekanoreseptorer (type III-fibre): Reagerer på strekk og bevegelse i muskelen.
Metaboreseptorer (type IV-fibre): Reagerer på stoffer som hoper seg opp under aktivitet, som laktat, H⁺, CO₂ og K⁺.
Disse signalene sendes via ryggmargen til hjernestammen, hvor de aktiverer VLM og dermed øker sympatisk nerveaktivitet.
Resultatet er:
- Økt blodtilførsel til arbeidende muskler
- Økt cardiac output (CO) via økt hjertefrekvens og slagvolum
- Omdirigering av blod bort fra ikke-aktive organer (f.eks. hud og fordøyelse)
Dette gir bedre oksygenforsyning og opprettholdelse av blodtrykk under fysisk aktivitet.
Kardiovaskulær regulering under fysisk aktivitet
Kroppen har en evne til å forberede og tilpasse hjerte- og karsystemet når vi skal være fysisk aktive. Allerede før selve bevegelsen starter, setter hjernen i gang en forberedende respons, og under aktiviteten videreføres og forsterkes denne reguleringen gjennom komplekse nevro-hormonelle og lokale mekanismer.
Før aktivitet: Forventningsresponsen
Før du løper, sykler eller trener, vil kroppen automatisk begynne å forberede seg. Denne anticipatoriske responsen styres av hjernens motoriske områder og andre høyere sentre (det såkalte central command), og er en delvis bevisst og delvis ubevisst reaksjon. Signaler fra hjernen aktiverer det kardiovaskulære senteret i hjernestammen, noe som fører til økt sympatisk nerveaktivitet og samtidig hemming av parasympatiske signaler, særlig mot sinusknuten.
Konsekvensen av dette er at hjertefrekvensen begynner å øke allerede før du har tatt det første steget. Hjertets kontraktilitet øker, blodtrykket stiger lett, og blodårene i de arbeidende musklene begynner å utvide seg. Alt dette skjer for å sikre at blodstrøm og oksygentilførsel er i gang før det fysiske arbeidet starter.
Under aktivitet: Samspill mellom nerver og muskler
Når selve bevegelsen begynner, trekkes den parasympatiske aktiviteten ytterligere tilbake, og det sympatiske nervesystemet tar gradvis mer kontroll – i takt med økt intensitet. Dette fører til en progressiv økning i hjertefrekvens og kontraktilitet, samt økt total blodstrøm fra hjertet (cardiac output). Samtidig strammes blodårene inn (vasokonstriksjon) i ikke-aktive områder som hud, fordøyelsesorganer og nyrer, slik at mer blod kan omdirigeres til de arbeidende musklene.
Når selve bevegelsen starter, trekkes den parasympatiske aktiviteten ytterligere tilbake, og det sympatiske nervesystemet tar gradvis over kontrollen. Jo høyere intensitet, desto sterkere blir den sympatiske aktiveringen. Dette fører til en progressiv økning i både hjertefrekvens og kontraktilitet, og dermed øker også den totale blodstrømmen fra hjertet – det vi kaller cardiac output.
Samtidig strammes blodårene inn (vasokonstriksjon) i områder som fordøyelsessystemet, nyrer og i starten også huden, slik at mer blod kan prioriteres til de arbeidende musklene. Dette er en viktig del av kroppens omfordeling av ressurser under fysisk belastning.
Men etter hvert som kroppstemperaturen stiger under trening, skjer det en fysiologisk endring: hudens blodårer dilaterer for å muliggjøre varmeutveksling og svetteproduksjon. Dermed går huden fra å ha redusert blodtilførsel tidlig i økten, til å motta betydelig mer blod mot slutten – spesielt under langvarig eller intensiv trening. Denne justeringen styres av kroppens behov for å både prestere og kjøle seg ned samtidig.
Lokalt i musklene fører de samme metabolske endringene til vasodilatasjon, altså utvidelse av blodårene. Selv om sympatikus normalt gir vasokonstriksjon, vil disse lokale signalene kunne overstyre det sympatiske nervesystemet der det trengs mest – i de arbeidende musklene. Bemerk deg dette!
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3