For å passe på at alle prossesser i cellesyklus gjøres rett, for å for eksempel forhindre DNA feil og kreftdannelse, har cellesyklusen sjekkpunkter for å kontrollere alt før cellen kan gå videre i syklusen.
Disse sjekkpunktene er også kalt molekylære bremser, fordi de pauser syklusen på bestemte steder.
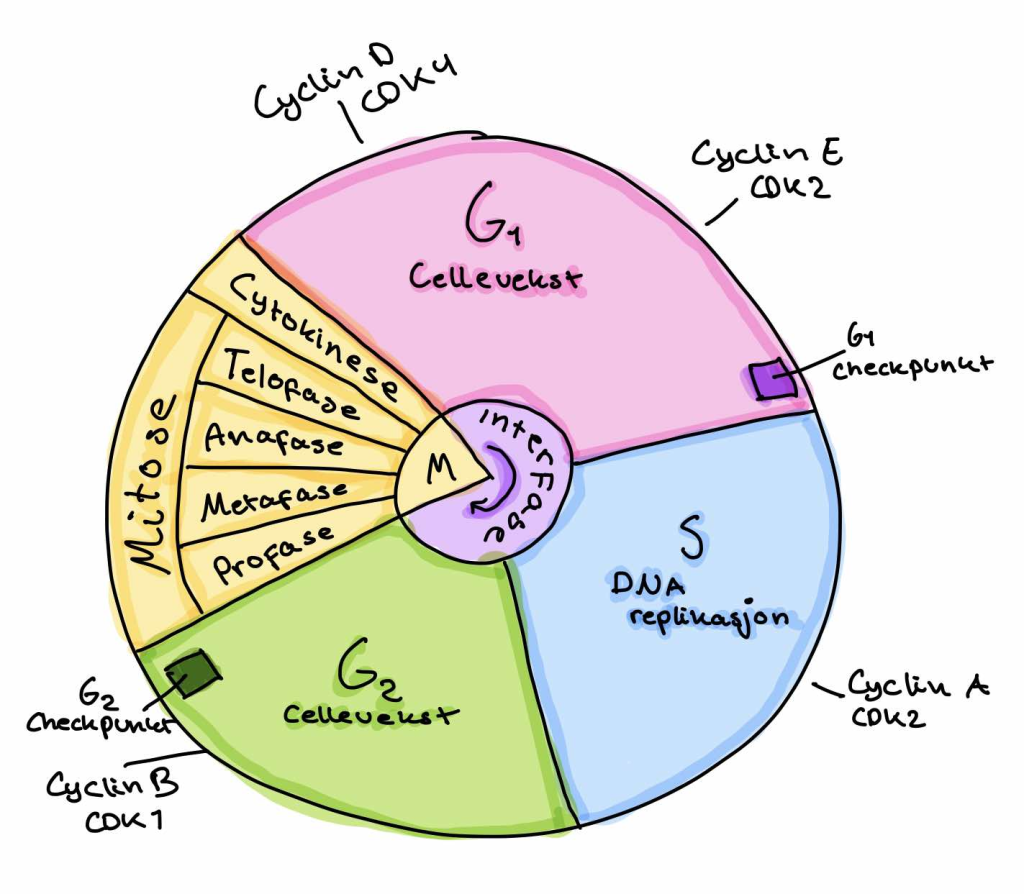
Tre hovedsjekkpunkter i cellesyklus:
G1/S-fase overgang:
Er miljøet bra nok til å starte celledeling?
Dette er det første store kontrollpunktet i cellesyklusen. Her bestemmer cellen om den skal begynne å dele seg eller ikke. Tenk på det som en «start-knapp» for celledeling.
Cellen lytter til signaler utenfra (som veksthormoner) som forteller den om det er trygt og nødvendig å starte delingen.
Hvis disse signalene er positive, begynner cellen å produsere et protein som kalles cyclin D.
Cyclin D fungerer som en nøkkel som setter i gang hele prosessen.
Når cyclin D er aktivt, starter det en kjedereaksjon som driver cellen fremover mot S-fasen, hvor selve DNA-kopieringen skal skje.
Dette er et viktig punkt fordi når cellen først har passert dette kontrollpunktet, er den vanligvis forpliktet til å fullføre hele cellesyklusen.
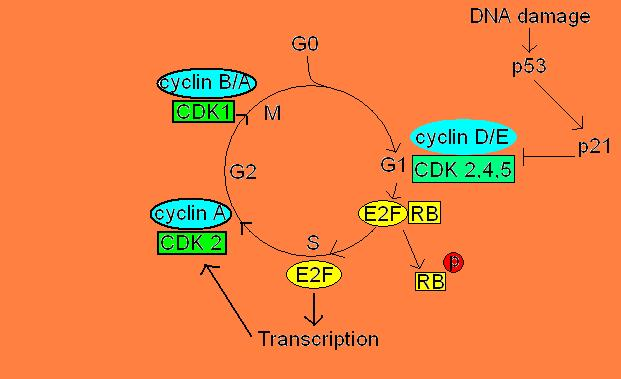
G2/M-fase overgang:
Er DNA replikert?
Er alt reparert?
Sjekker om DNA er korrekt og fullstendig replikert før cellen går videre til mitose. Sikrer at cellen har tilstrekkelig størrelse og ressurser for å gjennomføre celledelingen.
- Aktiverer proteiner som er nødvendige for å starte mitosen.
- Her er det spesielt viktig med regulering gjennom fosforylering.
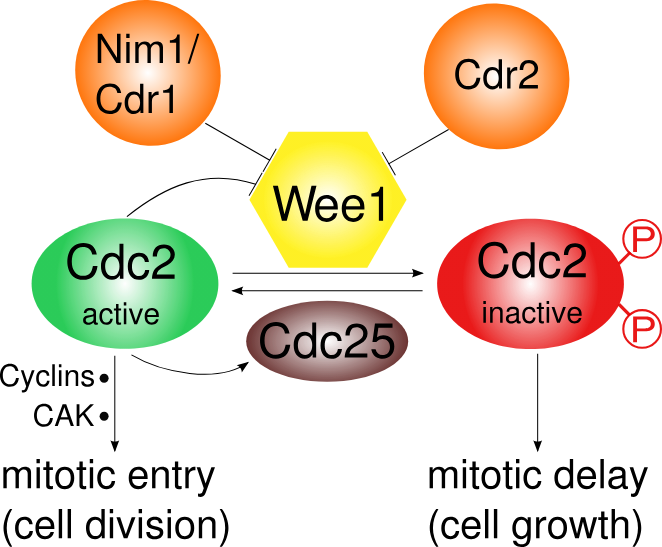
- Enzymet Wee1 kan hemme CDK gjennom fosforylering, mens fosfatasen Cdc25 kan fjerne disse hemmende fosfatgruppene for å reaktivere CDK
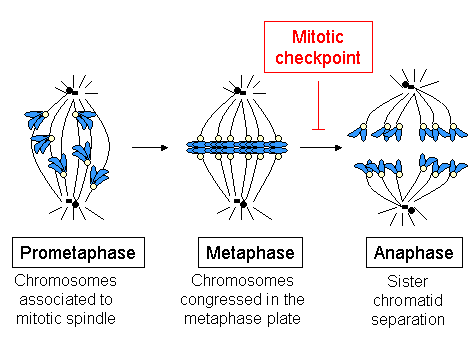
Overgangen metafase til anafase
Metafase-anafase-overgangen er et kritisk punkt i celledelingen. Det er her cellen bestemmer seg for å gå videre – eller vente. På dette tidspunktet ligger alle kromosomene pent oppstilt langs den midterste linjen i cellen, kjent som metafaseplaten. Men før cellen får klarsignal til å trekke kromosomene fra hverandre og gå inn i anafase, må en avgjørende kontroll utføres: Er alle kromosomene riktig festet til det mitotiske spindelapparatet?opprettholde genomisk stabilitet og forebygge unormal cellevekst.
En mekanisk og molekylær sjekk
Det mitotiske spindelapparatet består av mikrotubuli som vokser ut fra to motsatte poler i cellen.
Hver søsterkromatid-par må være festet til spindeltråder fra hver sin pol – slik at de senere kan trekkes korrekt fra hverandre.
Dersom et kromosom ikke er ordentlig koblet til, vil ikke separasjonen kunne gjennomføres på en trygg måte.
For å sikre at alt er riktig, har cellen et kontrollsystem kjent som spindelsjekkpunktet. Dette er en slags molekylær kvalitetskontroll som overvåker koblingene mellom mikrotubuli og de spesifikke proteinstrukturene på kromosomene, kalt kinetokorer.
APC/C – det molekylære klarsignalet
Når alle kromosomene er riktig festet og i balanse mellom polene, sendes et signal som aktiverer et stort enzymkompleks kalt Anaphase Promoting Complex/Cyclosome (APC/C).
Dette er en slags biokjemisk bryter som sørger for at cellen kan gå videre til neste fase.
APC/C fungerer ved å merke spesifikke regulatoriske proteiner for nedbrytning via ubiquitinering. Blant de viktigste målene er:
- Securin, som normalt holder enzymet separase inaktivt.
- Visse cykliner, som regulerer CDK-aktivitet og dermed cellesyklusens progresjon.
Når securin brytes ned, frigjøres separase. Dette enzymet kløyver proteinbåndene som holder søsterkromatidene sammen – kjent som cohesin-komplekser. Først da kan kromatidene trekkes fra hverandre mot hver sin cellepol, og anafase er i gang.
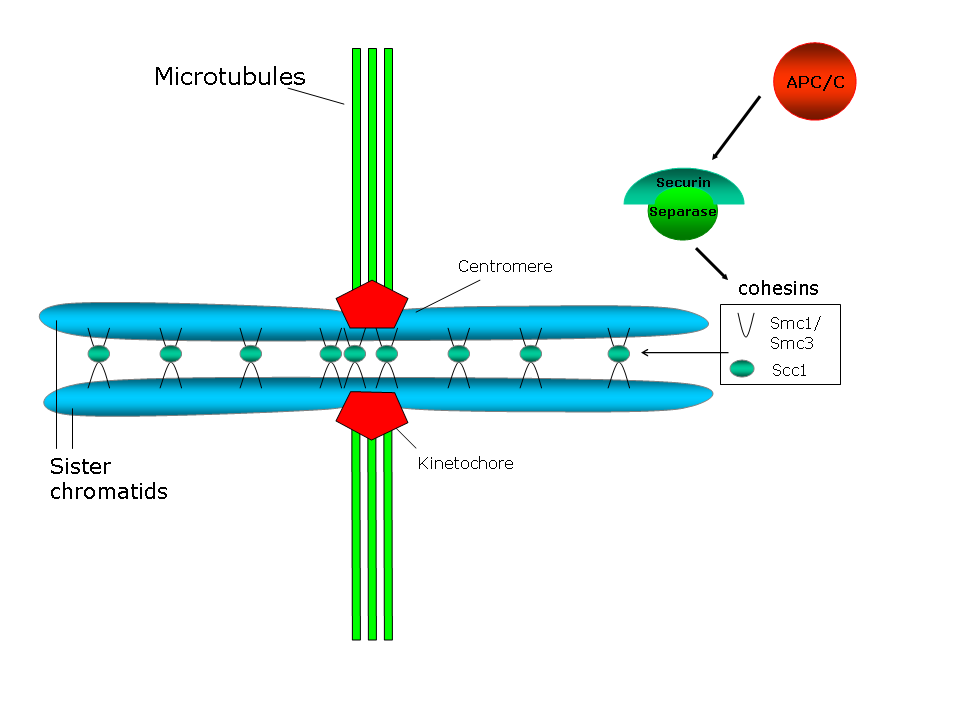
Hvis kromosomene deles feil, kan dattercellene få for mye eller for lite genetisk materiale, noe som kan føre til celledød eller utvikling av genetiske sykdommer og kreft.
Regulering av proteinaktivitet i cellesyklusen
For at cellen skal kunne dele seg trygt og effektivt, må den hele tiden kontrollere når visse proteiner skal være aktive – og når de skal slås av eller fjernes.
Denne reguleringen er helt avgjørende for at cellesyklusen skal gå riktig for seg.
Om ikke, kan det føre til ukontrollert vekst, genetisk ustabilitet og i verste fall kreftutvikling.
Celler bruker flere ulike mekanismer for å styre proteinaktivitet. De tre viktigste er:
- Fosforylering og defosforylering
- Proteinnedbrytning gjennom ubiquitinering
- Inhibitorproteiner
1. Fosforylering og defosforylering – proteinets av/på-bryter
Fosforylering er en kjemisk prosess der en fosfatgruppe festes til et protein, som oftest på aminosyrene serin, treonin eller tyrosin.
Dette gjøres av enzymer som kalles kinaser, og kan enten aktivere eller inaktivere proteinet.
Et eksempel er CDK (cyclin-dependent kinase), som i mange tilfeller må defosforyleres for å bli aktiv.
Det vil si at et fosfat må fjernes – og dette skjer ved hjelp av fosfataser, som for eksempel enzymet Cdc25. Dermed fungerer fosforylering som en fleksibel bryter som kan slå proteiner av og på, avhengig av hva cellen trenger.
2. Proteinnedbrytning – når proteiner må fjernes helt
Noen ganger holder det ikke å skru av et protein – det må brytes helt ned. Dette skjer gjennom en prosess som kalles ubiquitinering. Her festes små proteiner kalt ubiquitin til det uønskede proteinet, som et signal om at det skal destrueres. Det ubiquitinerte proteinet blir deretter fraktet til cellens “søppelsystem”, proteasomet, der det brytes ned til aminosyrer.
Nedbrytningen styres av ubiquitin-ligaser, som er enzymer som hekter ubiquitin på målproteinet. To spesielt viktige ubiquitin-ligaser i cellesyklusen er:
- APC/C (Anaphase Promoting Complex/Cyclosome)
- SCF-komplekset
APC/C er særlig aktiv ved overgangen til anafase, og markerer blant annet sykliner og securin for destruksjon – og dermed gir den klarsignal til at søsterkromatidene kan separeres. Når sykliner brytes ned, reduseres også CDK-aktiviteten, og cellen kan avslutte en fase og gå videre til neste.
3. Inhibitorproteiner – cellens bremseklosser
Celler har også egne proteiner som kan binde seg til CDK-syklin-komplekser og midlertidig hemme aktiviteten deres.
Disse kalles CDK-hemmere (CKI). Eksempler inkluderer:
- p21
- p27
- p16
Disse hemmerne blir spesielt viktige hvis DNA er skadet, eller hvis cellen trenger å stoppe cellesyklusen for å reparere feil før den går videre. Dermed fungerer de som et biologisk bremsesystem – og er avgjørende for å hindre ukontrollert celledeling.
Sykliner og CDK – en dynamisk duo
CDK står for cyclin-dependent kinase, og er sentrale enzymer i reguleringen av cellesyklusen.
Men de fungerer ikke alene – de må binde seg til et syklin for å bli aktivert.
Sykliner er proteiner som ikke har enzymaktivitet selv, men deres viktigste rolle er å binde og aktivere CDK. Når et syklin binder seg til sin spesifikke CDK, endres strukturen på enzymet slik at det kan fosforylere målproteiner.
Men binding til syklin er ikke nok.
CDK må også defosforyleres på riktig sted – for eksempel av Cdc25 – for å bli fullt aktiv. Dermed trengs både binding og kjemisk aktivering.
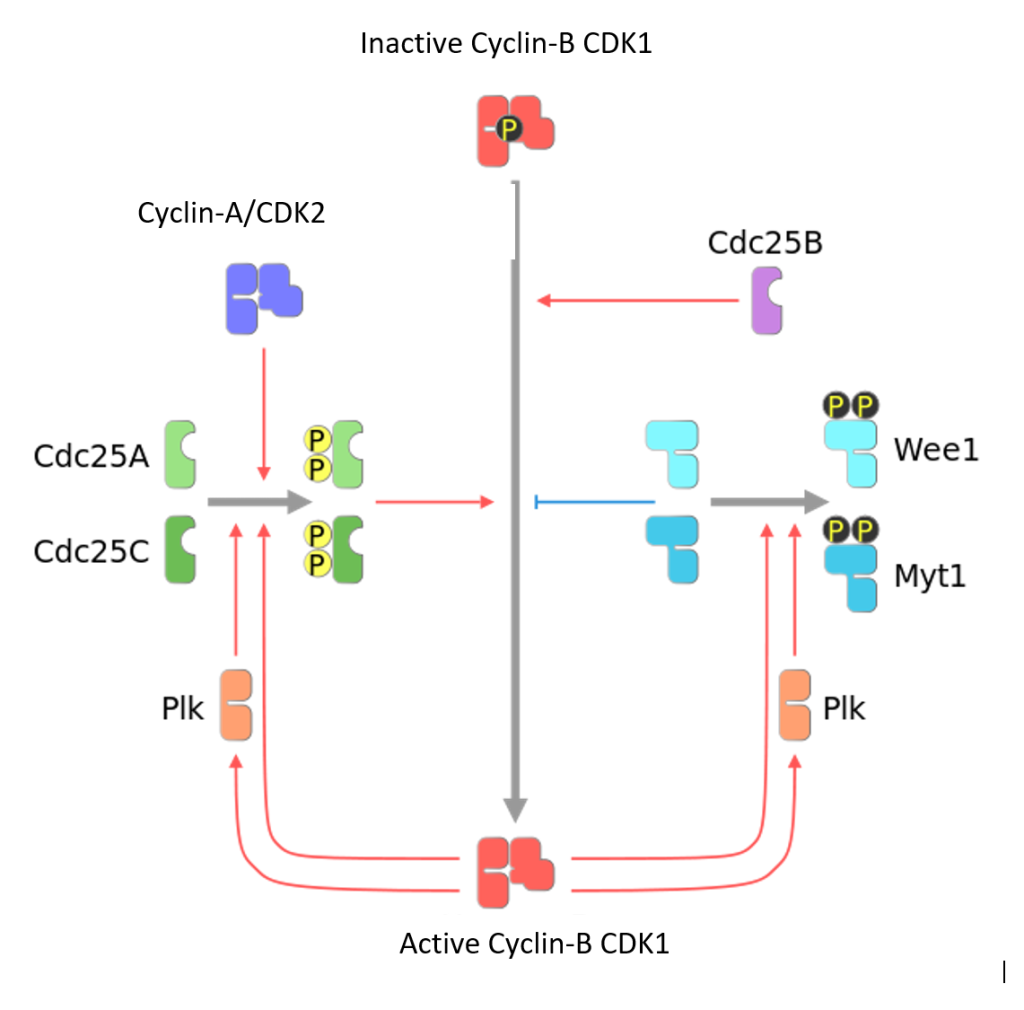
Sykliner kommer og går
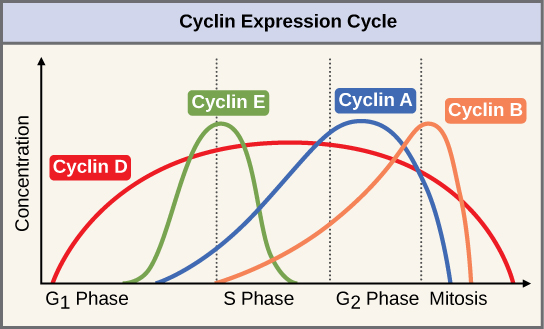
Nivået av sykliner er ikke konstant i cellen. I stedet varierer syklinnivåene gjennom cellesyklusen – et resultat av nøye regulert syntese og nedbrytning:
- Sykliner syntetiseres ved behov, ofte kontrollert av transkripsjonsfaktorer.
- Når de ikke lenger trengs, ubiquitineres de og sendes til proteasomet for nedbrytning.
Et godt eksempel på dette er igjen APC/C, som ved slutten av mitosen merker sykliner for destruksjon. Dette stopper CDK-aktiviteten og lar cellen gå tilbake til start – klar for en ny runde, eller for å gå inn i hvilemodus.
Du kan se det som en dans: CDK er danseren, syklinet er partneren som må være der for at dansen skal fungere – og APC/C er vakten som skrur av musikken når dansen er over.
Kontroll av CDK-aktivitet
CDK-aktivitet reguleres på flere måter:
CDK (Cyclin-Dependent Kinase) er et viktig enzym i cellesyklusen.
Kontrollen av CDK-aktivitet handler om hvordan cellen styrer denne bryteren. Det skjer på to hovedmåter:

Både Wee1 og CKI hemmer CDK-aktivitet!
Wee1 gjør det gjennom fosforylering (en reversibel prosess), mens CKI gjør det gjennom direkte binding til CDK-syklin-komplekser.
CKI er spesielt viktig i G1-fasen, mens Wee1 kan virke på ulike punkter i cellesyklusen.
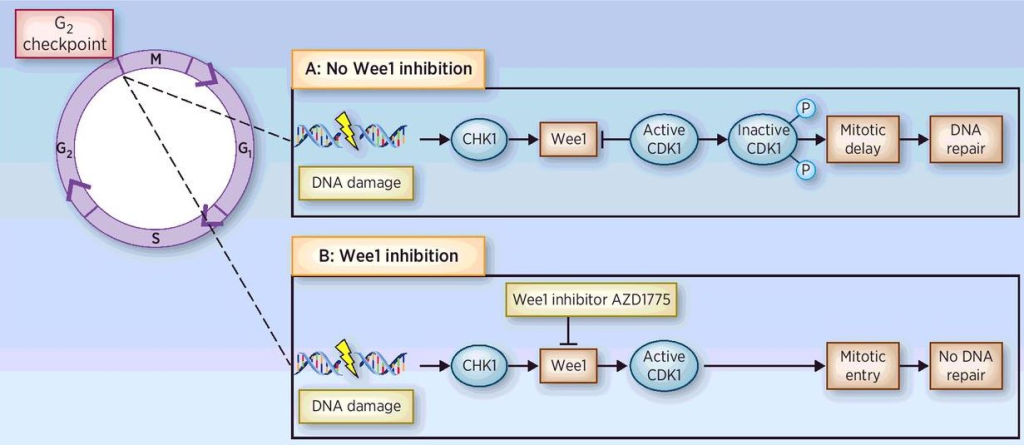
Hvordan eksterne signaler styrer cellesyklusen – veien fra G1 til S-fase
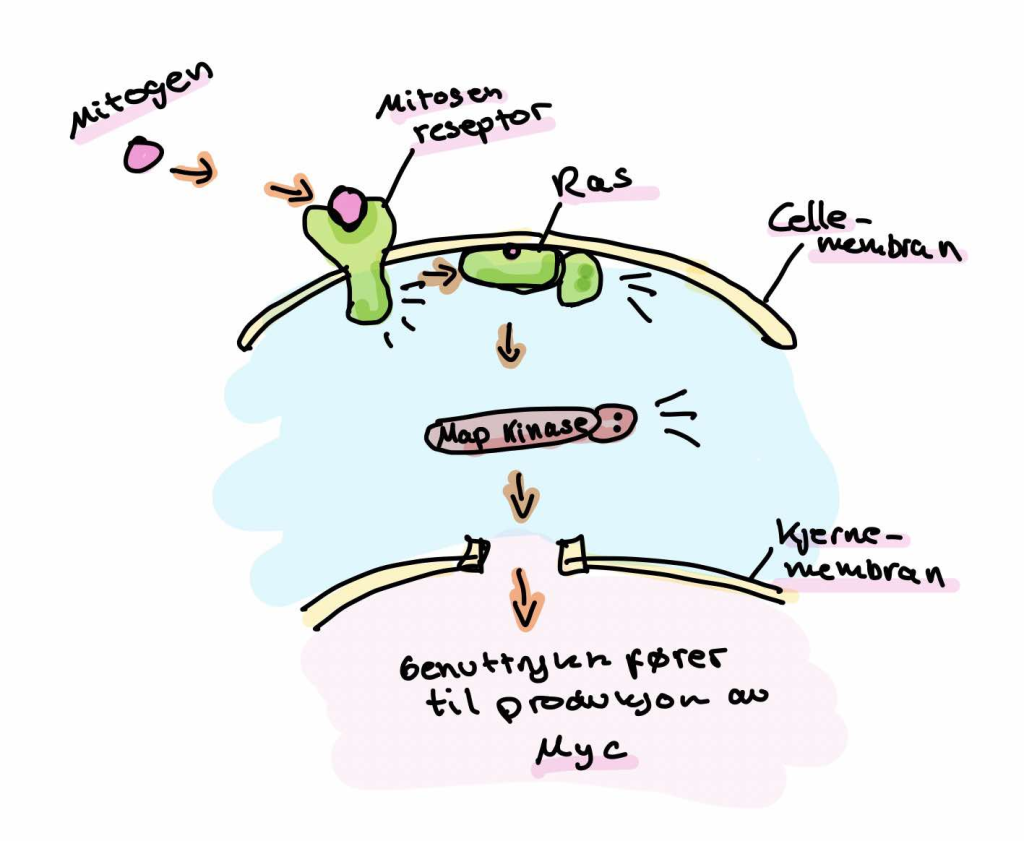
Celler lever ikke isolert. De står i kontinuerlig kontakt med omgivelsene, og tar imot signaler fra vekstfaktorer, naboceller og miljøet. Noen signaler forteller cellen at den skal dele seg – disse kalles mitogener. Men et mitogen alene får ikke cellen til å hoppe rett inn i celledeling. I stedet starter det en hel signal- og reguleringskjede som leder frem mot en viktig beslutning: skal cellen gå videre til DNA-replikasjon og starte S-fasen?
Denne prosessen – overgangen fra G1 til S-fase – er nøye kontrollert og involverer tre overordnede trinn: signaltransduksjon, genregulering og syklusaktivering.
1. Signaltransduksjon – budskapet fanges opp
Det hele starter når et mitogen binder seg til sin spesifikke reseptor på celleoverflaten.
Dette aktiverer en signalkaskade inne i cellen, der Ras-proteinet står sentralt.
Ras videreformidler signalet ved å aktivere en gruppe enzymer kalt MAP-kinaser, som igjen fosforylerer transkripsjonsfaktorer.
Disse fosforylerte faktorene vandrer inn i cellekjernen og setter i gang transkripsjon av gener som trengs for å drive cellen videre.
2. Genregulering – cellekjernen tar styring
I kjernen aktiveres såkalte umiddelbare tidlige gener, som raskt gir opphav til proteiner som Myc – en nøkkelregulator i kontrollen av cellevekst. Myc fungerer som en transkripsjonsfaktor og aktiverer igjen en rekke forsinkede gener, som blant annet koder for komponenter som driver cellesyklusen fremover, deriblant cykliner og CDK-er.
3. Aktivering av cellesyklus
Blant genene som Myc aktiverer, finner vi flere som stimulerer dannelsen av G1-CDK-komplekser.
Disse CDK-ene (for eksempel Cyklin D-CDK4/6) fosforylerer proteinet Rb (Retinoblastoma-protein).
Når Rb er ufosforylert, fungerer det som en bremse: det binder og hemmer transkripsjonsfaktorer som E2F, og forhindrer uttrykk av gener som trengs i S-fasen. Men når Rb fosforyleres, endres dets form og slipper E2F fri.
Frigjort E2F kan da aktivere gener som koder for:
- G1/S-CDK (f.eks. Cyklin E-CDK2)
- S-CDK (f.eks. Cyklin A-CDK2)
- Og andre proteiner som driver DNA-replikasjon
Dermed går cellen fra forberedelse til handling – S-fasen er i gang, og DNA-syntesen starter.
Positiv tilbakekobling
Et viktig kjennetegn ved denne overgangen er positiv tilbakekobling.
Når G1/S-CDK først blir aktiv, fosforylerer den mer Rb, som igjen frigjør mer E2F. Mer E2F betyr enda mer produksjon av cykliner og CDK-er, spesielt Cyklin E, som ytterligere øker CDK-aktiviteten.
Slik skapes en selvforsterkende syklus der aktivering leder til mer aktivering, og CDK-aktiviteten stiger brått. Denne typen tilbakekobling gjør overgangen rask og irreversibel – når cellen først har bestemt seg for å gå videre, er det ingen vei tilbake.
Dette prinsippet gjelder ikke bare for G1/S-overgangen.
Også i overgangen til mitose (M-fase) ser vi liknende mekanismer: CDK-aktivitet stimulerer sin egen forsterkning, noe som sørger for at hele mitosen gjennomføres i ett kraftfullt, koordinert løp.
Hvorfor regulering er helt nødvendig
I en kompleks organisme som mennesket, er det helt avgjørende at cellene kun deler seg når det er behov. Under fosterutvikling er deling nødvendig for vekst. I voksen alder trengs det for vevsreparasjon og for å erstatte celler som naturlig dør – som hudceller eller tarmepitel.
Men ukontrollert celledeling – uten korrekt regulering – er en av hovedårsakene til kreft.
Mange kreftceller har defekter i proteiner som p53, Rb eller CDK-hemmere – og dermed kjører cellesyklusen videre uten kontroll, selv om DNA er skadet.
Medisinsk relevans – når vi angriper cellesyklus
Fordi mange kreftformer skyldes svikt i cellesyklusens regulering, brukes dette som angrepspunkt i moderne behandling.
- Taksaner (f.eks. paklitaksel) er cellegift som hindrer mikrotubuli i å brytes ned. Uten dynamisk omorganisering av mikrotubuli, kan ikke kromosomene separeres i anafase – og cellen dør midt i mitosen. Dette rammer både kreftceller og normale celler som deler seg raskt.
- CDK-hemmere, som palbociklib og ribociklib, brukes i behandling av visse brystkrefttyper. Disse hemmer CDK4 og CDK6, og blokkerer dermed G1/S-overgangen. Resultatet er at cellene stopper opp før de rekker å kopiere DNA-et sitt – og får ikke gjennomført ny deling.
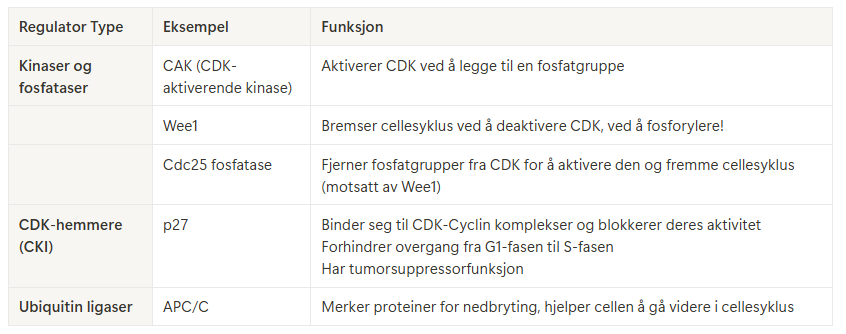
De viktigste regulatorene OVERSIKT
 Anki-kort
Anki-kort
Obs, tomt! Kommer etterhvert <3
 Eksamensoppgaver
Eksamensoppgaver
NTNU
UIO
Obs, her var det tomt! Kommer snart!
 Klinisk case
Klinisk case
Obs, tomt! Kommer etterhvert <3