Nervesystemet er kroppens høyhastighets-kommunikasjonssystem. I motsetning til hormonsystemet, som formidler informasjon langsommere via blodet, overfører nervesystemet signaler i form av elektriske impulser. Disse elektriske signalene kalles aksjonspotensialer, og de gjør det mulig for kroppen å reagere raskt på både ytre og indre stimuli.
Et aksjonspotensial er en rask, forbigående endring i spenningen over cellemembranen til en nervecelle. Dette signalet oppstår først ved aksonhalsen og forplanter seg deretter langs aksonet, helt ut til nerveendene. Der kan det enten overføres videre til en annen nervecelle eller til en effektorcelle, som en muskel- eller kjertelcelle. Det er denne elektriske ledningen som gjør det mulig for deg å trekke hånden vekk fra en varm kokeplate, kjenne et stikk fra en nål eller aktivere en bestemt muskel for å smile.
Den elektriske signaleringen i nervesystemet er preget av tre nøkkelkvaliteter:
- Raskhet: Aksjonspotensialer kan bevege seg med hastigheter opp mot 120 meter per sekund i store, myeliniserte aksoner.
- Presisjon: Signalet er tydelig og nøyaktig – enten sendes det, eller så gjør det ikke. Dette gir lite rom for feiltolkning.
- Lang rekkevidde uten signaltap: Nervefibrene er spesialisert for å sikre at det elektriske signalet kan overføres over lange avstander, helt fra ryggmargen og ut i tærne, uten at det svekkes.
Kliniske eksempler på elektrisk signalering:
- Motornevroner leder elektriske signaler fra ryggmargen til skjelettmuskulaturen, og gjør det mulig å styre frivillige bevegelser som å løfte armen eller gå.
- Sensoriske nevroner overfører signaler fra huden og indre organer tilbake til sentralnervesystemet, slik at vi kan kjenne smerte, temperatur og berøring.
Grunnlaget for elektrisk signalering i nerveceller
Hvordan små ioner skaper store signaler
For at en nervecelle skal kunne sende et elektrisk signal, må det først eksistere en elektrisk spenning over cellemembranen. Denne spenningen – eller potensialforskjellen – oppstår fordi ulike typer ioner er ulikt fordelt mellom innsiden og utsiden av cellen. Forskjellen i ionekonsentrasjoner og membranens selektive gjennomtrengelighet for bestemte ioner gir opphav til et membranpotensial.
Men hva er det egentlig som skaper og opprettholder denne forskjellen? Svaret ligger i ioner, ionekanaler, og aktive transportmekanismer – særlig natrium-kalium-pumpen.
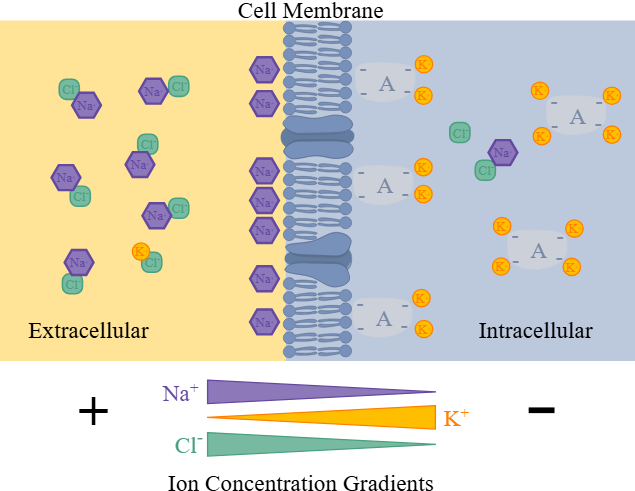
Ioner og deres fordeling
Ioner er elektrisk ladde partikler, og i nervesystemet spiller spesielt fire av dem hovedroller:
| Ion | Mest utenfor eller inni cellen? | Funksjon |
|---|---|---|
| Na⁺ (natrium) | Mest utenfor | Ansvarlig for depolarisering (starter aksjonspotensialet) |
| K⁺ (kalium) | Mest inni | Viktig for hvilemembranpotensialet og repolarisering |
| Ca²⁺ (kalsium) | Svært lavt inni, høyt utenfor | Stimulerer vesikkelfrigjøring og kontraksjon |
| Cl⁻ (klorid) | Mest utenfor | Ofte involvert i inhibisjon (gjør membranen mer negativ) |
Denne fordelingen er ikke tilfeldig. Cellen bruker energi for å opprettholde den, og det skjer gjennom spesialiserte transportproteiner.
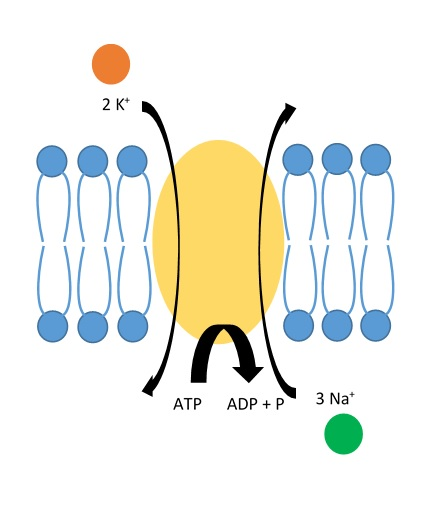
Natrium-kalium-pumpen – den elektriske grunnmuren
Natrium-kalium-pumpen (Na⁺/K⁺-ATPase) er et enzym som forbruker ATP for å pumpe ioner mot konsentrasjonsgradienten. For hvert ATP-molekyl som brukes, transporterer pumpen 3 natriumioner ut og 2 kaliumioner inn. Dette gir to viktige effekter:
- Det dannes og opprettholdes en konsentrasjonsgradient: Mer Na⁺ utenfor cellen, mer K⁺ inni cellen.
- Det skapes en elektrisk ladningsforskjell: Fordi flere positive ladninger fjernes enn det som tas inn, blir innsiden av cellen mer negativ enn utsiden.
Pumpen jobber kontinuerlig i bakgrunnen og er helt essensiell for at nervecellen skal være klar til å sende signaler. Uten denne pumpen ville ionekonsentrasjonene jevnes ut, og nervesignalene ville opphøre.
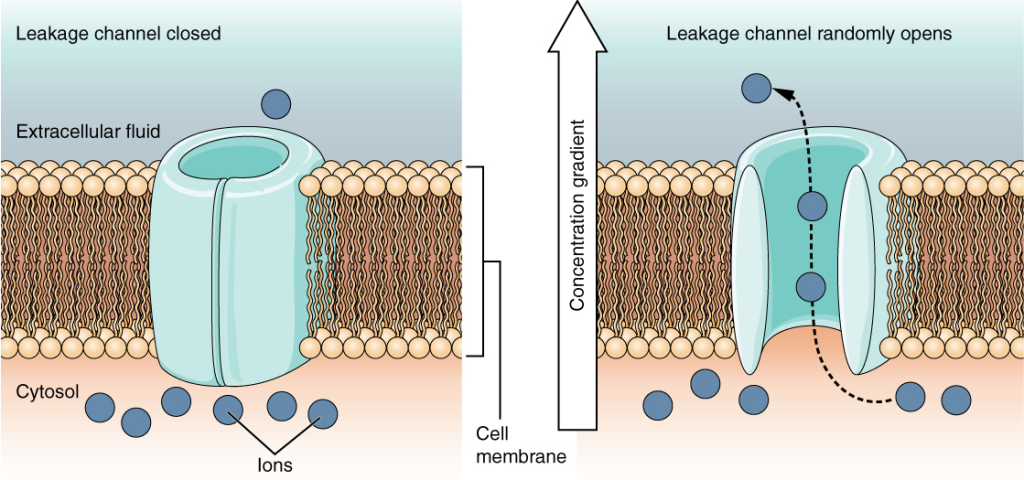
Ionekanaler – cellemembranens porter
Selv om membranen er en tett barriere for ioner, finnes det spesialiserte proteiner som lager små, selektive åpninger – ionekanaler. Disse gjør det mulig for ioner å bevege seg ned sine elektrokjemiske gradienter uten bruk av energi. Kanalene er ekstremt spesifikke:
- Kaliumkanaler slipper nesten bare K⁺ gjennom.
- Natriumkanaler er bygget for Na⁺.
- Kalsiumkanaler er svært selektive for Ca²⁺.
Ionekanalene finnes i flere varianter:
- Lekkasjekanaler: Alltid åpne – særlig kaliumkanaler, som forklarer hvorfor cellen er mest permeabel for K⁺ i hvile.
- Ligandstyrte kanaler: Åpnes når et signalstoff, som f.eks. acetylkolin, binder seg til kanalen.
- Mekanisk styrte kanaler: Åpnes av fysisk trykk eller strekk.
- Spenningsstyrte kanaler: Åpnes når membranpotensialet når en bestemt terskelverdi – disse er helt avgjørende for aksjonspotensialet.
Gjennom samspillet mellom ionepumper og kanaler bygges det opp et hvilemembranpotensial, og det legges grunnlaget for alt som skal skje videre i nervesignalet.
Membranpotensialet
Hvordan ladningsforskjellen mellom innsiden og utsiden av cellen skaper elektrisk spenning
Alle levende celler har en elektrisk spenning over cellemembranen – et såkalt membranpotensial. For nerveceller er dette spesielt viktig, fordi det danner grunnlaget for at cellen kan sende elektriske signaler. Membranpotensialet skyldes ulik fordeling av ioner mellom celleinnsiden og utsiden, og at membranen er selektivt permeabel for disse ionene.
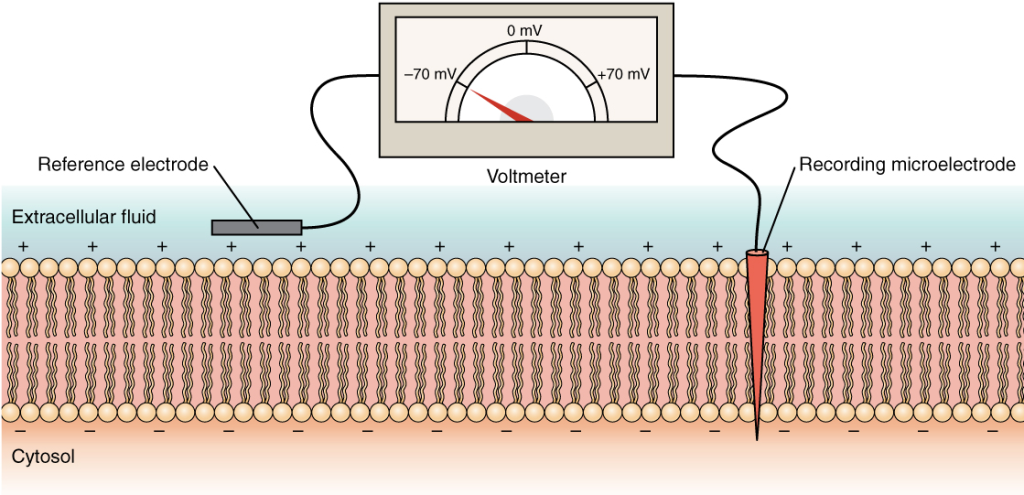
Hvilemembranpotensialet
Når en nervecelle ikke sender signaler, sier vi at den er i hvile. I denne tilstanden opprettholdes et stabilt membranpotensial, typisk rundt –70 millivolt (mV). Det betyr at innsiden av cellen er negativ i forhold til utsiden.
Dette hvilepotensialet oppstår hovedsakelig fordi:
- Kaliumioner (K⁺) lekker ut av cellen via åpne lekkasjekanaler, ettersom det er høyere K⁺-konsentrasjon inni cellen enn utenfor.
- Når K⁺ strømmer ut, etterlater det negative ladninger (f.eks. proteiner og fosfater) inne i cellen.
- Etter hvert som flere K⁺ forlater cellen, bygges det opp en negativ ladning på innsiden som motvirker ytterligere utstrømming – til en likevekt oppstår.
Membranen i hvile er mest permeabel for K⁺ – det er derfor hvilemembranpotensialet ligger nær K⁺ sitt likevektspotensial, som er ca. –75 mV.
Samtidig lekker det litt Na⁺ inn i cellen, men dette motvirkes aktivt av Na⁺/K⁺-pumpen, som opprettholder ionefordelingen.
🧠 Kort oppsummert: Hvilemembranpotensialet skyldes hovedsakelig K⁺-lekkasje ut av cellen og Na⁺/K⁺-pumpeaktivitet som holder ionefordelingen stabil.
Likevektspotensialet og Nernst-ligningen
For hvert ion finnes det en bestemt spenning der det er i elektrisk og kjemisk likevekt. Dette kalles likevektspotensialet (Eₓ). For K⁺ er det som nevnt rundt –75 mV, og for Na⁺ er det omtrent +55 mV.
Likevektspotensialet beregnes ved hjelp av Nernst-ligningen:
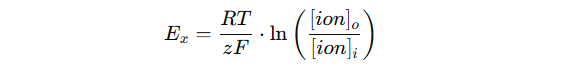
Der:
- Eₓ = likevektspotensial for ionet
- R = gasskonstant
- T = absolutt temperatur
- z = ionets valens (ladning)
- F = Faradays konstant
- [ion]o = konsentrasjon utenfor cellen
- [ion]i = konsentrasjon inni cellen
I praksis bruker vi Nernst-ligningen til å forstå hva som ville skjedd med membranpotensialet hvis cellen kun var permeabel for ett bestemt ion.
Endringer i membranpotensial
Membranpotensialet er ikke statisk – det kan endres, og dette er nøkkelen til nervesignalering.
- Depolarisering: Membranpotensialet blir mindre negativt (f.eks. fra –70 mV til –50 mV). Dette skjer vanligvis når Na⁺ strømmer inn i cellen. Dersom depolariseringen er stor nok til å nå terskelverdi, starter et aksjonspotensial.
- Hyperpolarisering: Membranpotensialet blir mer negativt enn hvilenivået (f.eks. –80 mV). Dette reduserer cellens evne til å fyre av et nytt aksjonspotensial.
- Repolarisering: Etter at cellen har vært depolarisert, må den gå tilbake til hvilepotensial. Dette skjer når K⁺ strømmer ut av cellen.
Elektrokjemiske krefter
Ioners bevegelser over membranen styres av to krefter:
- Konsentrasjonsgradienten: Ionene beveger seg fra høy til lav konsentrasjon.
- Elektrisk kraft: Positivt ladde ioner tiltrekkes av negativt ladede områder, og motsatt.
Kombinasjonen av disse to kalles den elektrokjemiske gradienten. For eksempel:
- K⁺ vil strømme ut fordi det er mye av det inni cellen, men den negative ladningen inni trekker det tilbake.
- Na⁺ vil strømme inn, fordi det er både høyere konsentrasjon ute og innsiden er negativ.
📌 Derfor: Hvilemembranpotensialet er resultatet av en balanse mellom passive strømmer av ioner og aktiv pumping, hovedsakelig styrt av K⁺-permeabilitet.
Aksjonspotensialet
Et aksjonspotensial er en kortvarig, eksplosiv endring i membranpotensialet som sprer seg langs aksonet og overfører informasjon. Det fungerer som en digital «av/på»-bryter – enten skjer det, eller så gjør det ikke. Aksjonspotensialet er selve grunnen til at vi kan bevege oss, sanse omgivelsene, oppfatte smerte og kommunisere mellom celler i kroppen.
I hvile er nervecellen negativ på innsiden. Når et signal når et visst terskelnivå, endres dette brått: innsiden blir positiv i løpet av noen millisekunder før den repolariseres og går tilbake til hvile.
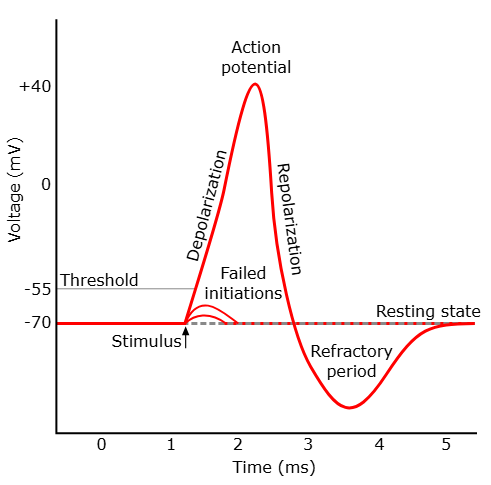
Hvordan aksjonspotensialet starter og forplanter seg
Alt starter med en depolarisering, for eksempel ved at en nevrotransmitter binder seg til en reseptor og slipper inn Na⁺ gjennom ligandstyrte kanaler. Dersom nok Na⁺ kommer inn, og membranpotensialet når en terskelverdi (rundt –55 mV), skjer det noe dramatisk:
- Spenningsstyrte natriumkanaler åpner seg plutselig.
- Na⁺ strømmer inn i cellen – både fordi det er mer Na⁺ på utsiden, og fordi innsiden er negativ.
- Membranpotensialet skyter raskt opp mot +30 mV – dette er depolariseringen.
Deretter skjer en like rask repolarisering:
- Na⁺-kanalene lukkes og inaktiveres.
- Spenningsstyrte kaliumkanaler åpner seg, og K⁺ strømmer ut av cellen.
- Dette fører membranpotensialet tilbake mot hvileverdi.
Etter repolarisering får vi en kortvarig hyperpolarisering fordi K⁺-kanalene forblir åpne litt for lenge. Til slutt lukkes de også, og membranpotensialet stabiliseres igjen på hvilenivå.
🔄 Hele denne syklusen – fra start til slutt – tar bare noen få millisekunder.
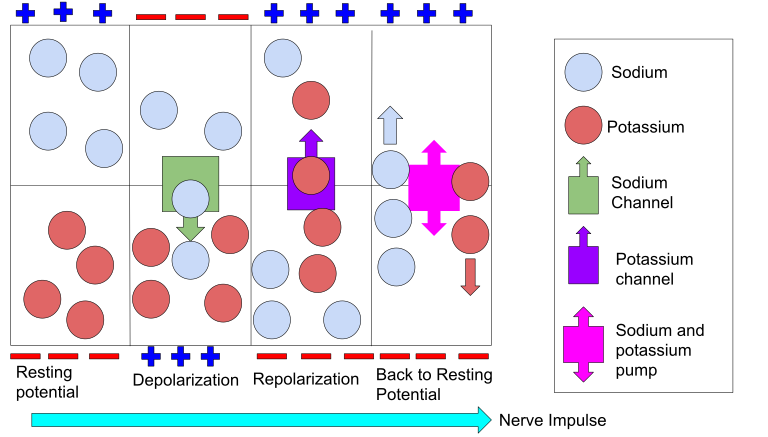
Fornyelse av aksjonspotensialet langs aksonet
Et viktig trekk ved aksjonspotensialet er at det ikke svekkes over avstand, til tross for at det reiser hele veien fra ryggmargen til tærne. Dette er mulig fordi signalet regenereres i hver del av aksonet.
Når Na⁺ strømmer inn i én del av aksonet, blir området ved siden av også depolarisert. Dermed åpnes spenningsstyrte Na⁺-kanaler der, og aksjonspotensialet «hopper» videre. Dette gir en bølge av elektrisk aktivitet som brer seg hurtig nedover aksonet.
I myeliniserte aksoner, hvor axonet er omgitt av isolerende myelinskjeder, skjer dette spesielt raskt. Her finnes spenningsstyrte Na⁺-kanaler bare ved ranvierske innsnøringer (små åpne områder mellom myelinskjeder). Aksjonspotensialet «hopper» fra én innsnøring til den neste – en prosess kalt saltatorisk ledning. Det er dette som gjør ledningen opptil 100 ganger raskere enn i umyeliniserte fibre.
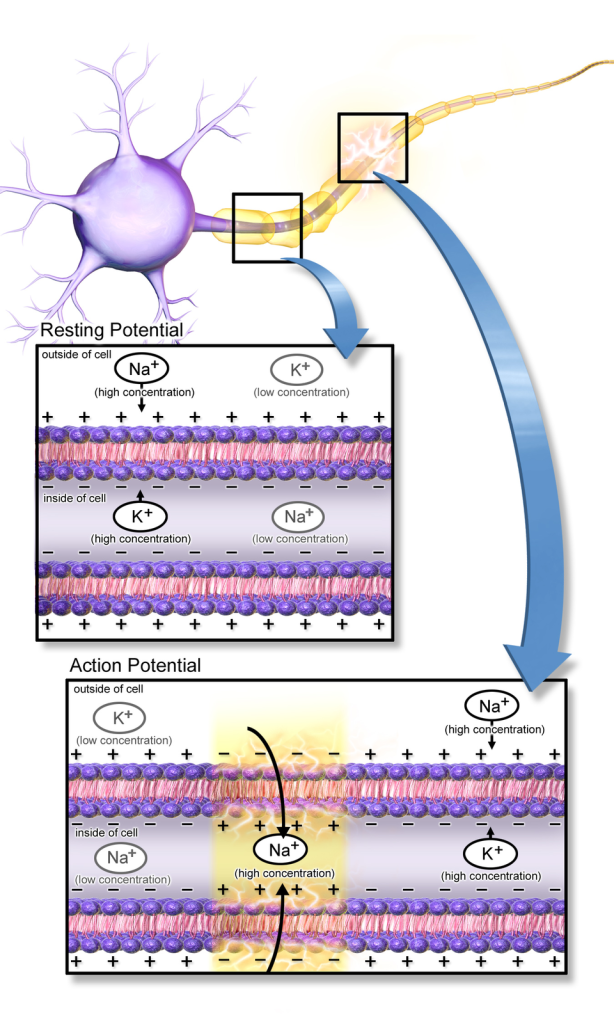
De ulike fasene i aksjonspotensialet
Det finnes seks karakteristiske faser i aksjonspotensialet, som kan vises i en typisk spenningskurve:
- Hvilemembranpotensial (–70 mV): Kalium-lekkasjekanaler og Na⁺/K⁺-pumpen holder cellen stabil.
- Terskelverdi nås (–55 mV): Et lite stimuli åpner noen spenningsstyrte Na⁺-kanaler.
- Depolarisering: Mange Na⁺-kanaler åpnes, og Na⁺ strømmer inn.
- Toppfase (+30 mV): Na⁺-innstrømningen stopper – kanalene inaktiveres.
- Repolarisering: K⁺ strømmer ut gjennom åpne K⁺-kanaler.
- Hyperpolarisering: K⁺-kanalene lukkes litt for sent, og cellen blir mer negativ enn hvile. Dette gir en midlertidig relativ refraktærperiode.
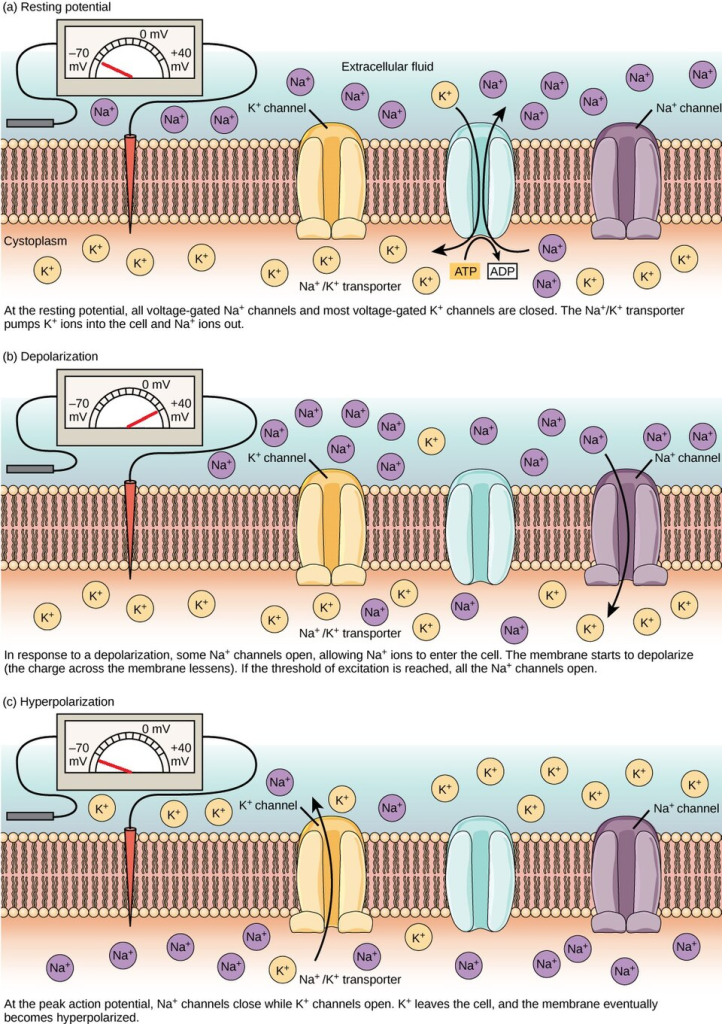
Refraktærperiodene – når cellen ikke kan fyre igjen
Etter et aksjonspotensial trenger nervecellen en kort pause. Dette kalles refraktærperiode, og den deles i to:
- Absolutt refraktærperiode: I denne fasen er Na⁺-kanalene inaktive, og et nytt aksjonspotensial er umulig – uansett hvor sterkt stimuli er.
- Relativ refraktærperiode: K⁺-kanaler er fortsatt åpne, og cellen er hyperpolarisert. Et nytt aksjonspotensial kan fyres, men det krever sterkere stimuli enn vanlig.
Disse periodene sikrer at signalet bare går én vei og at nervecellen ikke overaktiveres.
Synaptisk transmisjon
Hvordan nervesignalet hopper fra én celle til en annen
Aksjonspotensialet har beveget seg hele veien nedover aksonet, men hva skjer når det når enden? Her må signalet videre – til neste nervecelle, til en muskelcelle eller til en kjertel. Dette skjer i en synapse, en spesialisert kontaktflate der signalet overføres fra én celle til en annen. Denne prosessen kalles synaptisk transmisjon.
Synaptisk transmisjon kan være elektrisk eller kjemisk, men i menneskekroppen er det kjemisk signaloverføring som er dominerende – spesielt i sentralnervesystemet og i muskulaturen.
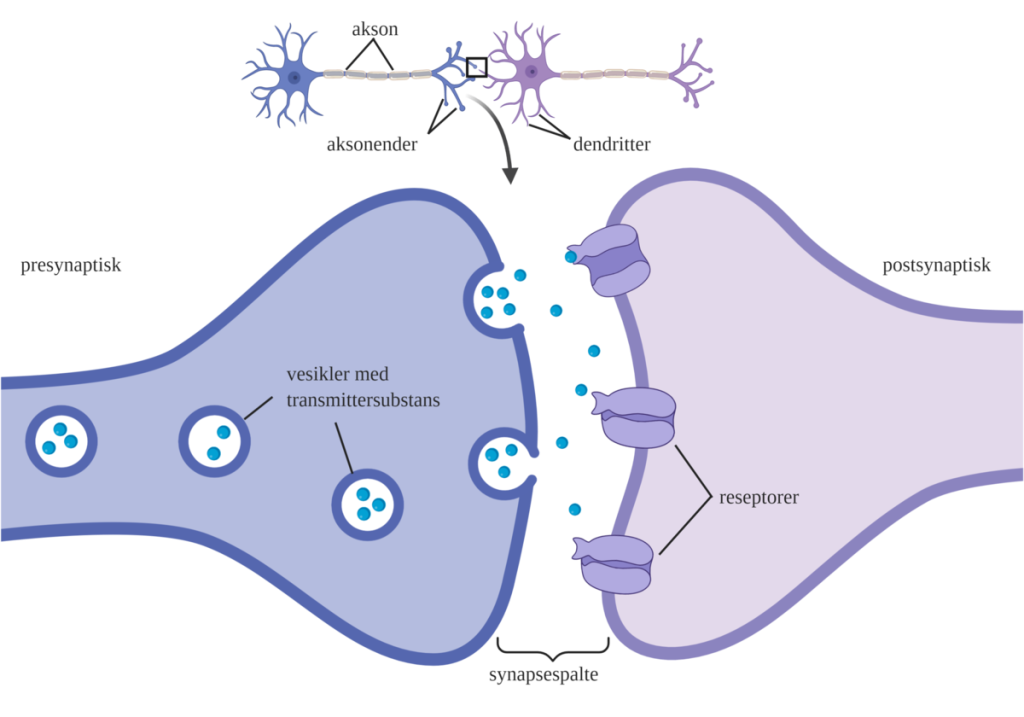
Synapsens struktur
En kjemisk synapse består av tre hoveddeler:
- Presynaptisk membran – enden av aksonet som sender signalet
- Synaptisk kløft – det smale mellomrommet mellom de to cellene
- Postsynaptisk membran – mottakersiden, enten en annen nervecelle, en muskelcelle eller en kjertel
Her frigjøres kjemiske signalstoffer, kalt nevrotransmittere, som diffunderer over kløften og binder seg til reseptorer på den postsynaptiske membranen.
Fra elektrisk signal til kjemisk overføring
Synaptisk transmisjon i kjemiske synapser kan deles inn i flere trinn:
a) Presynaptiske hendelser – signalet ankommer
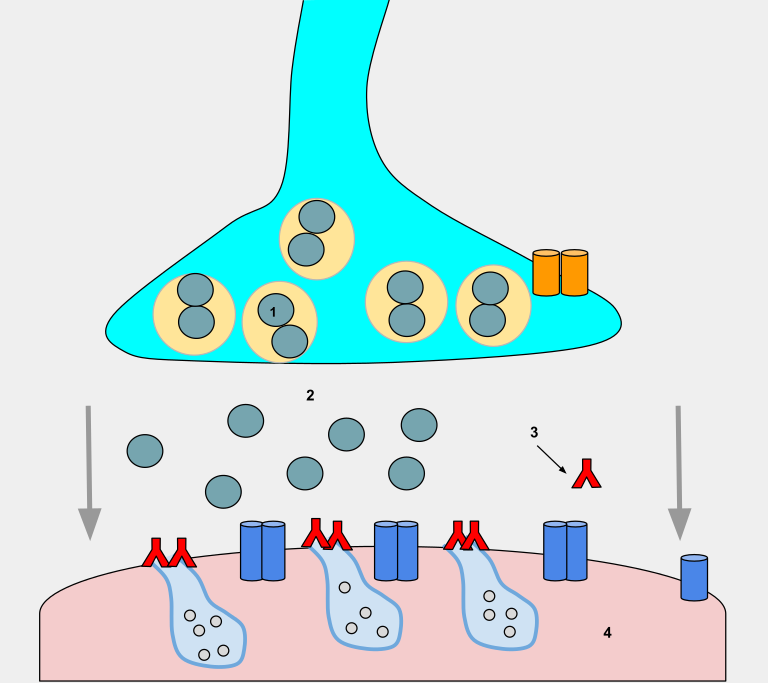
Når aksjonspotensialet når den presynaptiske terminalen, skjer en rask depolarisering av membranen der. Dette åpner spenningsstyrte kalsiumkanaler (VGCC), som slipper Ca²⁺ inn i nerveenden.
Ca²⁺ fungerer som et viktig signalmolekyl. Når det strømmer inn, starter det en kjedereaksjon som fører til at små blærer, synaptiske vesikler, smelter sammen med cellemembranen. Disse vesiklene inneholder nevrotransmittere, og når de smelter med membranen, tømmes innholdet ut i synapsespalten. Denne prosessen kalles eksocytose.
b) I synaptisk kløft – signalet diffunderer
Nevrotransmitterne beveger seg passivt over den synaptiske kløften og binder seg til reseptorer på mottakercellen. Dette skjer svært raskt – på bare millisekunder.
c) Postsynaptiske hendelser – hva skjer på mottakersiden?
Nevrotransmittere binder seg til spesifikke reseptorer, og disse kan være av to hovedtyper:
- Ionotrope reseptorer: Disse er ligandstyrte ionekanaler. Når nevrotransmitteren binder seg, åpnes kanalen umiddelbart, og ioner strømmer inn eller ut av cellen. Dette gir en rask endring i membranpotensialet.
- Metabotrope reseptorer: Disse er G-protein-koblede reseptorer. Når de aktiveres, starter de en intracellulær signalvei som til slutt kan åpne ionekanaler eller endre cellens respons på annen måte. Dette tar litt lengre tid, men gir mer langvarige og modulære effekter.
Eksitatoriske og inhibitoriske synapser
Alt avhenger av hvilke ioner som strømmer og hvilke reseptorer som aktiveres:
- Eksitatoriske postsynaptiske potensialer (EPSP) oppstår når membranen depolariseres – ofte ved at Na⁺ strømmer inn. Dette gjør det lettere å utløse et nytt aksjonspotensial.
- Inhibitoriske postsynaptiske potensialer (IPSP) oppstår når membranen hyperpolariseres – f.eks. når Cl⁻ strømmer inn eller K⁺ strømmer ut. Dette gjør det vanskeligere å nå terskel og hemmer fyring.
Fjerning av nevrotransmittere
Etter at signalet er overført, må nevrotransmitteren fjernes raskt for å unngå vedvarende stimulering. Dette skjer på tre måter:
- Enzymatisk nedbrytning: Eksempel: acetylkolin brytes ned av acetylkolinesterase.
- Reopptak: Nevrotransmitteren tas aktivt opp igjen i den presynaptiske terminalen og resirkuleres.
- Diffusjon: Noen molekyler driver bort og forsvinner ut av synapsen.
Nevrotransmittere og deres reseptorer
Nevrotransmittere er kroppens egne signalmolekyler, og de brukes for å formidle informasjon mellom nerveceller og mellom nerveceller og andre celletyper, som muskel- og kjertelceller. Når en elektrisk nerveimpuls når den presynaptiske enden av et nevron, settes en kjede av hendelser i gang som ender med at nevrotransmittere frigjøres i synapsespalten. Disse molekylene diffunderer raskt over til mottakersiden, hvor de binder seg til spesifikke reseptorer i cellemembranen på den postsynaptiske cellen. Hvordan cellen svarer, avhenger både av hvilken nevrotransmitter som er involvert og hvilken reseptor som aktiveres.
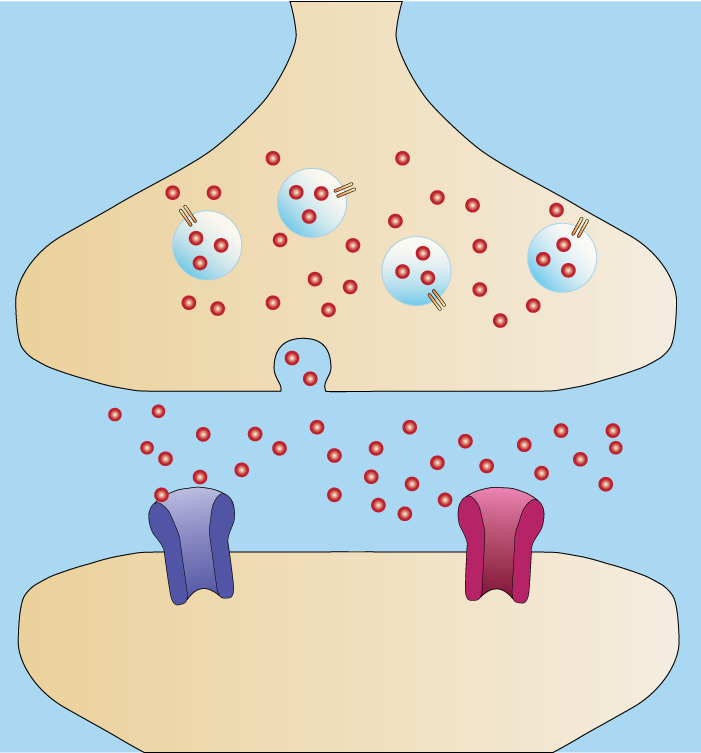
De mest kjente nevrotransmitterne i sentralnervesystemet er små molekyler som produseres og lagres i nerveendene. Disse virker raskt og har ofte kortvarig effekt. Et eksempel er glutamat, som er den mest utbredte eksitatoriske nevrotransmitteren i hjernen. Når glutamat binder seg til reseptorer på den postsynaptiske cellen, åpnes ionekanaler for natrium og kalsium.
Dette gjør innsiden av cellen mindre negativ – altså en depolarisering – som øker sannsynligheten for at cellen skal fyre et nytt aksjonspotensial.
Glutamat kan aktivere både ionotrope reseptorer som AMPA- og NMDA-reseptorer, og metabotrope glutamatreseptorer som virker gjennom intracellulære signalveier og har en mer modulert virkning.
I motsatt ende av skalaen finner vi GABA – gamma-aminosmørsyre – som er den viktigste inhibitoriske nevrotransmitteren i hjernen. Når GABA binder seg til sine reseptorer, åpnes vanligvis kloridkanaler. Dette fører til at negative kloridioner strømmer inn i cellen, som gjør membranpotensialet mer negativt. Dermed blir det vanskeligere å nå terskelverdien for et nytt aksjonspotensial.
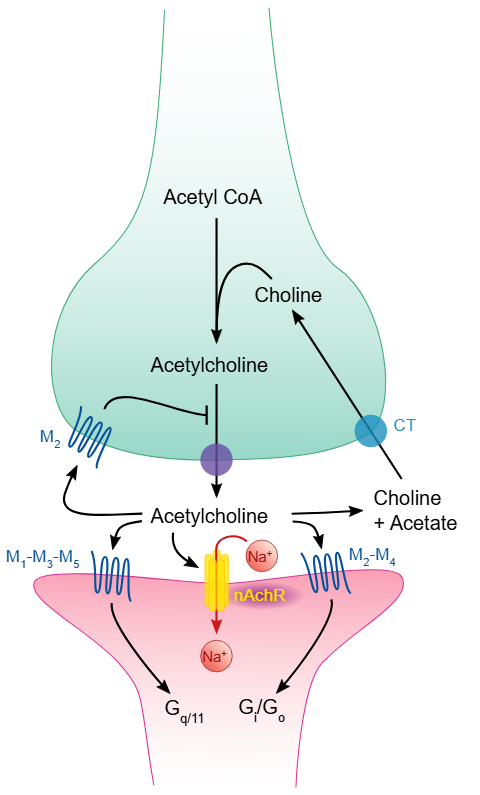
Acetylkolin er en tredje, svært viktig nevrotransmitter, som har sentrale funksjoner både i det somatiske og det autonome nervesystemet.
I den nevromuskulære overgangen spiller acetylkolin hovedrollen når det gjelder å overføre signalet fra motornevronet til muskelfiberen. Her binder acetylkolin seg til nikotinreseptorer, som er ionotrope og gir en rask og effektiv åpning av natriumkanaler i muskelmembranen. I det autonome nervesystemet og i hjernen kan acetylkolin også virke gjennom muskarinreseptorer, som er metabotrope og medfører mer langsomme og langvarige effekter.
I tillegg til de små molekylene har vi en annen klasse signalstoffer som kalles neuropeptider. Disse er større, ofte mer komplekse, og finnes i et stort antall varianter – faktisk over hundre forskjellige er kjent. I motsetning til de små nevrotransmitterne dannes neuropeptider i cellekroppen, og de transporteres i vesikler langs aksonet før de lagres i nerveenden. Når de frigjøres, virker de i hovedsak via metabotrope reseptorer og gir mer langvarige, ofte mer diffuse effekter på målcellen.
Et eksempel på et slikt neuropeptid er substans P, som finnes i sensoriske nerver og spiller en viktig rolle i smerteoverføring. Et annet er VIP – vasoaktivt intestinalt peptid – som påvirker blodkar og glatt muskulatur, særlig i tarmen. Enkefaliner og endorfiner er også peptider, og de virker gjennom kroppens egne opioidreseptorer for å dempe smerte og redusere stress.
Den nevromuskulære transmisjonen
Nevromuskulær transmisjon er prosessen som kobler nervesystemet til musklene og gjør bevegelse mulig. Denne typen synapse, mellom en motorisk nervecelle og en muskelfiber, er et av de mest studerte og best forståtte eksemplene på synaptisk signaloverføring. Det er her nervesystemets elektriske språk oversettes til mekanisk kontraksjon.
Fra motornevron til muskelfiber
En motorisk nervecelle har sitt cellelegeme i ryggmargen og sender ut et langt akson som forgreiner seg ut i kroppen. Hver gren av dette aksonet ender i kontakt med én enkelt muskelfiber. Kontaktpunktet mellom en motorisk nerve og en muskelfiber kalles muskelendeplaten, og hele enheten – én motorisk nerve og alle muskelfibrene den kontrollerer – omtales som en motorisk enhet.
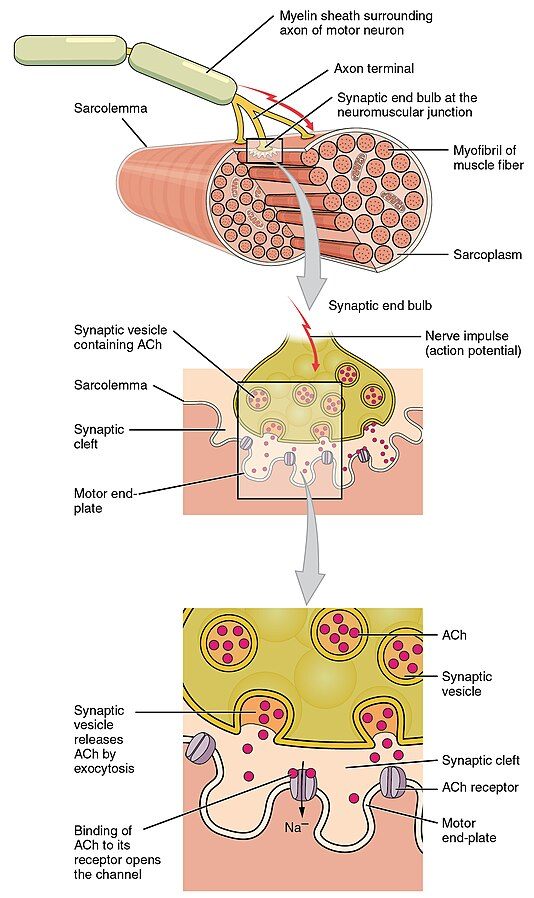
I enden av nervegrenen danner aksonet små knopper, såkalte boutoner, som ligger tett inntil muskelcellens membran, men uten direkte kontakt. Mellomrommet mellom nerve og muskel kalles den synaptiske spalten.
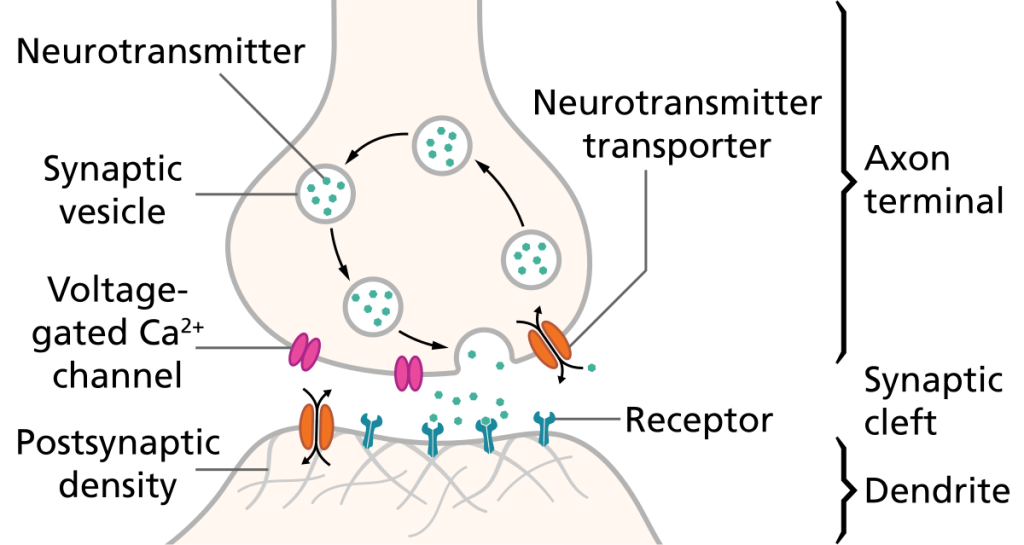
Den elektriske impulsen ankommer
Når et aksjonspotensial beveger seg nedover det motoriske aksonet og når boutonene, depolariseres membranen. Dette åpner spenningsstyrte kalsiumkanaler i nerveendene, og kalsiumioner strømmer inn. Denne kalsiuminnstrømningen er signalet som trengs for at vesikler fylt med acetylkolin skal smelte sammen med den presynaptiske membranen og slippe innholdet sitt ut i synapsespalten – altså eksocytose.
Acetylkolin diffunderer raskt over spalten og binder seg til nikotinerge reseptorer på muskelcellens overflate. Disse reseptorene fungerer som ligandstyrte ionekanaler, og når acetylkolin binder seg, åpnes kanalene og slipper natriumioner inn i muskelcellen. Dette skaper en lokal depolarisering – et såkalt endeplatepotensial.
Hvis dette potensialet når terskelnivået, utløses et fullt aksjonspotensial i muskelfiberen. Dette aksjonspotensialet brer seg raskt over muskelmembranen og ned i små innbuktninger kalt T-tubuli, som sørger for at signalet når dypt inn i cellen.
Signalet i T-tubuli aktiverer spenningssensorer som er koblet til kalsiumlagre inne i muskelen – det sarkoplasmatiske retikulum. Kalsium slippes ut i cytosol, og når dette kalsiumet binder seg til troponin, skjer det en strukturell endring som gjør at tropomyosin flyttes til side. Dette eksponerer bindingssetene for myosin på aktinfilamentene, og en serie av «power strokes» kan starte – muskelen trekker seg sammen.
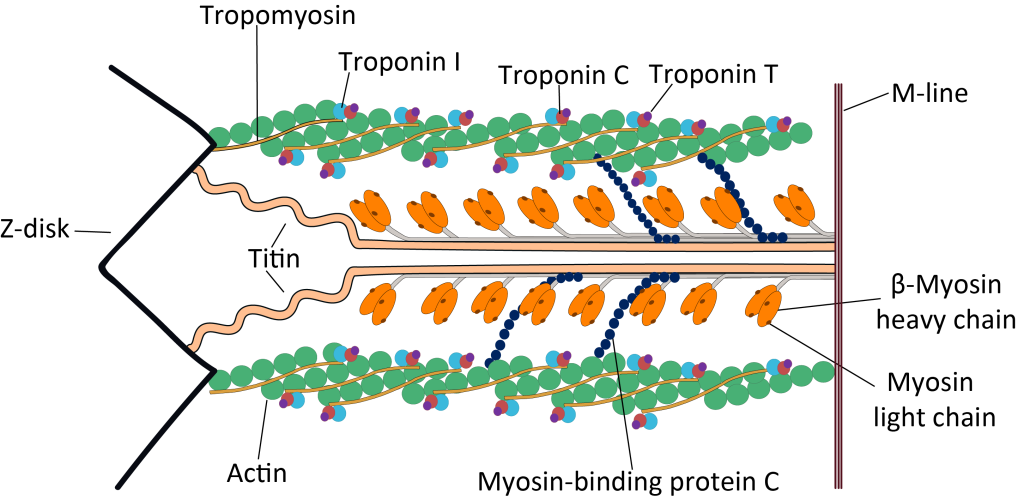
Avslutning og forberedelse til neste signal
Etter at signalet er sendt og muskelen har trukket seg sammen, må systemet nullstilles. Acetylkolin fjernes raskt fra synapsespalten, hovedsakelig ved hjelp av enzymet acetylkolinesterase, som bryter det ned til inaktive komponenter.
Disse tas opp igjen og brukes til å lage nytt acetylkolin.
Samtidig pumpes kalsium tilbake inn i det sarkoplasmatiske retikulum, og tropomyosin dekker igjen bindingsstedene på aktin. Muskelen slapper av – klar til neste nerveimpuls.
Klinisk relevans: sykdommer og stoffer som påvirker nevromuskulær transmisjon
Når signalet ikke kommer frem – og hva som skjer når det gjør for mye
Nevromuskulær transmisjon er normalt en presis og pålitelig prosess, men den kan forstyrres på flere nivåer. Både sykdomstilstander og visse toksiner kan påvirke signaloverføringen mellom nervecelle og muskelfiber. Resultatet kan være svakhet, lammelser eller ukontrollerte muskelkontraksjoner – alt avhengig av hvor i prosessen ting går galt.
Myasthenia Gravis
Myasthenia Gravis er en autoimmun sykdom hvor kroppens immunsystem angriper reseptorene for acetylkolin på muskelfibrenes overflate. Dette skjer typisk ved at antistoffer binder seg til nikotinreseptorene og enten blokkerer dem eller bidrar til at de blir ødelagt. Når færre reseptorer er tilgjengelige, blir den postsynaptiske responsen svekket, og det kreves mer acetylkolin for å utløse et nytt aksjonspotensial i muskelfiberen.
Dette gir karakteristiske symptomer på muskelsvakhet, særlig i musklene som brukes ofte og over tid. Øyelokk, ansiktsmuskler, svelg og respirasjonsmuskler rammes gjerne først. Et typisk trekk er at svakheten forverres ved aktivitet og bedres ved hvile – det motsatte av hva vi ser ved mange andre nevromuskulære sykdommer.
Behandlingen retter seg ofte mot å hemme nedbrytningen av acetylkolin ved å gi medikamenter som blokkerer enzymet acetylkolinesterase. Dermed økes konsentrasjonen av acetylkolin i synapsespalten, og selv om reseptorene er færre, øker sannsynligheten for at de aktiveres.
Lambert-Eaton myastenisk syndrom
I Lambert-Eaton myastenisk syndrom (LEMS) ligger problemet på den presynaptiske siden. Også her er årsaken en autoimmun prosess, men denne gangen rettes antistoffene mot de spenningsstyrte kalsiumkanalene i nerveenden. Når disse kanalene blokkeres, kommer det mindre kalsium inn når et aksjonspotensial ankommer nerveenden. Uten tilstrekkelig kalsium, frigjøres det også mindre acetylkolin.
Pasienter med LEMS opplever muskelsvakhet, men til forskjell fra Myasthenia Gravis, forbedres symptomene gjerne ved aktivitet. Forklaringen er at gjentatte aksjonspotensialer gradvis øker kalsiuminnholdet i nerveenden, slik at det til slutt frigjøres nok acetylkolin til å oppnå en synaptisk effekt. Sykdommen forekommer ofte som paraneoplastisk syndrom ved småcellet lungekreft, og det er viktig med grundig utredning ved nyoppdaget LEMS.
Botulinumtoksin
Botulinumtoksin – kjent fra både kosmetikk og nevrologi – produseres av bakterien Clostridium botulinum. Dette toksinet virker ved å hemme selve eksocytoseprosessen i den presynaptiske nerveterminalen. Det gjør dette ved å ødelegge spesifikke proteiner som er nødvendige for at vesiklene med acetylkolin skal kunne smelte sammen med cellemembranen. Når eksocytosen stopper opp, frigjøres ikke lenger acetylkolin, og den postsynaptiske muskelfiberen får ikke beskjed om å trekke seg sammen.
Resultatet er midlertidig lammelse av de aktuelle musklene. Ved kosmetisk bruk injiseres små doser av toksinet i ansiktsmuskler for å redusere mimikk og dermed glatte ut rynker. I medisinsk sammenheng brukes botulinumtoksin også mot tilstander med overdreven muskelaktivitet, som dystoni eller spastisitet.
Organofosfater og nervegasser
Noen giftstoffer virker i motsatt retning av botulinumtoksin. I stedet for å hemme acetylkolinfrigjøring, blokkerer de nedbrytningen. Dette gjelder særlig organofosfater, som finnes i enkelte plantevernmidler og i nervegasser som Novichok. Disse stoffene hemmer enzymet acetylkolinesterase, som normalt bryter ned acetylkolin raskt etter frigjøring. Når enzymet hemmes, akkumuleres acetylkolin i synapsespalten.
Konsekvensen er at musklene stimuleres kontinuerlig, noe som fører til kramper, ukontrollert sekresjon, pustestans og i verste fall død. Behandling innebærer både å motvirke den kolinerge overstimuleringen og å forsøke å reaktivere det hemmede enzymet – ofte med legemidler som atropin og pralidoksim.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3
❓ Test deg selv
Obs, tomt! Kommer etterhvert <3