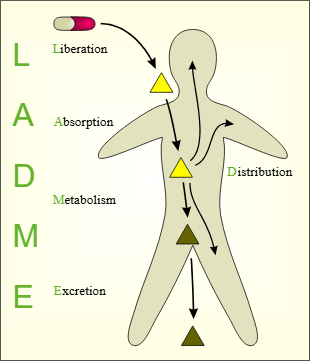
ADME
ADME og toksisitet på cellenivå
Når et giftstoff kommer inn i kroppen, starter en reise. Det er ikke nok at et stoff i seg selv er skadelig; det må faktisk nå cellene, overleve kroppens egne forsvarssystemer og være i stand til å påvirke biologiske prosesser.Først da kan det gjøre skade. For å forstå dette, må vi følge stoffet gjennom fire hovedfaser, ofte omtalt med forkortelsen ADME: absorpsjon, distribusjon, metabolisme og ekskresjon.
Disse fasene utgjør grunnmuren i toksikologiens forståelse av hvordan et fremmedstoff oppfører seg i kroppen – og dermed også hvordan vi vurderer hvor farlig det egentlig er.
Absorpsjon – veien inn i kroppen
Det første steget i denne reisen er absorpsjon.
Det handler rett og slett om hvordan stoffet kommer seg fra utsiden av kroppen og over i blodbanen.
Dette kan skje på flere måter: gjennom magesekken eller tarmen hvis stoffet er svelget, via lungene dersom det pustes inn, eller gjennom huden dersom det kommer i kontakt med kroppens overflate.
Noen stoffer absorberes lett fordi de er fettløselige og glir gjennom cellemembraner som smør.
Andre møter mer motstand – for eksempel store, vannløselige molekyler som ikke passer like lett gjennom membranen.
Distribusjon – hvor stoffet havner
Når stoffet først er inne i kroppen, fraktes det med blodet til ulike vev og organer. Dette kalles distribusjon. Men stoffet havner ikke tilfeldig – det tiltrekkes av visse vev mer enn andre, avhengig av både stoffets kjemiske egenskaper og kroppens egne mekanismer.
Fettløselige stoffer samler seg gjerne i fettvev, mens andre stoffer har affinitet for organer med høy blodgjennomstrømning, som lever og nyrer.
Noen stoffer binder seg til plasmaproteiner og sirkulerer passivt, mens andre trekker inn i cellene og begynner å virke.
Metabolisme – kroppens forsøk på å uskadeliggjøre
Kroppen forsøker å beskytte seg selv.
Et viktig ledd i dette er metabolismen – også kjent som biotransformasjon.
I denne fasen, som foregår hovedsakelig i leveren, bryter kroppen ned fremmede stoffer for å gjøre dem lettere å skille ut.
Målet er å gjøre stoffene mer vannløselige, slik at de kan skilles ut med urin eller galle.
Men denne omdannelsen har en bakside. I mange tilfeller blir stoffet mindre aktivt og mindre farlig, men noen ganger dannes det reaktive metabolitter – stoffer som er mer toksiske enn det opprinnelige molekylet. Ironisk nok kan altså kroppens egne avgiftningsmekanismer være med på å skape skade.
Ekskresjon – ut med det
Til slutt må kroppen kvitte seg med det som er igjen. Dette skjer gjennom ekskresjon – det vil si utskillelse. De fleste giftstoffer og metabolitter skilles ut gjennom nyrene, og havner i urinen. Andre kan skilles ut gjennom gallen, og sendes videre til tarmen, mens noen stoffer pustes ut gjennom lungene. Hvor raskt og effektivt kroppen kvitter seg med stoffet, har stor betydning for hvor mye skade det rekker å gjøre.
Hva skjer når stoffet når cellen?
Dersom et giftstoff kommer seg helt frem til cellene og ikke skilles ut i tide, begynner neste kapittel i toksisitetens historie: cellulær skade.
Dette handler ikke bare om celledød.
Faktisk er det ofte mer subtilt – små forstyrrelser som likevel får store konsekvenser. Cellene våre er avhengige av balanse: de må kunne sende signaler, produsere proteiner, kopiere DNA, og opprettholde struktur.
Giftstoffer kan forstyrre alt dette.
En celle kommuniserer med andre celler og med sitt indre miljø.
Den bruker signalmolekyler som hormoner, nevrotransmittere og second messengers som cAMP for å regulere prosesser som vekst, metabolisme og immunrespons.
Toksiske stoffer kan blokkere eller overaktivere disse signalene. Resultatet? Kaos i cellens styringssystem. Dette kan føre til hormonforstyrrelser, nevrologiske symptomer, eller ubalanser i immunforsvaret.
Celler er bygget opp av proteiner, lipider og nukleinsyrer.
Disse komponentene er sårbare.
Toksiske stoffer kan denaturere proteiner slik at de mister sin funksjon, oksidere lipider i cellemembranen slik at den lekker eller kollapser, eller skade DNA, slik at mutasjoner oppstår. Over tid kan slike skader føre til celledød, feil i celledeling, eller kreftutvikling.
Noen giftstoffer påvirker hvordan genene uttrykkes – altså hvordan DNA oversettes til funksjonelle proteiner.
Dette kan føre til at cellen går inn i programmert celledød (apoptose), eller det kan føre til ukontrollert cellevekst, som igjen kan utvikle seg til kreft.
Jo oftere en celle deler seg, desto større er risikoen – derfor er fostervev og stamceller særlig utsatt.
Noen ganger er skaden midlertidig. Cellen klarer å hente seg inn igjen, reparere det som er ødelagt, og gjenoppta sine normale funksjoner.
Dette kalles dysfunksjon – en reversibel tilstand.
Men hvis skaden blir for stor, eller hvis livsviktige strukturer går tapt, er det ingen vei tilbake.
Da oppstår irreversibel skade, og cellen går enten til grunne eller fungerer permanent dårlig.
Mekanismene bak celletoksisitet
Giftstoffer kan påvirke cellen på ulike nivåer:
Signalnettverk: Cytokiner, hormoner og synaptisk signalering svekkes, med konsekvenser for immunforsvar, vekst og nervefunksjon.
De biokjemiske prosessene: Enzymer hemmes, proteinsyntese stopper opp, energiproduksjonen svikter.
Cellemodning og differensiering: Umodne celler er ekstra sårbare, spesielt i fosterlivet.
Celleadhesjon: Cellenes evne til å binde seg til hverandre og til vevet svekkes – noe som truer hele vevsstrukturen.
Cytoskjelettet: Cellens indre reisverk brytes ned hvis balansen forstyrres, for eksempel ved feil i kalsiumregulering.
Hvordan giftstoffer krysser cellemembranen
For at et giftstoff skal kunne gjøre skade, må det først inn i cellen.
Det betyr at det må krysse cellemembranen, som fungerer som en selektiv portvakt. Måten stoffet kommer seg inn på, avhenger i stor grad av hva slags stoff det er, og hvilke transportmekanismer cellen har tilgjengelig.
Fettløselige stoffer har en stor fordel: de kan bevege seg rett gjennom membranen ved passiv diffusjon. Så lenge det er mer stoff utenfor cellen enn inni, vil molekylene bevege seg med konsentrasjonsgradienten og diffundere fritt gjennom membranen. Dette går raskt og krever ingen energi.
For vannløselige eller polare stoffer er det ikke like enkelt. De trenger hjelp, og får det i form av spesialiserte transportproteiner. I fasilitert diffusjon gjenkjenner et transportprotein det aktuelle molekylet og lar det slippe inn – fortsatt uten at cellen må bruke energi. Dette er viktig for mange biologisk aktive stoffer, som for eksempel glukose.
Noen ganger må cellen derimot aktivt jobbe for å ta opp eller skille ut stoffer.
I slike tilfeller snakker vi om aktiv transport.
Dette er en energikrevende prosess som bruker ATP for å frakte molekyler mot konsentrasjonsgradienten. Denne typen transport er avgjørende for å opprettholde indre balanse, spesielt i nyrer, lever og nervevev.
For større molekyler og partikler finnes det også løsninger. Cellen kan rett og slett omslutte stoffet og trekke det inn ved hjelp av endocytose. Når større partikler som bakterier tas opp, kalles det fagocytose. Når det er væske og små løste stoffer, snakker vi om pinocytose.
Evnen et stoff har til å krysse cellemembranen påvirkes også av pH i miljøet rundt. Svake syrer, som benzosyre, er uladede og fettløselige i sure omgivelser – for eksempel i magesekken – og tas derfor lett opp der.
I mer basiske miljøer blir de ladet, og opptaket reduseres.
Svake baser, som anilin, oppfører seg motsatt: de tas lettere opp i basisk miljø, som i tynntarmen.
Ioniserte (ladede) molekyler har generelt vanskelig for å komme seg gjennom membranen ved passiv diffusjon.
De trenger derfor hjelp av transportproteiner.
Det betyr at pH kan avgjøre hvor i kroppen et giftstoff tas opp best – og at samme stoff kan være harmløst i ett vev, men toksisk i et annet.
Proteinbinding, biotransformasjon og toksisitet
Ikke alle fremmede stoffer i kroppen er umiddelbart toksiske.
Faktisk er det ofte bare en liten brøkdel av et stoff som er biologisk aktivt – og det er nettopp denne frie fraksjonen som avgjør hvor mye skade det kan gjøre.Resten kan være bundet til transportproteiner i blodet, og i bundet tilstand er stoffene inaktive. Først når de løsner, kan de diffundere over cellemembraner, påvirke cellenes funksjon og utløse toksiske effekter.
I blodet finnes flere slike transportproteiner.
Albumin er det mest kjente, og binder seg til en rekke legemidler og kjemikalier. Transferrin og ceruloplasmin spiller også viktige roller i transporten av spesifikke stoffer.
Disse proteinene fungerer som en slags kjemisk buffer, og holder den frie konsentrasjonen av potensielt toksiske forbindelser lav.
Dette er kroppens måte å beskytte seg selv på – ved å holde stoffene «pakket inn» og utilgjengelige for cellene.
Men balansen er skjør.
Dersom et annet stoff konkurrerer om samme bindingssete, kan det forskyve det opprinnelige molekylet og øke den frie fraksjonen i blodet.
Dette kan føre til akutt toksisitet, selv om total mengde av stoffet i kroppen ikke har endret seg.
Et kjent klinisk eksempel på dette er legemidlet warfarin, som binder seg sterkt til albumin.
Ved samtidig bruk av enkelte andre legemidler kan warfarin fortrenges, noe som fører til økt fri konsentrasjon i blodet – og dermed økt risiko for alvorlige blødninger.
Det er derfor viktig å forstå at høy proteinbinding kan gi en viss beskyttelse mot akutt toksisitet, men samtidig kan det forlenge virkningstiden.
Stoffene frigis gradvis, og kroppen utsettes for en forlenget eksponering, noe som kan være problematisk i kliniske sammenhenger – særlig ved kronisk eksponering eller ved svekket evne til utskillelse.
Biotransformasjon
Når kroppen først skal kvitte seg med et toksisk stoff, skjer det i hovedsak gjennom prosessen vi kaller biotransformasjon.
Dette er kroppens kjemiske avgiftningssystem, og det foregår hovedsakelig i leveren. Her gjennomgår stoffet en rekke enzymatiske reaksjoner som gjør det mer vannløselig og dermed lettere å skille ut med urin eller galle.
Biotransformasjon deles gjerne inn i to faser.
Fase I – Transformasjon
I fase I skjer det en kjemisk omforming av molekylet.
Dette kan være gjennom oksidasjon, reduksjon eller hydrolyse.
De viktigste enzymene i denne fasen tilhører cytokrom P450-familien (CYP450), men også enzymer som alkoholdehydrogenase, glutationperoksidase og esterases er involvert. m
Målet er ofte å gjøre molekylet mer reaktivt, ved å introdusere funksjonelle grupper som -OH eller -NH₂.
Dette gjør stoffet klart for neste steg, men det innebærer også en risiko: noen ganger dannes det metabolitter som er mer toksiske enn det opprinnelige stoffet.
Et klassisk eksempel er paracetamol, hvor en av metabolittene – NAPQI – kan forårsake alvorlig leverskade hvis det ikke raskt nøytraliseres.
Fase II – Konjugering
Etter fase I følger fase II, også kalt konjugeringsfasen.
Her kobles det reaktive molekylet til en vannløselig gruppe, som glukuronsyre, sulfat, glutation eller glysin.
Dette gjør stoffet mye lettere å skilles ut – enten med urinen via nyrene, eller med gallen via leveren.
En kjent reaksjon er glukuronidering, som også brukes i elimineringen av bilirubin. Andre viktige prosesser er sulfatering, som blant annet benyttes for å bryte ned steroidhormoner.
Til sammen utgjør fase I og II kroppens viktigste forsvarslinje mot toksiske forbindelser.
Men dette systemet er sårbart.
Hvis leveren er syk, eller enzymene hemmes av andre stoffer, kan giftstoffene hope seg opp. Da fungerer ikke avgiftningen som den skal, og det oppstår risiko for alvorlige toksiske reaksjoner – selv ved doser som normalt ville vært ufarlige.
Når giftstoffer virker sammen
I virkeligheten blir vi sjelden utsatt for bare ett toksisk stoff av gangen.
Kroppen eksponeres ofte for en hel cocktail av kjemikalier – fra medisiner og miljøgifter til matrester og forurensning.
Når flere slike stoffer er til stede samtidig, kan de påvirke hverandres effekt. Resultatet kan bli at effekten øker, svekkes, eller endres totalt.
Dette kaller vi interaksjoner mellom toksiske stoffer, og de kan ha stor klinisk betydning.
En vanlig form for interaksjon er den additive effekten.
Her virker to stoffer sammen på en måte som rett og slett summerer seg.
Hvis det ene stoffet gir en effekt på to, og det andre på tre, gir de til sammen fem. Det er enkelt, men viktig.
Mange smertestillende legemidler virker på denne måten, for eksempel paracetamol og ibuprofen, som begge demper smerte og betennelse – og sammen gir de en forutsigbar, kumulativ effekt.
Mer dramatisk er det når interaksjonen er synergistisk.
I slike tilfeller er totalen langt større enn summen av delene.
To stoffer som hver for seg har moderat effekt, kan sammen føre til alvorlig toksisitet. Et kjent og farlig eksempel er kombinasjonen av alkohol og benzodiazepiner.
Hver for seg virker de dempende på nervesystemet, men sammen kan de føre til dyp sedasjon og livstruende respirasjonsdepresjon – selv i doser som ellers ville vært trygge.
Noen ganger kan et stoff uten egne toksiske egenskaper forsterke et annet.
Dette kalles potentiering.
Stoffet som i utgangspunktet er «nøytralt», påvirker kroppens evne til å håndtere et annet toksisk stoff – for eksempel ved å hemme eliminasjonen eller aktivere en farligere metabolitt.
Et eksempel er isopropanol, som ikke er svært giftig i seg selv, men som kan øke toksisiteten til visse løsemidler ved å forstyrre kroppens avgiftning.
Og så finnes det heldigvis også antagonisme – situasjoner der ett stoff reduserer eller opphever effekten av et annet.
Dette er selve grunnlaget for mye av behandlingen ved forgiftninger. Når pasienter har fått i seg opioider i farlige mengder, gir vi nalokson, som blokkerer opioidreseptorene og redder liv. Eller vi kan gi aktivt kull for å binde toksiner i mage-tarmkanalen før de rekker å bli absorbert.
Eksponering over tid: eliminering og dosering
Konsentrasjonen av et stoff i kroppen er ikke statisk.
Den endrer seg over tid, avhengig av hvor raskt stoffet elimineres, og hvor ofte det tilføres.
Dette utgjør det vi kaller en eksponeringsprofil, og forståelsen av denne er avgjørende både i toksikologi og ved legemiddelbehandling.
Et sentralt begrep i denne sammenhengen er halveringstid – tiden det tar før konsentrasjonen av et stoff reduseres til halvparten.
Stoffets eliminasjonshastighet bestemmer hvor lenge det forblir i kroppen etter en enkeltdose. Noen stoffer har kort halveringstid og forsvinner raskt. Andre elimineres så langsomt at de kan bli værende i kroppen i måneder eller til og med år.
Ved gjentatt dosering blir eliminasjon og administreringsfrekvens to sider av samme sak.
Dersom et stoff gis oftere enn det rekker å elimineres, kan det akkumulere i kroppen, og konsentrasjonen øker gradvis for hver dose.
Dette er særlig viktig for stoffer med lang halveringstid, der selv små doser kan hope seg opp og nå toksiske nivåer over tid.
Et stoff som elimineres raskt, derimot, forlater kroppen mellom hver dose, og det er lite risiko for akkumulering. Men dette betyr også at man må gi stoffet oftere for å opprettholde en stabil og terapeutisk konsentrasjon.
Forskjellen blir tydelig når man sammenligner enkelt- og flerdoseprofiler. Etter én enkelt dose synker konsentrasjonen gradvis med tiden.
Hvis stoffet har lang halveringstid, som for eksempel ett år, forsvinner det nesten ikke i det hele tatt – og kan ligge latent i kroppen.
Et stoff med middels halveringstid, som én dag, representerer et mer balansert bilde, slik vi ofte ser ved vanlige legemidler.
Og stoffer med svært kort halveringstid, under doseringsintervallet, forsvinner før neste dose gis.
Når dosene gjentas, ser vi tydelig hvordan halveringstiden avgjør graden av opphopning.
Lang halveringstid gir fare for kumulativ toksisitet.
Moderat halveringstid gir stabil konsentrasjon ved jevn dosering. Og kort halveringstid gir minimalt med opphopning, men krever til gjengjeld hyppigere administrasjon.
Uansett hva slags stoff det er snakk om, er det altså kombinasjonen av eliminasjonshastighet og doseringsfrekvens som avgjør hvordan kroppen påvirkes over tid – og om grensen mellom virkning og toksisitet blir krysset.
Dose, respons og individuell toksisitet
Et stoff er ikke nødvendigvis giftig i seg selv – det er dosen og individets følsomhet som avgjør om skade oppstår.
Dette er et grunnprinsipp i toksikologi: alle stoffer kan være ufarlige i små mengder og giftige i store, og mennesker reagerer ulikt.
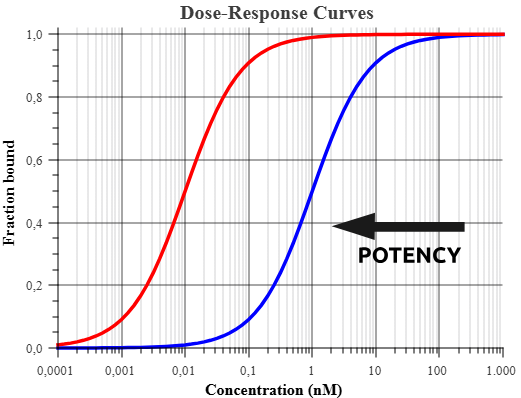
Sammenhengen mellom dose og toksisk effekt kan vises i en dose-respons-kurve, der man ser hvordan effekten øker med økende dose.
Noen stoffer har en tydelig terskelverdi, under hvilken ingen skade oppstår. Andre stoffer – som enkelte nevrotoksiner og hormonforstyrrende kjemikalier – kan være toksiske selv i svært små mengder, uten noen trygg nedre grense.
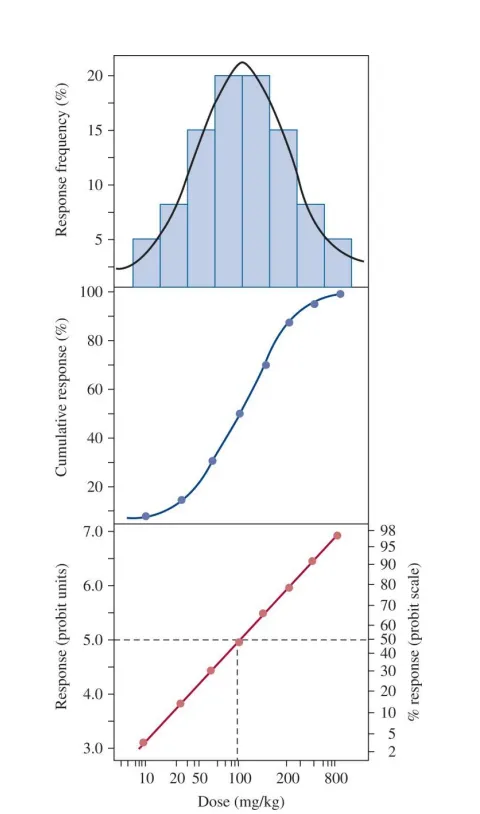
Når man vurderer dose-respons på gruppenivå, brukes ofte kvantal dose-respons-analyser.
Her ser man ikke på graden av effekt i hvert individ, men på hvor mange som reagerer i det hele tatt ved en gitt dose – altså en «alt eller ingenting»-respons. Dette skiller seg fra graderte kurver, der effekten øker trinnvis.
Mennesker er forskjellige, og denne variasjonen i følsomhet følger ofte en normalfordeling. I en slik fordeling vil omtrent 68 % av befolkningen respondere innenfor én standardavvik, over 95 % innenfor to, og så videre.
For å gjøre analysene mer håndterbare, kan man bruke probit-enheter eller NED (Normal Equivalent Deviations), som gjør det mulig å tegne en rett linje og lettere sammenligne data mellom grupper.
Effekt og dose
I toksikologi skiller vi mellom begrepene dose–effekt og dose–respons, og forskjellen ligger i hva vi måler.
Effekt viser til graden av endring i ett individ, for eksempel hvor mye blodtrykket senkes ved økende dose, mens respons viser til andelen individer i en populasjon som får en bestemt reaksjon, som kvalme eller død.
Dose–effekt brukes altså for å vurdere hvor sterk virkningen er i ett individ, mens dose–respons handler om hvor mange som reagerer ved ulike doser.
Variasjonene i følsomhet kan være store. Hyperfølsomme individer reagerer allerede ved svært lave doser, mens resistente individer trenger mye høyere eksponering før de får samme effekt. Slike forskjeller skyldes blant annet genetikk, enzymaktivitet, alder, sykdom og andre fysiologiske faktorer.
I toksikologisk forskning er det vanlig å angi dosen som trengs for å gi en gitt respons hos 50 % av en testet populasjon.
Dette oppgis som ED50 for ønsket effekt, TD50 for toksisk effekt, og LD50 for letal (dødelig) effekt.
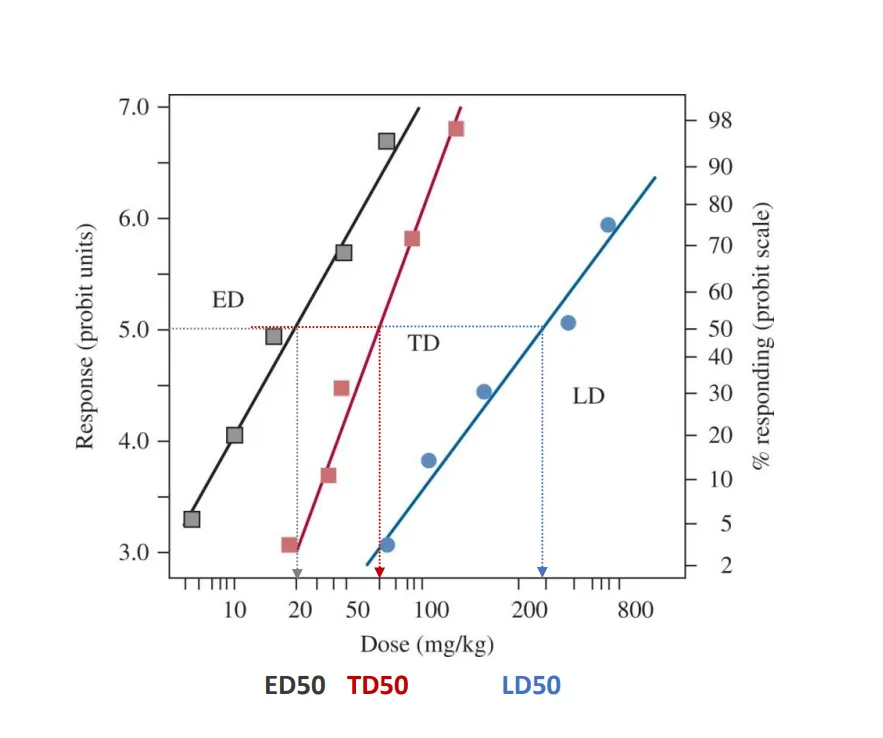
Disse verdiene gir et bilde av hvor kraftig og farlig et stoff er.
For legemidler brukes også begrepet terapeutisk indeks (TI), som er forholdet mellom TD50 og ED50.
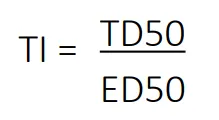
Jo høyere dette forholdet er, desto større er avstanden mellom den dosen som virker og den dosen som gir bivirkninger – og dermed desto tryggere er legemidlet.
Noen legemidler har høy terapeutisk indeks, som penicillin, som tåles godt selv ved høye doser. Andre, som warfarin, har en lav TI og krever tett overvåking. Hos slike legemidler kan små variasjoner i dose føre til store og potensielt farlige konsekvenser – som alvorlige blødninger.
Sikkerhetsmarginer: MOS, NOAEL og LOAEL
Når man skal vurdere hvor trygt et stoff er – enten det gjelder et legemiddel eller et miljøkjemikalie – er det ikke nok å vite hvilken dose som fungerer, eller hvilken som er giftig.
Det viktigste er hvor langt det er mellom disse to grensene.
Jo større avstand, desto tryggere er bruken. Dette beskrives med Margin of Safety (MOS) – et mer konservativt og realistisk mål enn den klassiske terapeutiske indeksen.
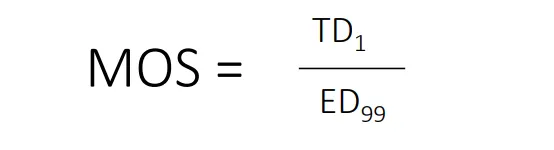
Mens terapeutisk indeks sammenligner gjennomsnittsdoser for effekt og toksisitet, går MOS ett steg videre og ser på ytterpunktene:
ED99, som er dosen som gir terapeutisk effekt hos 99 % av befolkningen
TD1, som er den laveste dosen hvor bare 1 % får toksiske effekter.
Dersom TD1 er mye høyere enn ED99, har stoffet en bred sikkerhetsmargin – og en høy MOS.
Dette gir et tryggere og mer presist bilde av risikoen, særlig for utsatte grupper.
MOS er spesielt nyttig i toksikologisk risikovurdering, der målet er å beskytte ikke bare «gjennomsnittspersonen», men også de mest følsomme individene i befolkningen. Det brukes hyppig ved regulering av både legemidler, kjemikalier og miljøgifter.
For å fastsette grenseverdier i praksis, må man også vite hvor de toksiske effektene faktisk begynner å vise seg.
Her brukes to nøkkelverdier: NOAEL og LOAEL.
NOAEL står for No Observable Adverse Effect Level, og definerer den høyeste dosen som ikke gir noen målbare eller statistisk signifikante skadelige effekter i dyreforsøk. Den fungerer som et nullpunkt – en trygg grense før kroppen begynner å reagere.
LOAEL, Lowest Observed Adverse Effect Level, er den laveste dosen hvor man kan påvise en toksisk effekt. Det er altså det første punktet på dose-respons-kurven hvor skade kan dokumenteres.
Disse to verdiene brukes sammen for å identifisere et sikkert doseområde. De danner utgangspunktet for reguleringsarbeid og anbefalinger, og de justeres med usikkerhetsfaktorer før de brukes på mennesker – for å ta høyde for forskjeller mellom dyrearter og individuell variasjon.
I toksikologi handler alt i bunn og grunn om avstand: avstanden mellom det som virker, og det som skader. MOS, NOAEL og LOAEL hjelper oss med å måle nettopp det – og er uunnværlige verktøy i arbeidet for å gjøre eksponering trygg.
Fra graf til grenseverdi: Hvordan vi beregner trygg eksponering
Når vi vurderer hvor mye av et stoff et menneske trygt kan utsettes for, er det ikke tilstrekkelig å bare vite om det er farlig eller ikke.
Vi må vite ved hvilken dose effekten begynner – og hvor stor sikkerhetsmargin vi trenger før det regnes som trygt.
I toksikologi brukes dose-respons-grafer for å kartlegge dette.
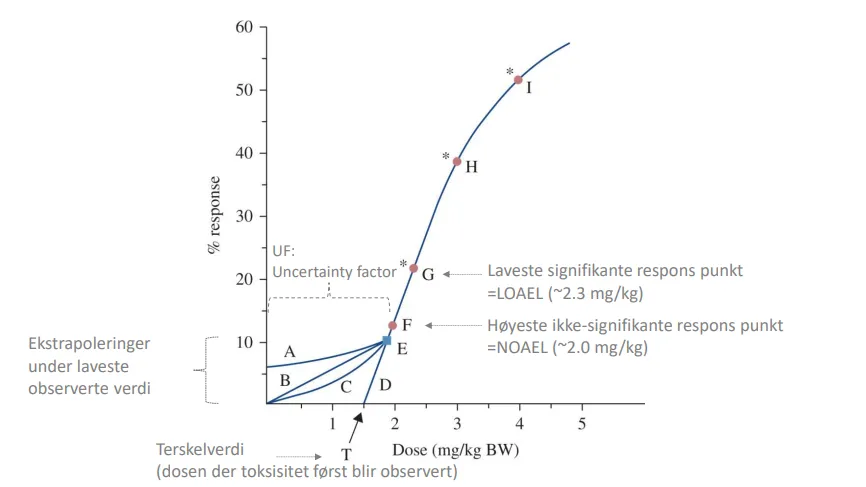
På en typisk graf legges dosen (i mg/kg kroppsvekt) på x-aksen, og andelen av en testet populasjon som får toksisk effekt på y-aksen.
Kurven starter gjerne flatt – det skjer lite ved lave doser – men stiger etter hvert som dosen økes.
Der kurven begynner å løfte seg, finner vi terskelverdien – den laveste dosen hvor en toksisk respons kan observeres.
Rett før dette punktet ligger NOAEL, som markerer den høyeste dosen hvor ingen signifikant effekt ses.
Like etter kommer LOAEL, som angir den laveste dosen hvor en signifikant toksisk effekt oppstår.
Disse to verdiene er avgjørende i all risikovurdering.
Men det stopper ikke der. Dyreforsøk gir viktige data, men mennesker er ikke forsøksdyr – vi er mer komplekse, og vi varierer mye. For å kunne bruke NOAEL eller LOAEL i praktisk regulering, må vi derfor justere disse verdiene med usikkerhetsfaktorer (UF).
En typisk tilnærming er å bruke en 100x sikkerhetsmargin. Først justeres det for artsforskjeller – at mennesker og dyr ikke nødvendigvis reagerer likt – med en 10x faktor.
Deretter kommer en ny 10x faktor for individuell variasjon, for å beskytte sårbare grupper som barn, eldre og personer med nedsatt lever- eller nyrefunksjon.
Til sammen gir dette en UF på 100.
Hvis for eksempel NOAEL er målt til 10 mg/kg/dag, vil man dele dette på 100 og sette den akseptable grensen til 0,1 mg/kg/dag.
Dette danner grunnlaget for et av de viktigste begrepene i risikovurdering: ADI – Akseptabelt Daglig Inntak.
ADI defineres som den mengden av et stoff (per kg kroppsvekt per dag) som et menneske trygt kan innta hver dag gjennom hele livet, uten å risikere helseskade.
ADI brukes i reguleringen av tilsetningsstoffer, miljøgifter og plantevernmidler i mat og drikkevann.
Det hjelper myndighetene med å sette grenseverdier som beskytter folkehelsa – ikke bare for gjennomsnittspersonen, men også for de mest sårbare.
Selv om 100x-sikkerhetsmarginen er standard, kan den justeres opp eller ned basert på ny forskning. Noen stoffer har mer robuste data, og krever mindre forsiktighet. Andre er mer usikre eller virker på spesielle måter – og da kan marginen økes for å være på den sikre siden.
Oversikt over toksisitetstesting
Toksikologiske tester brukes for å vurdere hvor farlige kjemiske stoffer er, og hvordan de påvirker biologiske systemer over ulike tidsperspektiver. Testene kan deles inn etter varighet og alvorlighetsgrad av effekten.
| Testes for (type toksisitet) | Dose | Testperiode | Eksempel | Endepunkt |
|---|---|---|---|---|
| Akutt toksisitet | En dose | 24 timer – 14 dager | LD50-test | Død |
| Sub-akutt toksisitet | Flere doser | < 1 måned | Draize-test (øye- og hudirritasjon) | Irritasjon |
| Sub-kronisk toksisitet | Flere doser | < 10 % av livslengde | NOEL-studier | Organskade |
| Kronisk toksisitet | Flere doser | > 10 % av livslengde | Karsinogen testing | Neoplastiske (kreftrelaterte) endringer |
Legg igjen en kommentar