
Husk å trykke CTRL + f (Command + F) for å finne spesifikke begreper
Ventilasjon – mekanismene bak luftens bevegelse
Ventilasjon er selve motoren i respirasjonssystemet – det som får luft til å strømme inn i og ut av lungene. Uten ventilasjon er det ingen utveksling av gasser, ingen oksygen til cellene og ingen fjerning av karbondioksid. Men ventilasjon er langt mer enn bare pust: det er en presis, rytmisk prosess der trykk, muskelarbeid og volumendringer samspiller for å sikre liv.
Ventilasjon defineres som transporten av luft mellom atmosfæren og alveolene, og prosessen er rytmisk delt i to hovedfaser: inspirasjon og ekspirasjon.
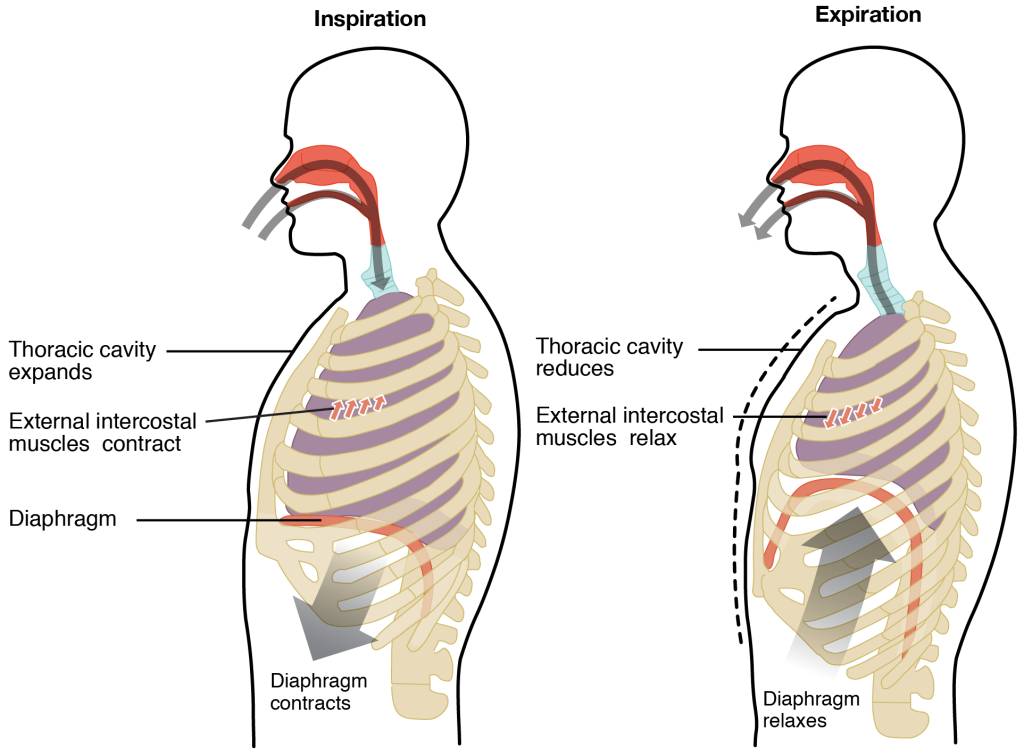
Den ventilatoriske syklus: Inspirasjon og ekspirasjon
Inspirasjon, eller innånding, er i utgangspunktet en aktiv prosess. Den starter med at respirasjonsmusklene – først og fremst diafragma – trekker seg sammen. Når diafragma kontraherer, flater den ut og øker volumet i thoraxhulen i vertikal retning. Samtidig aktiveres de ytre interkostalmusklene, som løfter ribbeina opp og utover, og utvider brystkassen horisontalt.
Denne volumøkningen fører til at trykket i pleurahulen faller til omkring -4 til -8 cmH₂O. Dette negative intrapleurale trykket «drar» lungene med seg ut, og skaper et undertrykk i alveolene som gjør at luft strømmer inn fra atmosfæren. Prosessen er aktiv, og krever energi.
Ekspirasjon, eller utånding, er derimot passiv under hvile. Når inspirasjonsmusklene slapper av, trekker lungene og brystveggen seg automatisk tilbake til utgangsposisjon på grunn av sine elastiske egenskaper.
Denne elastiske rekylkraften presser luften ut av lungene uten at det kreves muskelarbeid.
Ved økt pustebehov – som under fysisk aktivitet eller ved lungesykdom – aktiveres flere muskler for å støtte ekspirasjonen.
Dette kalles forsert ekspirasjon, og inkluderer de indre interkostalmusklene samt magemusklene, som aktivt presser bukhulen oppover og reduserer thoraxvolumet. Hos pasienter med kroniske lungesykdommer, som KOLS, kan selv ekspirasjon i hvile kreve muskelarbeid. Disse pasientene rekrutterer da ofte aksessoriske muskler, som m. sternocleidomastoideus og scalenus, for å hjelpe til med både inn- og utpust.
Grad av ventilasjon – når tempoet endres
Ventilasjonen er ikke alltid konstant. Den kan økes eller reduseres avhengig av kroppens behov og tilstand.
Hyperventilasjon innebærer en økt ventilasjonshastighet eller -dybde, som fører til økt utskillelse av karbondioksid og ofte redusert PaCO₂ i blodet.
Dette kan sees ved angst, smerte eller intens fysisk aktivitet. I noen tilfeller kan det være et uttrykk for underliggende sykdom, som ved metabolsk acidose. Et klassisk eksempel er Kussmaul-respirasjon ved diabetisk ketoacidose – en dyp og rask pusting som kroppen bruker for å kvitte seg med overskudd av H⁺-ioner gjennom CO₂-utskillelse.
Hypoventilasjon innebærer redusert ventilasjon, med påfølgende CO₂-opphopning og ofte lavt oksygentrykk i blodet.
Årsakene kan være mange og sammensatte: kroniske lungesykdommer som KOLS, fedme som hemmer diafragmas bevegelighet. I tillegg kan sykdommer i nervesystemet, som amyotrofisk lateral sklerose (ALS), eller ryggmargsskader påvirke respirasjonsmusklene. Også rus og forgiftninger som demper respirasjonssenteret i hjernen, kan føre til alvorlig hypoventilasjon.
Hva ventileres – alveoler eller dødsrom?
Det er viktig å skille mellom hvor luften går i løpet av et åndedrag. All luft som pustes inn, når ikke nødvendigvis alveolene. En del fyller bare luftveiene – det vi kaller det anatomiske dødsrommet – og deltar ikke i gassutveksling. Resten av luften når alveolene og bidrar til oksygenering av blodet.
Alveolær ventilasjon er derfor den delen av total ventilasjon som faktisk deltar i gassutveksling, og er langt viktigere enn bare minuttventilasjonen – som er summen av all luft som beveger seg inn og ut av lungene per minutt.
Ventilasjonen kan altså være normal i volum, men ineffektiv hvis mye av luften kun fyller dødsrommet – for eksempel ved rask og grunn respirasjon.
Restriktiv og obstruktiv ventilasjonsinnskrenkning
Når ventilasjonen er redusert, snakker vi om ventilasjonsinnskrenkning. Denne kan være enten restriktiv eller obstruktiv.
Ved restriktiv ventilasjonsinnskrenkning er det selve lungens evne til å utvide seg som er begrenset. Det kan skyldes stivhet i lungevevet, som ved lungefibrose, eller ytre forhold som hindrer ekspansjon – for eksempel pleurasykdommer, fedme eller thoraksdeformiteter.
Ved obstruktiv ventilasjonsinnskrenkning er det luftveiene som er trange eller delvis blokkert, noe som øker motstanden mot luftstrøm. KOLS og astma er klassiske eksempler. Her blir særlig ekspirasjonen påvirket, og pasienten bruker mye energi på å presse luften ut – ofte med hjelp av aksessoriske muskler og med forlenget ekspirasjonstid.
Hva som ventileres – dødsrom og alveolær ventilasjon
Ikke all luft som pustes inn, bidrar til gassutveksling. Dette er et viktig poeng i forståelsen av ventilasjonens effektivitet. Når vi puster, fordeler luftvolumet seg mellom områder der gassutveksling skjer – og områder hvor luften bare passerer gjennom, uten å ha noen utvekslingsfunksjon. Å forstå forskjellen mellom dødsromsventilasjon og alveolær ventilasjon er avgjørende både fysiologisk og klinisk.
Dødsromsventilasjon – luften som ikke brukes
Dødsromsventilasjon, ofte betegnet som V_D, refererer til den delen av ventilasjonen som ikke deltar i gassutvekslingen. Dette kan virke som bortkastet luft – og i en viss forstand er det nettopp det. Selv om denne luften ikke gir noe oksygen til blodet og ikke fjerner karbondioksid, krever det fortsatt energi å ventilere den.
Dødsrommet deles i to komponenter:
1. Anatomisk dødsrom
Dette omfatter luftveiene fra nese og munn ned til og med de terminale bronkiolene – altså den ledende transportsonen i luftveiene. Det utgjør omtrent 150 ml hos en voksen person. Denne mengden er relativt konstant uavhengig av pustedybde, men det betyr også at andelen av et lite åndedrag som går til dødsrommet blir stor. Dermed bidrar overfladisk pusting i liten grad til gassutveksling.
2. Alveolært dødsrom
Dette er noe mer subtilt. Det oppstår når alveolene får luft, men det ikke er tilstrekkelig blodtilførsel i tilknyttede kapillærer. Slike alveoler ventileres, men perfunderes ikke – og dermed skjer det ingen gassutveksling. Dette kan skje ved for eksempel lungeemboli, hvor en blodpropp blokkerer lungekapillærer, eller ved hypovolemi, hvor redusert blodvolum gir dårlig perfusjon perifert i lungene.
3. Fysiologisk dødsrom
Dette begrepet beskriver summen av det anatomiske og alveolære dødsrommet, og gir en bedre indikator på hvor stor andel av ventilasjonen som faktisk er ineffektiv. Det fysiologiske dødsrommet er normalt litt større enn det anatomiske, men kan øke betydelig ved sykdommer som KOLS, hjertesvikt og lungeemboli, hvor det forekommer ventilasjons–perfusjons–mismatch.
Alveolær ventilasjon – den effektive pustingen
Mens dødsromsventilasjon representerer luften som ikke
«virker», står alveolær ventilasjon for den delen av ventilasjonen som faktisk når frem til gassutvekslingsområdene og bidrar til oksygenering og CO₂-fjerning. Denne delen av pustingen betegnes V_A, og er essensiell for å opprettholde normal blodgass og syre-base-balanse.
Dersom den alveolære ventilasjonen reduseres – for eksempel ved grunn, overfladisk pust – kan karbondioksid hope seg opp i blodet, noe som gir respiratorisk acidose. Dette skjer raskt, særlig ved underliggende lungesykdom eller respirasjonssvikt.
Et viktig klinisk poeng er at økt respirasjonsfrekvens alene ikke nødvendigvis øker den alveolære ventilasjonen, særlig dersom hvert åndedrag er lite. Dette skyldes at det anatomiske dødsrommet er konstant, og at det da utgjør en større andel av hvert pust. Dermed blir rask, grunn pusting – selv om det ser dramatisk ut – ofte en form for hypoventilasjon i praksis. Mye av luften går til dødsrommet, og lite når alveolene.
Minuttventilasjon – total pustemengde
For å kvantifisere hvor mye luft som ventileres per minutt, bruker vi begrepet minuttventilasjon, som er summen av alle åndedrag per minutt. En person i hvile har vanligvis en minuttventilasjon på mellom 5 og 8 liter per minutt, men dette kan øke dramatisk ved fysisk anstrengelse – hos veltrente personer kan verdier over 100 liter per minutt forekomme.
Men høy minuttventilasjon betyr ikke nødvendigvis høy alveolær ventilasjon. Det er fordelingen av ventilasjonen – ikke bare totalvolumet – som avgjør hvor effektiv gassutvekslingen blir.
Dødsromsventilasjon og måling
For å forstå effektiviteten i ventilasjonen må vi ikke bare kjenne til hvor luften går, men også være i stand til å kvantifisere hvilke deler av ventilasjonen som faktisk deltar i gassutveksling. I klinikk og forskning har man derfor utviklet metoder for å måle dødsromsventilasjon – både den anatomiske og den fysiologiske komponenten.
Måling av anatomisk dødsrom: Fowlers metode
Fowlers metode er en klassisk teknikk for å måle det anatomiske dødsrommet – altså luftvolumet som fyller ledende luftveier, fra nese og munn ned til terminale bronkioler.
Metoden bygger på nitrogenutvasking. Pasienten puster først vanlig luft, som inneholder nitrogen. Deretter puster han inn ren oksygen, og utåndingsluften analyseres kontinuerlig for nitrogeninnhold. Siden oksygenet først fyller de anatomiske luftveiene ved inspirasjon, vil den første delen av ekspirasjonsluften inneholde lite eller ingen nitrogen – den kommer nemlig fra området som aldri var i kontakt med nitrogenholdig luft (dødsrommet). Etter hvert som luften fra alveolene kommer opp, vil nitrogeninnholdet i utpust stige.
Ved å analysere denne stigningen kan man beregne volumet som trengs for å «vaske ut» nitrogen – og dermed beregne størrelsen på det anatomiske dødsrommet.
Måling av fysiologisk dødsrom: Bohrs ligning
Mens Fowlers metode kartlegger anatomisk dødsrom, må Bohrs ligning til for å beregne det fysiologiske dødsrommet – altså summen av anatomisk og alveolært dødsrom. Dette er mer klinisk relevant, siden det også tar høyde for alveoler som er ventilert, men ikke perfundert.
Bohrs ligning sammenligner to trykkverdier for karbondioksid:
- PACO2: CO₂-trykket i alveoleluft. Dette representerer den luften som er i direkte kontakt med blodet i kapillærene, og gjenspeiler kroppens evne til å kvitte seg med CO₂.
- PECO2: CO₂-trykket i den samlede ekspirasjonsluften. Denne luften er en blanding av luft fra alveolene og fra anatomisk dødsrom – og vil derfor ha et lavere CO₂-innhold enn ren alveoleluft.
Fysiologisk dødsrom beregnes med formelen:
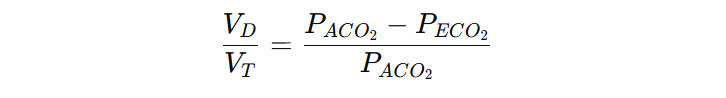
og reflekterer hvor stor andel av hvert pust som ikke deltar i gassutveksling. Jo større denne forskjellen er, desto større er dødsromsandelen – og desto mindre effektiv er ventilasjonen.
Enghoffs modifikasjon – en praktisk tilnærming
I praksis er det vanskelig å måle PACO2 direkte, siden det krever prøvetaking av ren alveoleluft. Enghoff foreslo derfor en modifikasjon av Bohrs ligning, hvor man rett og slett erstatter PACO2 med PaCO2 – altså det arterielle karbondioksidtrykket målt i blodet.
Hos friske personer vil disse to verdiene være nærmest identiske, ettersom det i normal fysiologi er likevekt mellom CO₂ i alveolene og i blodet.
Derfor gir Enghoffs tilnærming et godt estimat på fysiologisk dødsrom med en enkel blodgassmåling.
Men ved sykdomstilstander, som for eksempel KOLS eller lungeemboli, hvor det oppstår ventilasjon–perfusjon-ubalanse (V/Q mismatch), vil forskjellen mellom alveolært og arterielt CO₂-trykk øke. Det betyr at Enghoffs modifikasjon også fanger opp alvorlighetsgraden av slike tilstander, og kan være et verdifullt verktøy i vurdering av pasientens respiratoriske effektivitet.
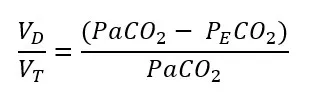
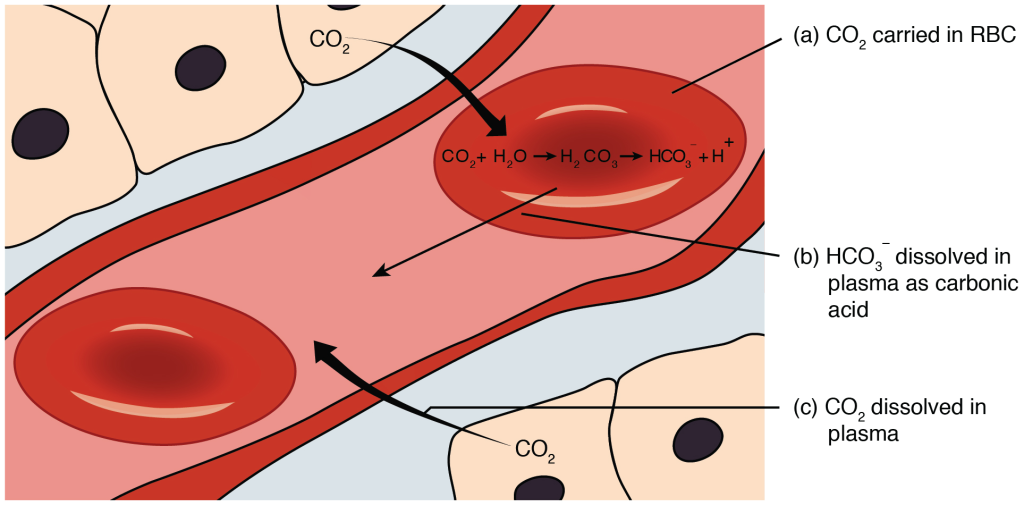
Alveolær ventilasjon og CO₂-utskillelse
Et sentralt fysiologisk prinsipp er at all CO₂ i utåndingsluften kommer fra alveolene. Dette skyldes at CO₂ transporteres fra blodet til alveolluften gjennom diffusjon, og ikke finnes i signifikante mengder i ledende luftveier.
Dermed blir mengden CO₂ som pustes ut, et direkte uttrykk for hvor godt alveolene ventileres. Dersom den alveolære ventilasjonen reduseres, som ved grunn eller langsom pusting, får kroppen problemer med å kvitte seg med CO₂.
Resultatet er hyperkapni, som defineres som forhøyet karbondioksidtrykk i arterielt blod (PaCO₂). Denne opphopningen av CO₂ fører til respiratorisk acidose, fordi CO₂ i blodet reagerer med vann og danner karbonsyre.
Sammenhengen mellom alveolær ventilasjon og CO₂-trykk kan beskrives matematisk i den alveolære ventilasjonsligningen, som viser at PaCO₂ er omvendt proporsjonal med den alveolære ventilasjonen – forutsatt at CO₂-produksjonen i kroppen er konstant.
Dette innebærer at dersom ventilasjonen til alveolene halveres, vil PaCO₂ i prinsippet dobles.
Økt metabolisme krever økt ventilasjon
Under fysisk aktivitet øker kroppens stoffskifte, og dermed produseres mer CO₂. For å opprettholde normale blodgassverdier må ventilasjonen øke proporsjonalt. Dette skjer først og fremst ved at den alveolære ventilasjonen øker, slik at CO₂ skilles ut i samme takt som det dannes.
Dersom kroppen ikke klarer å øke ventilasjonen nok til å møte dette behovet – for eksempel ved lungesykdom – kan CO₂ hope seg opp og pH falle. Samtidig vil anaerob metabolisme kunne bidra med produksjon av melkesyre, noe som forverrer acidosebildet.
Ved hyperventilasjon, derimot, overstiger ventilasjonen kroppens behov. Dette fører til en reduksjon i PaCO₂ – kjent som hypokapni – og kan forårsake respiratorisk alkalose, som ofte oppstår ved angst, smerte eller frivillig overpusting.
Minuttventilasjon og fysiologisk regulering
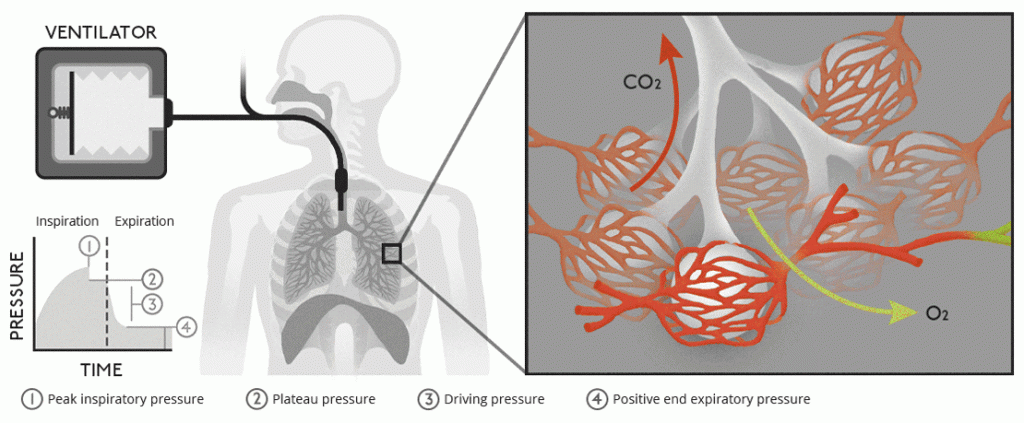
Den totale luftmengden som beveger seg inn og ut av lungene per minutt kalles minuttventilasjon (V̇_E). Den beregnes som tidalvolum multiplisert med respirasjonsfrekvens.
Kroppen kan øke minuttventilasjonen på to måter:
- Ved å øke tidalvolumet (V_T) – dette gir større luftmengde per pust. Det er en mer effektiv måte å øke ventilasjonen på, fordi en større andel av hver innånding når alveolene og deltar i gassutveksling.
- Ved å øke respirasjonsfrekvensen (RF) – flere pust per minutt. Dette er en rask tilpasning, men mindre energieffektiv. Ved høye frekvenser øker nemlig andelen av luften som går til dødsromsventilasjon, og dermed reduseres ventilasjonens effektivitet.
Ideelt sett vil kroppen i starten av økt behov – som ved fysisk aktivitet – primært øke tidalvolumet, og først deretter øke frekvensen dersom behovet vedvarer.
Fysisk aktivitet og ventilatorisk respons
Ved fysisk aktivitet skjer det en betydelig økning i metabolsk aktivitet. Muskelarbeidet fører til økt produksjon av CO₂, og ved intens anstrengelse også melkesyre, som begge senker blodets pH.
For å opprettholde syre-base-balanse, øker ventilasjonen. Den alveolære ventilasjonen stiger for å kvitte seg med det økte CO₂-nivået, og samtidig for å bedre oksygenering.
Ved lett til moderat aktivitet øker først og fremst tidalvolumet. Ved intens fysisk belastning øker også respirasjonsfrekvensen markant. Denne kombinasjonen sikrer at mest mulig luft når alveolene og deltar i gassutveksling, slik at CO₂ fjernes og pH holdes stabil, til tross for det økte metabolske trykket.
Mekaniske faktorer og lungevolum
Lungens evne til å fylle seg med luft og kvitte seg med den igjen er avhengig av både statisk kapasitet og dynamisk luftstrøm. Disse to aspektene – hvor mye luft lungene kan inneholde, og hvor raskt luft kan bevege seg – bestemmer ventilasjonens effektivitet og kroppens evne til å møte oksygenbehovet.
Statisk og dynamisk begrensning av ventilasjon
Ventilasjonen kan begrenses av statiske eller dynamiske mekaniske faktorer.
De statiske faktorene handler om hvor mye lungene kan utvide seg – og er bestemt av elastisiteten i lungevevet, brystkassens bevegelighet og diafragmaets funksjon. Om lungene er stive, brystkassen begrenset i bevegelse, eller diafragma er svekket, reduseres volumet som lungene kan fylles med.
Man kan sammenligne dette med en stiv ballong – uansett hvor mye man prøver å blåse, lar den seg ikke fylle helt.
De dynamiske faktorene handler om hvor lett luften kan strømme gjennom luftveiene. Her spiller luftveienes diameter, lengde og luftstrømmens karakter (laminær eller turbulent) en avgjørende rolle.
Ved sykdommer som astma eller KOLS snevres luftveiene inn, og særlig under ekspirasjon kan luftveiene klappe sammen. Det er som å forsøke å blåse ut gjennom et trangt sugerør – jo mindre tverrsnitt, desto høyere motstand og lavere flyt.
Lungevolumer og ventilasjonskapasiteter
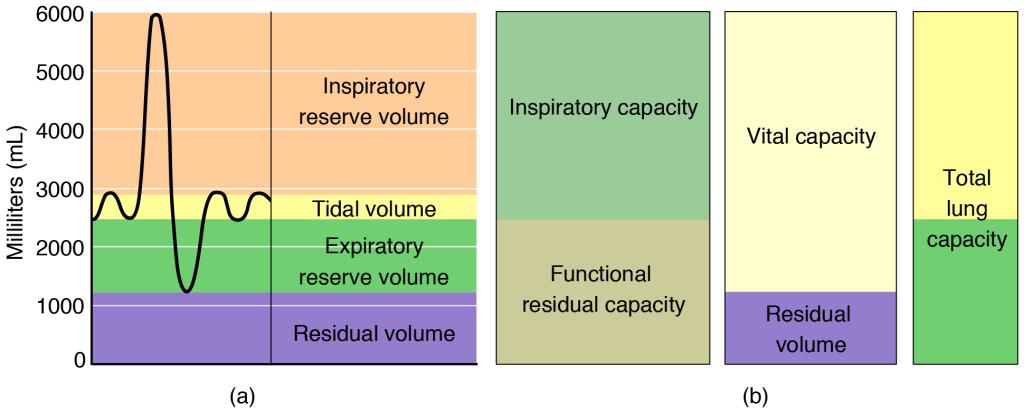
Lungens volum kan beskrives gjennom en rekke definerte parametere. Disse måler enten statiske volumer (mengder luft ved ulike faser i pustesyklusen), eller kombinasjoner av volumer (kapasiteter). Kunnskap om disse gjør det mulig å forstå normal og patologisk respirasjon.
Total lungekapasitet (TLC)
TLC er den maksimale luftmengden lungene kan inneholde etter en full inspirasjon. Normalt ligger dette rundt 5–6 liter hos voksne. TLC reduseres ved restriktive tilstander, hvor lungevevet ikke kan utvide seg normalt, og øker ofte ved obstruktive sykdommer som KOLS på grunn av hyperinflasjon.
Vitalkapasitet (VC)
Vitalkapasitet er det totale luftvolumet en person kan puste inn og ut mellom maksimal inspirasjon og maksimal ekspirasjon. Det tilsvarer TLC minus residualvolumet (RV). VC reduseres både ved restriktive og obstruktive lungesykdommer – enten fordi lungene ikke kan utvide seg nok, eller fordi de ikke tømmes effektivt.
Funksjonell residualkapasitet (FRC)
FRC er mengden luft som gjenstår i lungene etter en normal, passiv ekspirasjon. Det representerer likevektspunktet mellom lungens og brystkassens elastiske krefter. FRC ligger normalt på 2,5–3 liter, men øker ved obstruktive sykdommer som følge av luftfelle og redusert elastisk tilbakeslag i lungevevet.
Residualvolum (RV)
Residualvolum er den mengden luft som blir igjen i lungene etter maksimal utpust. Det er denne luften som forhindrer alveolene fra å kollapse fullstendig. Normalt ligger RV på 1–1,5 liter. Ved KOLS kan RV øke betydelig på grunn av luftfelle. Ved enkelte restriktive tilstander kan RV være redusert, men det er sjeldnere.
Inspiratorisk reservevolum (IRV)
IRV er den ekstra luftmengden man kan trekke inn etter en vanlig innpust. Det er kroppens ventilasjonsreserve under for eksempel trening eller stress. IRV ligger på rundt 3 liter. Ved hyperinflasjon, som presser diafragma nedover, reduseres IRV fordi det ikke er rom for ytterligere ekspansjon.
Ekspiratorisk reservevolum (ERV)
ERV er den ekstra luftmengden som kan pustes ut etter en normal ekspirasjon. ERV er typisk 1–1,5 liter. Ved obstruktive sykdommer reduseres ERV tidlig, da luftveiskollaps under utpust hindrer full tømming av lungene. ERV reduseres også ved fedme og andre restriktive forhold hvor diafragma og brystkasse er mekanisk begrenset.
Tidalvolum (TV)
Tidalvolum er den luftmengden som pustes inn og ut ved hver normal respirasjon, og utgjør omtrent 500 ml i hvile. Ved fysisk aktivitet kan tidalvolumet økes betydelig, opptil 50–60 % av vitalkapasiteten. Ved behov for mekanisk ventilasjon tilpasses tidalvolumet nøye for å unngå ventilasjonsindusert lungeskade.
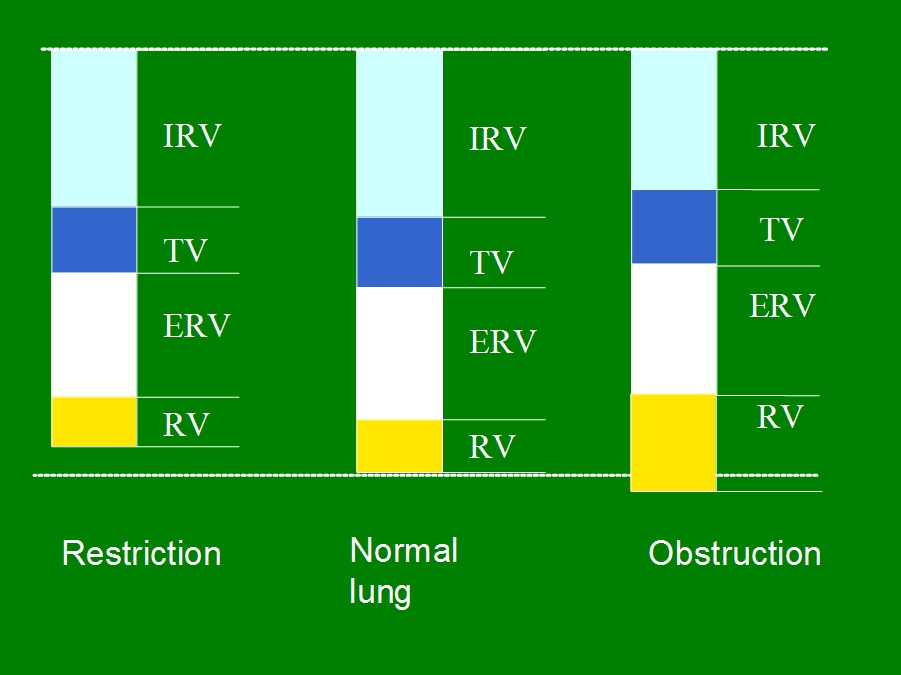
Endringer ved økt ventilasjonsbehov
Når kroppen krever økt ventilasjon – som ved fysisk aktivitet, sykdom eller stress – vil tidalvolumet øke. Dette skjer på bekostning av IRV og ERV, som begge reduseres når man puster dypere og mer aktivt. Ved maksimal ventilasjon tømmes og fylles lungene nesten helt, og reservevolumene krymper til et minimum
God respirasjon forutsetter at lungene har tilstrekkelig volumkapasitet og lav motstand. To egenskaper er spesielt viktige:
Lavt residualvolum (RV) gir mer aktivt tilgjengelig volum.
Ved obstruktiv sykdom øker RV, og en større andel av lungens kapasitet fylles av luft som ikke kan brukes. Dette reduserer effektiviteten og gir ofte tungpust, spesielt ved anstrengelse.
Høy total lungekapasitet (TLC) gir større kapasitet til å øke ventilasjonen ved behov. Idrettsutøvere har ofte høyere TLC enn gjennomsnittet, noe som gir økt ytelse og ventilasjonsmargin.
Innskrenket ventilasjon – når lungene hindres i å gjøre jobben
Ventilasjonen i lungene kan reduseres på ulike måter. I medisinsk sammenheng skiller man mellom to hovedtyper av innskrenkning: restriktiv og obstruktiv. Begge fører til redusert evne til å ventilere lungene effektivt, men mekanismene, årsakene og konsekvensene er ulike.
Den restriktive typen handler om volum – lungene klarer ikke å utvide seg som de skal. Den obstruktive typen handler om hastighet – luft kommer seg ikke raskt nok ut.
Restriktiv ventilasjonsinnskrenkning – når lungen ikke kan utvide seg
Ved restriktiv lungesykdom er det ofte inspirasjonen som er hovedproblemet. Lungene klarer ikke å ekspandere som normalt, og resultatet er redusert lungevolum.
Dette kan sammenlignes med en stiv ballong: selv om man prøver å blåse den opp, lar den seg ikke fylle ordentlig.
Den vanligste konsekvensen av dette er en reduksjon i tidalvolum og total lungekapasitet (TLC). Pasienter med restriktive tilstander opplever ofte tung pust, særlig ved fysisk aktivitet, fordi de ikke klarer å øke ventilasjonen i takt med kroppens behov.
Årsaker til restriksjon
Restriksjon kan skyldes både pulmonale og ekstrapulmonale faktorer.
Pulmonale årsaker inkluderer sykdommer som påvirker selve lungevevet. Interstitiell lungesykdom (ILD) og lungefibrose gir arrdannelse og fortykning av lungevevet, noe som reduserer elastisiteten. Lungeødem – væskeansamling i alveolene og interstitiet – gjør vevet tyngre og mindre medgjørlig.
Ekstrapulmonale årsaker påvirker lungens evne til å utvide seg via ytre forhold. Kyfoskoliose deformerer brystkassen og begrenser bevegelse. Nevromuskulære sykdommer, som ALS, rammer respirasjonsmusklene, og overvekt kan fysisk hindre thorax i å ekspandere. Graviditet påvirker også ventilasjonen ved å presse diafragma oppover.
Obstruktiv ventilasjonsinnskrenkning – når luften ikke slipper ut
Ved obstruktiv lungesykdom er problemet først og fremst knyttet til ekspirasjonen. Luften kommer inn i lungene, men møter motstand på vei ut. Det kan sammenlignes med å puste ut gjennom et smalt sugerør – luften kommer ut, men sakte og med økt anstrengelse.
Denne motstanden fører til at ikke all luft tømmes ut mellom hvert åndedrag. Residualvolumet (RV) øker, og pasienten utvikler luftfelle (air trapping). Over tid kan dette føre til hyperinflasjon, der lungene blir kronisk overfylt med luft.
Årsaker til obstruksjon
De vanligste obstruktive sykdommene er KOLS, astma, kronisk bronkitt og emfysem. Ved astma skyldes obstruksjonen sammentrekning av glatte muskler (bronkospasme), ødem og økt slimproduksjon – og tilstanden er som regel reversibel med behandling.
KOLS derimot, gir ofte irreversibel obstruksjon. I KOLS ser man både kronisk bronkitt, som gir økt slim og inflammasjon, og emfysem, der lungevevet brytes ned og mister sin elastisitet. De små luftveiene kollapser lett under ekspirasjon, noe som forsterker luftfellen og forverrer symptomene.
Dynamiske lungevolum og flow
Lungefunksjonen handler ikke bare om hvor mye luft lungene kan inneholde, men også om hvor raskt luften beveger seg. Denne luftstrømshastigheten – ofte omtalt som flow – er avgjørende for å vurdere om luftveiene er åpne og effektive. Måling av flow ved hjelp av spirometri er en av de viktigste og mest brukte undersøkelsene i klinisk lungemedisin.
Spirometri – måling av luftstrøm og volum
Spirometri er en enkel, ikke-invasiv test som måler mengden og hastigheten av luft som pustes inn og ut. Den egner seg svært godt til å påvise både obstruktive og restriktive forandringer i lungefunksjon, og brukes både diagnostisk og i oppfølging av sykdom.
Det er viktig å merke seg at spirometri ikke kan måle alt. Den registrerer kun luft som beveger seg inn og ut av lungene. Volumer som residualvolum (RV) og funksjonell residualkapasitet (FRC) kan ikke måles direkte med spirometri, men krever spesialundersøkelser som helkroppspletysmografi (Bodybox).
Forsert ekspirasjon – når lungene tømmes med kraft
En spirometritest starter med at pasienten puster maksimalt inn til total lungekapasitet (TLC), og deretter blåser så kraftig og raskt som mulig ut – helt ned til residualvolum (RV). Denne manøveren – kjent som forsert ekspirasjon – gir et mål på luftveismotstand, lungeelastisitet og muskelkraft.
Tre nøkkelparametere brukes i tolkning:
- FEV₁ (Forsert ekspiratorisk volum i første sekund) er volumet som pustes ut i løpet av det første sekundet etter starten av forsert ekspirasjon. FEV₁ er særlig følsom for luftveisobstruksjon, og reduseres tidlig ved sykdommer som KOLS og astma. Hos friske ligger FEV₁ typisk rundt 80 % av FVC.
- FVC (Forsert vitalkapasitet) er totalvolumet av luft som kan pustes ut etter maksimal inspirasjon. FVC kan være redusert både ved restriktive og obstruktive sykdommer, men årsakene er ulike. Ved restriksjon skyldes det redusert lungevolum. Ved obstruksjon skyldes det ofte luftfelle, som gjør at pasienten ikke klarer å tømme lungene fullstendig.
- FEV₁/FVC-ratio er forholdet mellom de to over, og er avgjørende for å skille mellom obstruktiv og restriktiv sykdom. En ratio < 0,7 (eller under nedre normalgrense) tyder på obstruktiv lungesykdom. Ved restriksjon reduseres begge verdiene proporsjonalt, slik at ratioen ofte er normal eller forhøyet.
Obstruksjon – spirometrisk definisjon og alvorlighetsgrad
Obstruksjon kjennetegnes av en redusert FEV₁/FVC-ratio. Dette innebærer at en uforholdsmessig stor andel av luftvolumet ikke kan pustes ut raskt, noe som reflekterer økt motstand i luftveiene, særlig under ekspirasjon.
Ved KOLS brukes klassifikasjonssystemet fra GOLD (Global Initiative for Chronic Obstructive Lung Disease), der alvorlighetsgraden bestemmes av hvor mye FEV₁ er redusert i forhold til forventet verdi:
- Mild: FEV₁ ≥ 80 %
- Moderat: 50 % ≤ FEV₁ < 80 %
- Alvorlig: 30 % ≤ FEV₁ < 50 %
- Svært alvorlig: FEV₁ < 30 %
Nyere retningslinjer anbefaler bruk av Lower Limit of Normal (LLN) i stedet for en fast grense på 0,7, siden denne tar hensyn til alder og kjønn og gir færre falske diagnoser hos eldre.
Tolkning av spirometrikurver
Resultatene fra spirometri presenteres ofte i to typer grafer:
1. Volum-tid-kurve
Denne kurven viser hvor mye luft som er pustet ut over tid. Hos friske personer ses en rask stigning og raskt platå, som reflekterer effektiv lungeuttømming. Ved obstruktiv sykdom ses en flatere kurve – det tar lengre tid å nå platå. Ved restriktiv sykdom ses en rask stigning til et lavere platå, fordi lungevolumene er redusert.
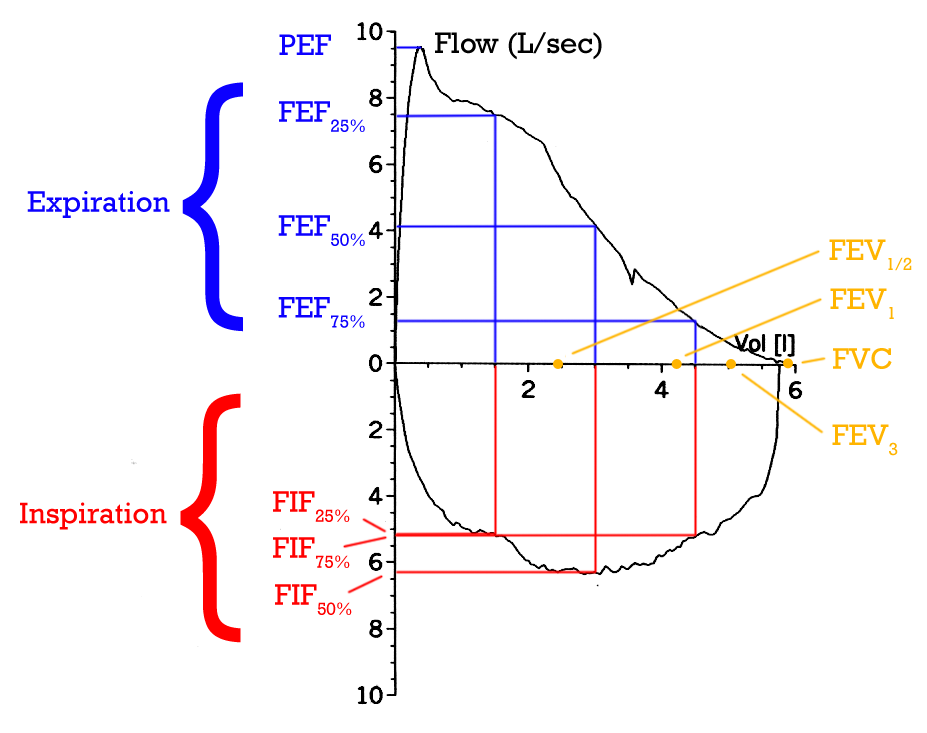
2. Flow-volum-kurve
Denne kurven viser flow (luftstrømshastighet) mot volum. Den starter med et kraftig toppunkt (Peak Expiratory Flow), etterfulgt av en jevn nedadgående kurve.
- Ved obstruktiv sykdom vil denne kurven ha en karakteristisk «hengekøye-form», med tidlig fall i luftstrømmen og redusert flow gjennom hele ekspirasjonen.
- Ved restriktiv sykdom er kurvens form normalt bevart, men den er smal og lavere, som følge av redusert volumkapasitet.
Kurveanalysen gir derfor verdifull innsikt i hvor i luftveiene problemet sitter, og hvilken type lungesykdom som foreligger.
 Anki-kort
Anki-kort
Obs, tomt! Kommer etterhvert <3
 Eksamensoppgaver
Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
 Klinisk case
Klinisk case
Obs, tomt! Kommer etterhvert <3
 Test deg selv
Test deg selv