
Kroppens sirkulasjonssystem er ikke statisk – det er dynamisk, fleksibelt og hele tiden i endring. Når du reiser deg opp fra sengen, begynner å løpe, eller spiser et måltid, må blodtrykket og blodstrømmen justeres raskt og presist for at kroppen skal fungere optimalt. Dette skjer gjennom en kompleks samhandling mellom nervesystemet, hormoner og lokale signaler – og denne prosessen kalles sirkulasjonsregulering.
Formålet med reguleringen er å sikre at hvert organ får tilstrekkelig blodtilførsel til enhver tid – enten du sitter stille eller er i fysisk aktivitet. Hjernen må alltid ha oksygen, nyrene må kunne filtrere blod, og musklene trenger mer blod når de jobber. Samtidig må blodtrykket holdes innenfor et visst område for at sirkulasjonen skal være effektiv og trygg.
For å oppnå dette, bruker kroppen flere reguleringsmekanismer som samarbeider:
- Nervøs regulering, først og fremst via det autonome nervesystemet, justerer raskt hjertefrekvens, kontraktilitet og blodkarenes diameter.
- Refleksmekanismer, som barorefleksen, oppdager endringer i blodtrykket og responderer i løpet av sekunder.
- Hormonelle systemer, som RAAS (renin-angiotensin-aldosteron-systemet), justerer blodvolum og karresistens over tid.
- Lokal autoregulering, der organene selv tilpasser blodstrømmen ut fra sitt behov.
I denne gjennomgangen skal vi utforske hvordan disse systemene fungerer, hvordan de virker sammen – og hva som skjer når reguleringen svikter. Vi starter med nervesystemets rolle, før vi går videre til refleksene, de hormonelle signalene og den lokale kontrollen i vevet.
Men før vi går videre, noter deg dette:
Forskjell på arterielt blodtrykk og total perifer motstand:
Arterielt blodtrykk (BT) er trykket blodet utøver mot arterieveggene.
Det bestemmes hovedsakelig av to faktorer: hvor mye blod hjertet pumper ut (hjerteminuttvolum) og motstanden blodet møter i blodårene.
Total perifer motstand (TPR) er summen av motstanden blodet møter i kroppens arteriole-nettverk.
Det handler om hvor trange eller vide de små blodårene er – og påvirkes særlig av diameteren på arteriolene.
🧠 Formelen som kobler dem sammen:
Blodtrykk = Hjerteminuttvolum × Total perifer motstand
Så:
- BT er resultatet/konsekvensen
- TPR er én av faktorene som bestemmer det
Det autonome nervesystemets rolle i sirkulasjonsregulering
For at blodtrykket og blodstrømmen skal kunne tilpasses ulike situasjoner – som når vi reiser oss opp, trener, hviler eller mister blod – trenger kroppen et system som reagerer raskt og presist. Dette systemet er det autonome nervesystemet (ANS), og det fungerer som en slags «automatisk justeringssentral» for sirkulasjonen. Det autonome nervesystemet regulerer både hjertets aktivitet og blodårenes tonus – altså hvor trange eller vide blodårene er – og er dermed helt avgjørende for å opprettholde stabilt blodtrykk og tilstrekkelig blodforsyning til alle organer.
Sympatikus – den dominerende aktøren
Når det kommer til regulering av blodårer og total perifer motstand, er det den sympatiske grenen av ANS som er sjefen. De fleste blodårer – spesielt arterier og vener i hud, splanchnicusorganer og beinmuskulatur – har tett sympatisk innervasjon. Her frisettes noradrenalin fra postganglionære sympatiske fibre, og dette binder seg hovedsakelig til α₁-adrenerge reseptorer i karveggen.
Resultatet er kontraksjon av glatt muskulatur og dermed vasokonstriksjon – en innsnevring av blodåren.
Når blodårene trekker seg sammen, øker den totale perifere motstanden (TPR), og det fører til at blodtrykket stiger. Dette er særlig viktig i situasjoner hvor blodtrykket trues – som når vi reiser oss opp fra liggende stilling, eller mister blod.
Sympatikus påvirker også venene og øker det venøse tilbakeføringen til hjertet ved å redusere venenes kapasitet – det gjør at mer blod kommer tilbake til hjertet, og dermed opprettholdes slagvolum og minuttvolum.
I tillegg til α₁-reseptorer finnes β₂-reseptorer i enkelte kar – særlig i skjelettmuskulatur – og når disse stimuleres (spesielt av adrenalin i lavere konsentrasjoner), gir det vasodilatasjon. Dette er viktig under fysisk aktivitet, slik at arbeidende muskler får tilstrekkelig blodtilførsel.
Parasympatikus
Parasympatikus har svært begrenset innvirkning på blodårer.
De fleste kar har ikke parasympatisk innervering.
Et unntak er enkelte kar i genitalia og spyttkjertler, hvor parasympatisk stimulering kan føre til vasodilatasjon via produksjon av nitrogenoksid (NO). Men i det store bildet er det sympatikus som regulerer kar og trykk.
Kort oppsummert:
- Sympatikus:
- α₁-reseptorer → vasokonstriksjon (↑TPR, ↑BT)
- β₂-reseptorer (adrenalin) → vasodilatasjon (f.eks. i muskler under aktivitet)
- Kontraksjon av vener → økt venøs retur → ↑ preload og slagvolum
- Parasympatikus:
- Minimal rolle i karregulering
Korttidsregulering av sirkulasjon
Når du reiser deg opp, fører tyngdekraften til at blodet samler seg i beina og bekkenet. Dette reduserer det venøse tilbakeløpet til hjertet, og dermed synker slagvolumet og blodtrykket i noen sekunder. Uten korreksjon kunne dette ført til svimmelhet eller besvimelse – og her trår det autonome nervesystemet til.
Baroreseptorene i aortabuen og sinus caroticus merker trykkfallet og sender signaler til hjernen via n. glossopharyngeus og n. vagus. Hjernen tolker det som et «alarmtegn» og aktiverer sympatikus mens parasympatikus hemmes:
- Hjertet slår raskere (↑ kronotropi)
- Hjertet slår kraftigere (↑ inotropi)
- Blodårer trekker seg sammen (↑ TPR)
- Vener kontraherer (↑ venøs retur)
Resultatet er at blodtrykket normaliseres – ofte i løpet av få sekunder.
Denne refleksen kalles barorefleksen, og den er avgjørende for øyeblikkelig regulering av blodtrykk.
Barorefleksen
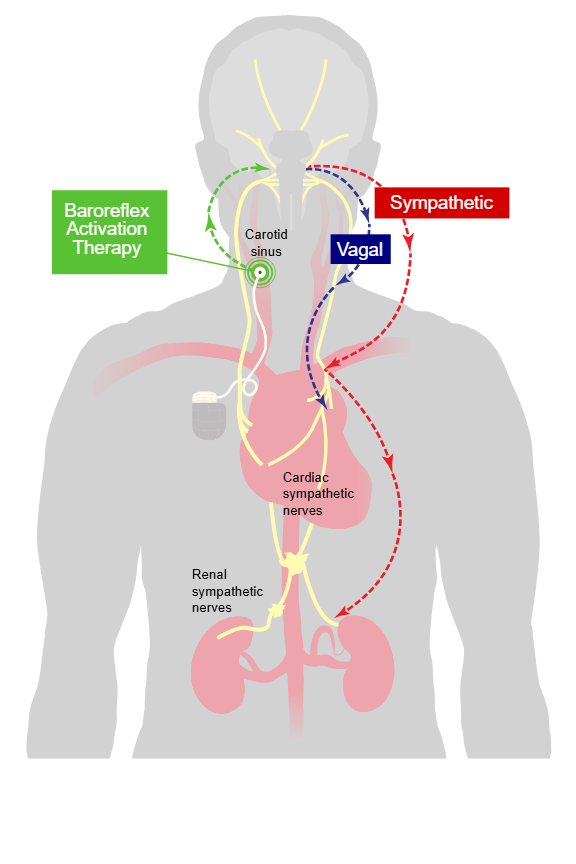
Tenk deg at du reiser deg brått opp fra sengen en morgen. Tyngdekraften trekker blodet nedover i kroppen, og plutselig blir det litt mindre blod tilgjengelig i brystkassen og hjernen. Dette kunne fort ført til svimmelhet eller besvimelse – hvis det ikke var for barorefleksen. Denne refleksen er kroppens egen nødbrems og gasspedal i ett, og den reagerer lynraskt på selv små endringer i blodtrykk for å sikre at blodet fortsetter å strømme dit det skal, også når kroppen brått skifter stilling eller havner i akutt ubalanse.
Langs veggene i visse store arterier sitter det spesialiserte sanseceller kalt baroreseptorer. De viktigste finner vi i sinus caroticus, der a. carotis deler seg, og i aortabuen. Disse reseptorene registrerer hvor mye karveggen strekkes – som et indirekte mål på blodtrykket. Når trykket øker, strekker karveggen seg mer. Når trykket synker, blir det mindre strekk. Dette tolkes av kroppen som endringer i blodtrykk, og svarene kommer raskt.
Informasjonen sendes videre til hjernen via to viktige hjernenerver: n. glossopharyngeus (CN IX) og n. vagus (CN X). Signalene ender i et kontrollsenter i den forlengede marg – nucleus tractus solitarius (NTS) – som fungerer som et slags trafikkpoliti for det autonome nervesystemet. Her bestemmes det om kroppen skal gire opp eller bremse ned.
Hva skjer når blodtrykket stiger?
Når trykket blir for høyt, gir baroreseptorene tydelig beskjed om at karveggen strekkes mer enn vanlig.
Dette fører til økt parasympatisk stimulering via vagusnerven og samtidig en demping av sympatisk aktivitet.
Hjertet responderer med å slå saktere og svakere, og blodårene får signal om å slappe av. Tilsammen gir dette lavere hjertefrekvens, mindre kontraktilitet og lavere perifer motstand – og trykket faller tilbake til normalen.
Hva skjer når blodtrykket faller?
Omvendt, når trykket synker, for eksempel når vi reiser oss, sender baroreseptorene færre signaler. Dette tolkes som behov for tiltak. Kroppen svarer med å bremse parasympatikus og skru opp sympatikus. Hjertet slår raskere og kraftigere, blodårene trekker seg sammen, og venene klemmer blodet tilbake mot hjertet. Dermed økes både minuttvolum og total perifer motstand, og blodtrykket stiger igjen – ofte på bare noen sekunder.
Hvor raskt virker barorefleksen?
Barorefleksen er en korttidsregulerende mekanisme.
Den fungerer på sekunder, og er helt essensiell i hverdagssituasjoner som stillingsendring, fysisk aktivitet og akutte smerte- eller stressreaksjoner. Men det er også en viktig begrensning her: baroreseptorene venner seg raskt til et nytt trykknivå. Hos personer med langvarig høyt blodtrykk vil baroreseptorene gradvis akseptere dette som «normaltilstand», og slutter dermed å aktivere responsen som skal senke trykket.
Når barorefleksen ikke fungerer som den skal, blir blodtrykket sårbart. Dette kan ses ved ortostatisk hypotensjon, der blodtrykket faller dramatisk ved oppreising. Det kan også ramme pasienter med autonom nevropati, som ved diabetes eller Parkinsons sykdom. I tillegg kan enkelte medisiner, som β-blokkere, gjøre barorefleksen mindre effektiv, fordi de hindrer hjertets evne til å øke frekvens og kontraktilitet.
Langtidsregulering av blodtrykk og sirkulasjon
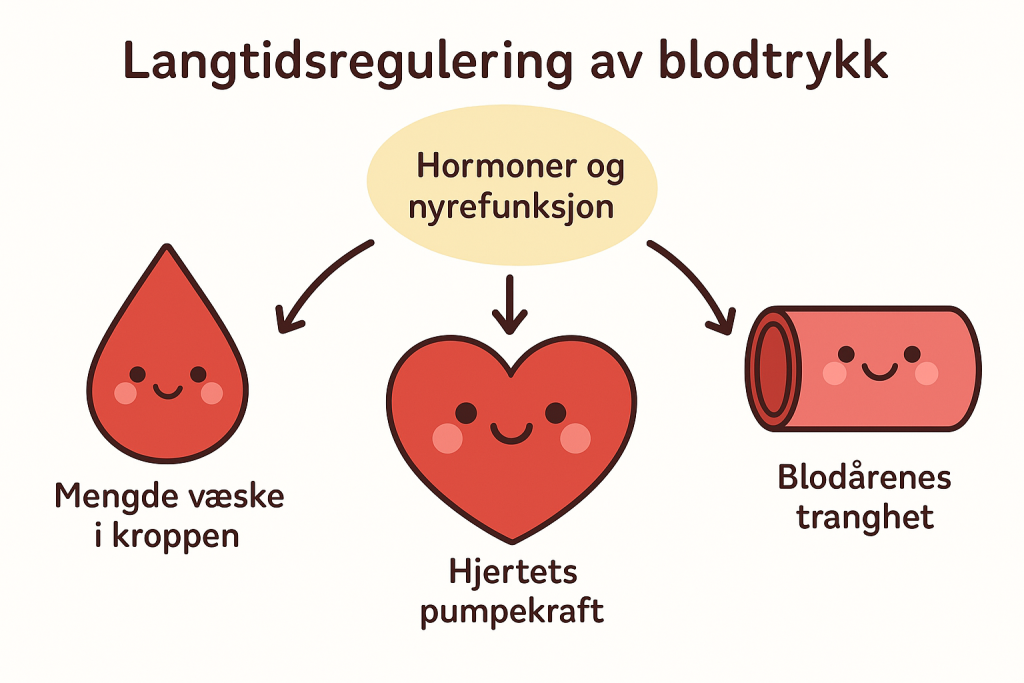
Blodtrykket i kroppen må holdes stabilt over tid for at vev skal få tilstrekkelig oksygen og næringsstoffer. Selv små, kroniske avvik i trykket kan føre til alvorlige konsekvenser for hjertet, hjernen og nyrene. Til dette kreves mer enn raske reflekser – kroppen trenger et system som kan justere sirkulasjonen over timer, dager og uker. Det er her de hormonelle og nyregitte mekanismene i langtidsreguleringen kommer inn.
Der barorefleksen fungerer som kroppens akutte “brannslukker” når trykket endrer seg raskt, er langtidsreguleringen mer som en termostat: Den finjusterer og holder blodtrykket stabilt over tid ved å regulere væskevolumet i kroppen.
Hvorfor trenger vi langtidsregulering?
Et stabilt blodtrykk er avgjørende for å sikre tilstrekkelig perfusjon til organene, spesielt hjerne og hjerte. Dersom blodvolumet synker (for eksempel ved blødning eller dehydrering), eller dersom trykket faller av andre årsaker, må kroppen ha mekanismer som kan justere:
- hvor mye væske som beholdes i kroppen
- hvor sterkt hjertet pumper
- hvor trangt blodårene er
Disse justeringene skjer ikke bare via nerver, men gjennom hormoner og nyrefunksjon.
Nyrene – langsiktig volumkontroll
Langtidsreguleringen av blodtrykk er i stor grad avhengig av nyrene.
Ved å bestemme hvor mye natrium og vann som skal skilles ut, regulerer nyrene det totale blodvolumet. Dette er direkte knyttet til trykket i karene – mer væske betyr høyere trykk, mindre væske betyr lavere trykk. Dersom blodvolumet faller, som ved dehydrering eller blødning, vil nyrene holde tilbake mer væske. Og motsatt: ved for høyt trykk øker væsketapet.
RAAS – kroppens hormonelle respons på lavt trykk
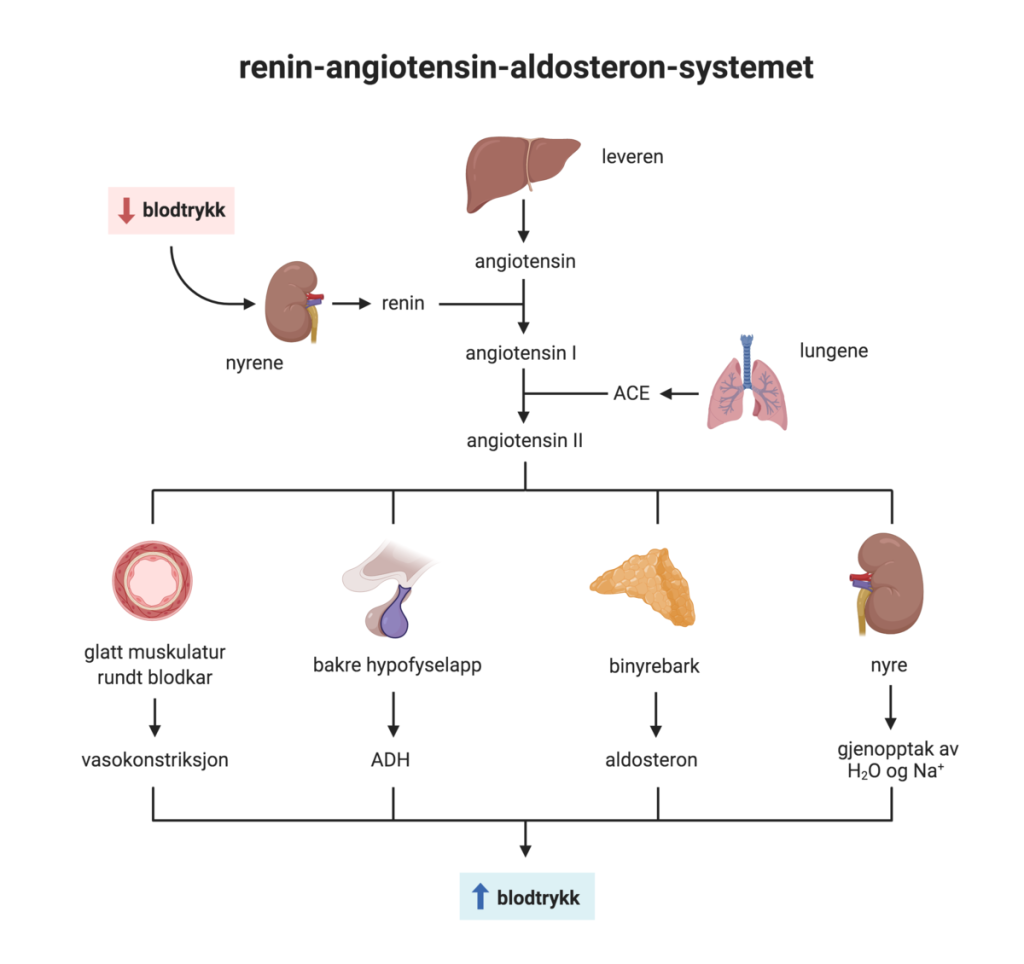
Et av kroppens viktigste systemer for langtidsregulering er renin-angiotensin-aldosteron-systemet, ofte forkortet til RAAS.
Dette aktiveres når kroppen registrerer at blodtrykket, sirkulasjonen eller natriumkonsentrasjonen er for lav.
Prosessen starter i nyrene. Spesialiserte celler i den juxtaglomerulære apparatet slipper ut enzymet renin. Renin omdanner et inaktivt protein fra leveren – angiotensinogen – til angiotensin I. Når dette passerer lungene, omdannes det videre til angiotensin II via enzymet ACE (angiotensin-converting enzyme).
Angiotensin II har flere kraftige effekter:
– Det trekker sammen blodårene, noe som øker det perifere motstanden og dermed blodtrykket.
– Det stimulerer tørst, slik at man drikker mer.
– Det fremmer utskillelsen av aldosteron fra binyrebarken, som øker natrium- og vannreabsorpsjon i nyrene.
– Det øker utskillelsen av ADH fra hypofysen, som også holder tilbake vann.
Summen av dette er at trykket øker – ikke bare ved at karene strammer seg, men også ved at blodvolumet stiger.
ADH – kroppens vannbevarer
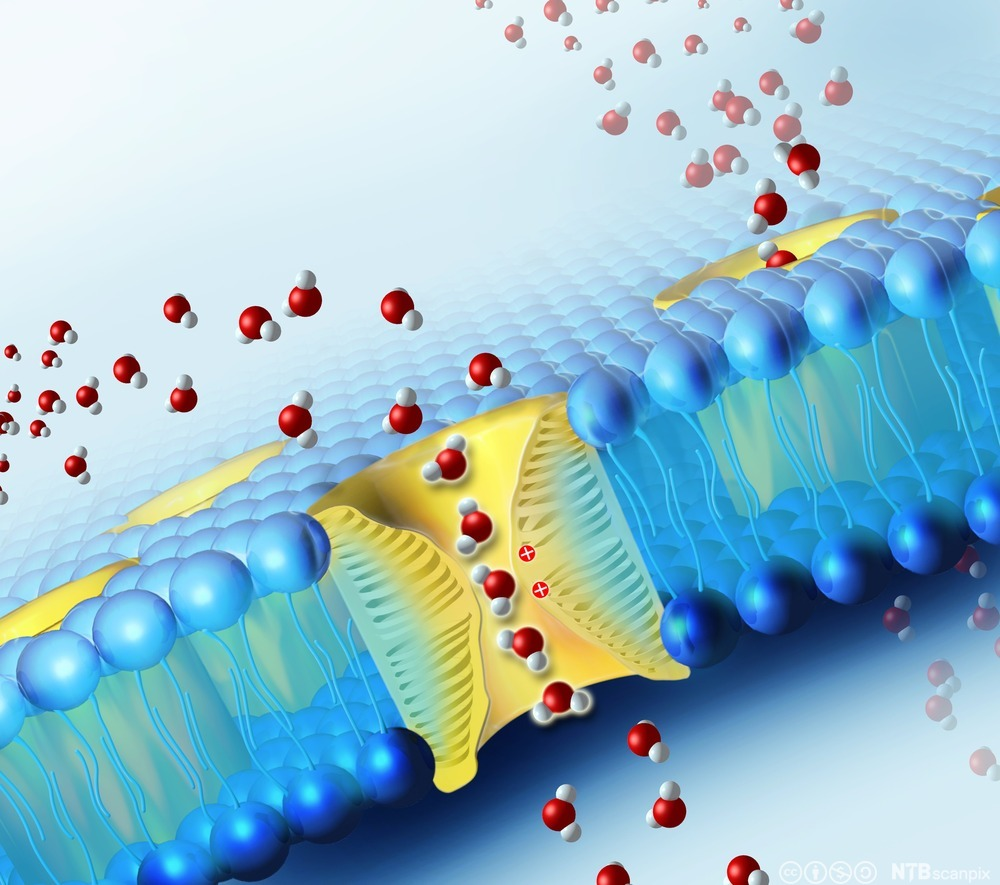
Antidiuretisk hormon (ADH), også kjent som vasopressin, skilles ut fra hypofysens baklapp når kroppen enten har lavt blodvolum eller høy osmolalitet. Hormonets hovedfunksjon er å bevare vann i kroppen.
I nyrene virker ADH på samlerørene og får dem til å åpne vannkanaler (aquaporiner), slik at vann trekkes tilbake til kroppen i stedet for å skilles ut med urinen. Ved høyere konsentrasjoner kan ADH også føre til mild vasokonstriksjon. Dette bidrar ytterligere til å øke blodtrykket.
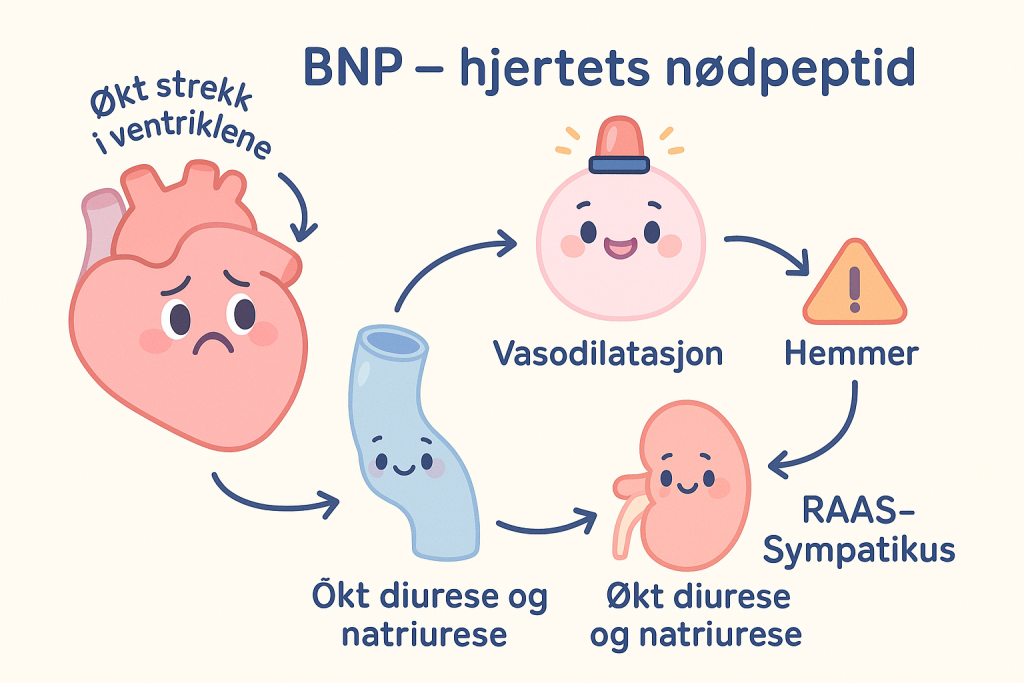
ANP og BNP – kroppens innebygde brems
Når blodvolumet blir for høyt, og atrier og ventrikler strekkes, skilles det ut natriuretiske peptider.
ANP (atrialt natriuretisk peptid) og BNP (brain natriuretic peptide) er hormoner som virker motsatt av RAAS. De fremmer natriumutskillelse (natriurese) og vannutskillelse (diurese), og hemmer både renin, aldosteron og ADH.
Dette gir redusert blodvolum og lavere trykk.
BNP er spesielt nyttig i klinikken – det brukes som blodprøve ved mistanke om hjertesvikt, da høye nivåer ofte tyder på strekk i ventriklene.
Kronisk sympatikusaktivering
Det sympatiske nervesystemet er egentlig laget for kortvarige responser, men ved kronisk aktivering – som ved hjertesvikt eller langvarig stress – kan det bidra til varig blodtrykksøkning og skade.
Langvarig sympatisk stimulering gir:
– Økt frekvens og kontraktilitet (via β₁-reseptorer)
– Økt vasokonstriksjon og motstand (via α₁-reseptorer)
– Stimulerer RAAS og ADH
– Remodellering av hjertet og redusert barorefleksfølsomhet
Dette fører til økt belastning på hjertet og kan forverre sykdomstilstander.
| System | Stimulus | Effekt |
|---|---|---|
| RAAS | Lavt trykk / lavt volum | Vasokonstriksjon, væskeretensjon, ↑ BT |
| ADH | Høy osmolalitet / lavt volum | Vannretensjon, ↑ BT |
| ANP / BNP | Høyt trykk / strekk | Økt natrium- og vanntap, ↓ BT |
| Kronisk sympatikus | Hjertesvikt / stress | ↑ Afterload, RAAS-aktivering, remodellering |
Lokal sirkulasjonsregulering
Sirkulasjonssystemet må kontinuerlig tilpasse seg kroppens behov.
Dette skjer ikke bare gjennom signaler fra hjerne og nerver – mange av de viktigste justeringene skjer lokalt, direkte i vevet.
Dette kalles lokal sirkulasjonsregulering, og gjør at blodstrømmen kan fininnstilles ut fra organenes egne behov, uten sentral styring.
Metabolsk regulering
Når en muskel arbeider, eller et hjerneområde blir aktivt, øker forbruket av oksygen og næringsstoffer. Samtidig akkumuleres avfallsstoffer som CO₂, H⁺ og laktat.
Disse metabolittene virker direkte på arteriolene og får dem til å utvide seg (vasodilatasjon).
Det samme gjelder signalstoffet adenosin, som skilles ut ved høy metabolsk aktivitet og virker sterkt vasodilaterende – særlig i hjertet.
Resultatet er økt blodstrøm til områder med høy aktivitet, uten at hjernen trenger å gi beskjed. Denne mekanismen er spesielt viktig i:
- Hjertet, hvor adenosin er nøkkelen til å øke blodtilførselen under belastning.
- Hjernen, hvor CO₂-nivået er den viktigste vasodilator.
Myogen autoregulering – karveggen føler trykk og justerer tonus
I mange organer, som hjerne og nyrer, er det helt avgjørende at blodstrømmen holdes stabil – selv om blodtrykket i kroppen svinger. Dette sikres blant annet gjennom myogen autoregulering, som er en iboende mekanisme i glatt muskulatur i karveggen.
Når trykket i blodkaret øker, strekkes karveggen – og som en respons trekker den glatte muskulaturen seg sammen. Dette reduserer diameteren og motvirker en for stor økning i blodstrømmen, noe som beskytter vevet mot skade.
På samme måte vil lavere trykk føre til redusert strekk, og karet slapper av for å opprettholde blodtilførselen.
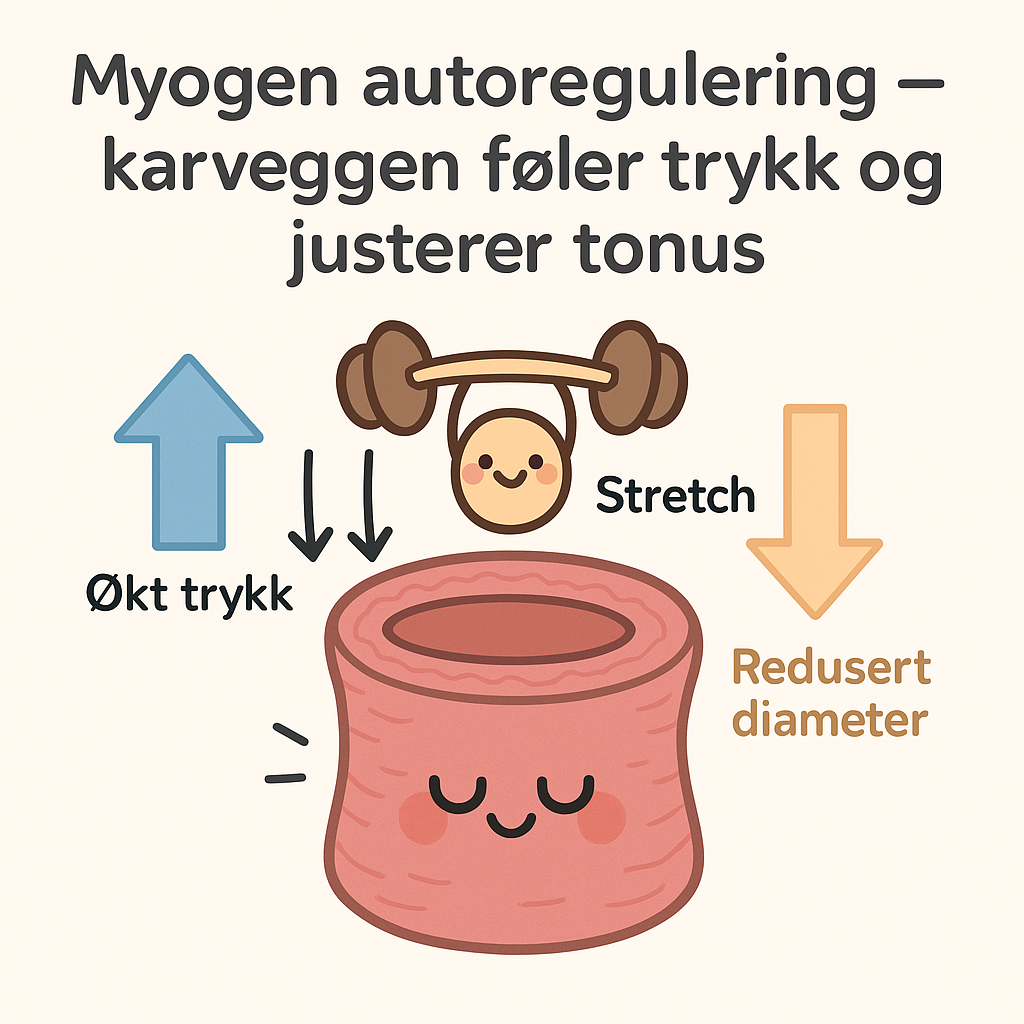
Denne evnen til å justere karnonus i sanntid er et sentralt prinsipp i lokal sirkulasjonsregulering.
👉 Les mer om kartonus og hvordan glatt muskulatur regulerer blodstrøm her → Kartonus
Endotelavhengig regulering – blodårenes egne signaler
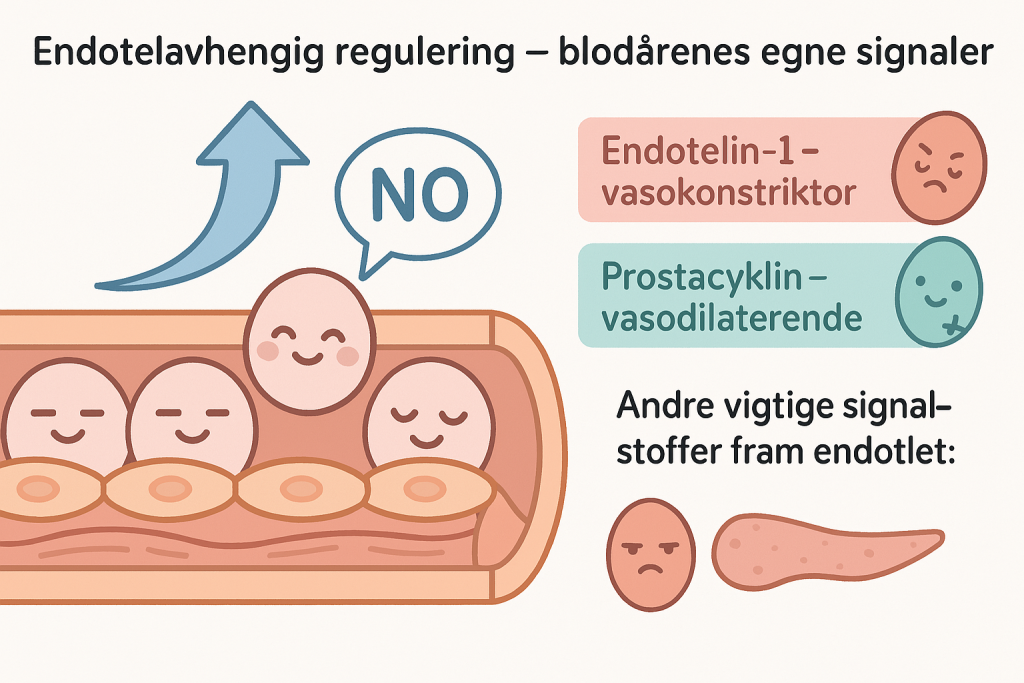
Endotelcellene, som ligger som et lag på innsiden av alle blodkar, spiller en aktiv rolle i å regulere diameteren på karet. Ved økt blodstrøm, eller ved kjemiske stimuli, slipper endotelet ut nitrogenoksid (NO) – et signalstoff som får glatt muskulatur til å slappe av. Dette gir lokal vasodilatasjon og økt blodtilførsel.
Andre viktige signalstoffer fra endotelet inkluderer:
- Endotelin-1 – en kraftig vasokonstriktor, særlig aktiv ved vevsskade og inflammasjon
- Prostacyklin – vasodilaterende og antitrombotisk
Endotelet fungerer dermed som et sanseorgan og en aktiv deltaker i sirkulasjonsreguleringen.
👉 Les mer om dette på egen side her: Endotelfunksjon
Autoregulering i spesifikke organer
Forskjellige organer har ulike behov og spesialiseringer innen lokal regulering:
- Hjertet: Krever konstant blodtilførsel, styres primært av adenosin og oksygennivå. Blodforsyningen skjer hovedsakelig i diastole, og den subendokardielle delen er mest utsatt ved iskemi.
- Hjernen: Har en svært presis autoregulering, og reagerer særlig på endringer i CO₂ og pH. Blodstrømmen holdes konstant mellom MAP 60–150 mmHg.
- Nyrene: Regulerer både blodstrøm og filtrasjon gjennom afferent og efferent arteriolerespons. Reagerer på både trykk og natriumkonsentrasjon i tubuli (via macula densa).
Sirkulasjonsregulering ved fysisk aktivitet
Allerede før selve bevegelsen starter, skjer det en forberedende aktivering i kroppen. Motoriske områder i hjernen sender signaler til det sympatiske nervesystemet i forkant av fysisk aktivitet – en mekanisme som kalles feedforward-regulering. Kroppen begynner altså å forberede seg før det faktiske behovet oppstår.
Dette gir en økning i både hjertefrekvens og kontraktilitet via β₁-adrenerge reseptorer, samtidig som vener trekker seg sammen for å øke venøs tilbakestrømming til hjertet. Samtidig oppstår vasokonstriksjon i kar som forsyner hud og indre organer – noe som omdirigerer blodstrømmen i forkant av den fysiske belastningen.
Når aktiviteten er i gang, forsterkes disse prosessene ytterligere.
Hjertet pumper raskere og kraftigere, og både hjertefrekvens og kontraktilitet stiger betydelig.
Slagvolumet øker som følge av bedre fylling (preload) og mer effektiv tømming, og dette gjør at hjertets minuttvolum kan øke dramatisk – fra 5–6 liter per minutt i hvile til over 20 liter, og hos godt trente personer enda høyere. Dette er nødvendig for å møte det økte oksygenbehovet i arbeidende muskulatur.
Et annet avgjørende trekk ved fysisk aktivitet er hvordan blodstrømmen omdirigeres. Blodkar som forsyner hud, fordøyelsesorganer og nyrer trekker seg sammen under påvirkning av sympatikus.
Samtidig skjer det en lokal vasodilatasjon i arbeidende muskler. Dette skyldes at metabolitter som adenosin, karbondioksid, H⁺-ioner og laktat akkumuleres i vevet og virker direkte på arteriolene. Resultatet er en kraftig utvidelse av blodårene og økt blodtilførsel – ofte slik at opptil 80–90 prosent av hjertets totale minuttvolum ledes mot musklene.
Respirasjonssystemet tilpasses også. Økt pustefrekvens og dypere respirasjon forbedrer oksygenopptaket, samtidig som trykkendringer i thorax og økt muskelaktivitet bidrar til økt venøs retur. Den såkalte muskel- og respirasjonspumpen er avgjørende for å sikre at nok blod returnerer til hjertet under fysisk aktivitet. Sympatisk venekonstriksjon bidrar ytterligere til å opprettholde preload.
Blodtrykket endrer seg også under trening.
Systolisk trykk øker, som følge av det høyere hjerteminuttvolumet, mens det diastoliske trykket ofte holder seg stabilt eller kan synke svakt.
Dette skyldes den reduserte perifere motstanden i arbeidende muskulatur. Resultatet er et økt pulstrykk – noe som er helt normalt under aktivitet.
Over tid fører regelmessig fysisk aktivitet til gunstige langtidsendringer i sirkulasjonssystemet.
Hjertet blir større og sterkere – en fysiologisk hypertrofi – og pumper mer blod per slag. Dette gir lavere hvilepuls og bedre yteevne. Samtidig øker kapillærtettheten i muskulaturen, noe som forbedrer diffusjonsforholdene for oksygen og næringsstoffer. Det skjer også en justering av det autonome nervesystemets balanse: sympatikusaktiviteten reduseres i hvile, og parasympatikus får en mer dominerende rolle. Disse endringene bidrar samlet til bedre oksygentransport, lavere blodtrykk i hvile og økt fysisk kapasitet.
Sirkulasjonsregulering ved blødning og sirkulasjonssvikt
Når kroppen mister blod – enten gradvis eller akutt – settes flere reguleringsmekanismer i gang for å opprettholde blodtrykket og beskytte de livsviktige organene. Sirkulasjonsregulering ved blødning er et samspill mellom det autonome nervesystemet, hormonelle systemer og lokale mekanismer i blodårene. Disse prosessene er livsviktige for å hindre sirkulasjonssvikt – en tilstand der kroppen ikke klarer å opprettholde tilstrekkelig blodgjennomstrømning til organene.
Når blodet forsvinner – hva skjer først?
En akutt blødning fører til at det sirkulerende blodvolumet reduseres. Det gir umiddelbart lavere venøs retur til hjertet, som igjen fører til redusert slagvolum og blodtrykk.
Baroreseptorene i aortabuen og sinus caroticus registrerer dette trykkfallet og sender færre signaler til hjernestammen. Hjernen reagerer lynraskt:
- Den øker sympatisk aktivering, og samtidig hemmer parasympatikus.
- Dette fører til økt hjertefrekvens og økt kontraktilitet.
- Blodårene i hud, nyrer, mage og andre ikke-essensielle organer trekker seg sammen (vasokonstriksjon) for å øke motstanden og sikre trykk.
- Vener kontraherer, slik at mer blod mobiliseres tilbake til hjertet.
Resultatet er at kroppen forsøker å opprettholde minuttvolum og blodtrykk, til tross for det reduserte blodvolumet.
Prioritering av blodstrøm – livsviktige organer først
Ved alvorlig blødning prioriteres sirkulasjonen til hjerne og hjerte. Dette skjer ved at arteriolene i disse organene forblir dilaterte eller påvirkes i mindre grad av den generelle vasokonstriksjonen. Samtidig får hud, nyre og tarm redusert blodtilførsel – en bevisst prioritering fra kroppen.
Denne omfordelingen gjør at pasienten kan bli blek og kald på hender og føtter, få lav urinproduksjon, og etter hvert nedsatt bevissthet hvis perfusjonen til hjernen ikke er tilstrekkelig.
Hormonell forsterkning
Hvis blodtapet fortsetter, trår de hormonelle systemene til for å forsterke den sympatiske effekten:
- RAAS aktiveres, og angiotensin II fører til vasokonstriksjon og økt aldosteronutskillelse, som sparer natrium og vann.
- ADH (vasopressin) skilles ut for å holde på vann og bidra til vasokonstriksjon.
- Samtidig reduseres nivåene av ANP og BNP, for å unngå vanntap.
Denne hormonelle kompensasjonen er avgjørende for å opprettholde blodtrykket i det lange løp, spesielt hvis væske ikke tilføres umiddelbart fra utsiden.
Kliniske tegn og alvorlighetsgrader
Tegnene på sirkulasjonssvikt blir gradvis tydeligere etter hvert som blodtapet øker:
- Mildt sjokk (tap av 15–30 %): Takykardi, normal bevissthet, lett perifer vasokonstriksjon
- Moderat sjokk (30–40 %): Uttalt takykardi, hypotensjon, angst, kald og blek hud
- Alvorlig sjokk (>40 %): Bevisstløshet, organsvikt, livstruende tilstand
Tidlige symptomer er gjerne rask puls, blek hud og redusert urinproduksjon – og jo raskere tiltak settes inn, jo bedre er prognosen.
Sirkulasjonsregulering ved kronisk hjertesvikt
Hjertesvikt oppstår når hjertet ikke lenger klarer å pumpe nok blod til å dekke kroppens behov. Dette kan skyldes ulike underliggende årsaker – som tidligere hjerteinfarkt, klaffefeil eller hypertensjon – men uavhengig av årsaken vil kroppen forsøke å kompensere for det reduserte minuttvolumet. Og nettopp denne kompensasjonen er selve kjernen i forståelsen av hvordan sirkulasjonsreguleringen forandres ved kronisk hjertesvikt.
Kroppens umiddelbare respons
I det øyeblikket blodtrykket faller og perfusjonen til vev trues, settes det sympatiske nervesystemet i gang.
Noradrenalin frisettes fra nerveender i hjertet og kar, og kroppen gjør et ærlig forsøk på å hjelpe:
Hjertet stimuleres til å slå raskere og kraftigere, og blodårene trekker seg sammen for å holde blodtrykket oppe. Vener strammes til slik at mer blod drives tilbake til hjertet, i håp om å fylle det bedre. Sammen fører disse tiltakene til økt hjertefrekvens, økt kontraktilitet, og høyere motstand i det perifere kretsløpet – alt for å opprettholde det livsnødvendige blodtrykket.
Men problemet er at hjertet allerede er svakt. Det klarer ikke å møte kravene, og dermed blir kompensasjonen etter hvert en byrde.
Når nyrene merker at trykket i glomeruli synker, tolker de det som et signal om at væske går tapt. Dette setter i gang det renin-angiotensin-aldosteron-systemet (RAAS), som får blodkarene til å trekke seg ytterligere sammen, og nyrene til å holde tilbake salt og vann. I tillegg skilles det ut antidiuretisk hormon (ADH), som øker kroppens evne til å holde på vann, og dermed volum.
Alt dette kan virke nyttig – og det er det, på kort sikt. Men når hjertet allerede er overbelastet, og volumet øker ytterligere, skaper det en ny utfordring: trykket i hjertets kamre stiger, og blodet begynner å hope seg opp i lungene og kroppen. Dette kan føre til tungpust og hevelser (ødemer), og gir en konstant følelse av å være andpusten og utmattet.
Remodellering og nedbrytning
Kronisk aktivering av sympatikus og RAAS tærer på hjertet. Over tid fører dette til strukturelle forandringer i selve hjertemuskelen – en prosess som kalles remodellering. Hjertet kan bli større og mer slapt (dilatasjon), eller tykkere og stivere (hypertrofi), avhengig av type belastning. Dette gjør det enda mindre effektivt, og setter i gang en ond sirkel med ytterligere reguleringsforsøk fra kroppen, som igjen forverrer tilstanden.
Samtidig ser vi at hjertet blir mindre følsomt for signalene det får. β₁-reseptorene nedreguleres, slik at hjertet ikke lenger responderer like godt på sympatisk stimulering. Det blir som om kroppen roper høyere og høyere til et hjerte som ikke lenger hører etter.
ANP og BNP
Når hjertets kamre blir overfylte og strukket, frisettes atrialt natriuretisk peptid (ANP) og brain natriuretic peptide (BNP). Disse hormonene forsøker å dempe den pågående væskeopphopningen ved å øke utskillelsen av salt og vann i nyrene, og hemme RAAS og ADH. De er kroppens egen motvekt mot overbelastning, men deres effekt er ofte utilstrekkelig når aktiveringen av de skadelige systemene er langvarig og kraftig.
I klinikken bruker vi ofte BNP som en blodprøve ved mistanke om hjertesvikt – høye nivåer tyder på at hjertet er strukket og overbelastet.
Symptomene som speiler reguleringen
De klassiske symptomene ved hjertesvikt er i stor grad konsekvenser av kroppens reguleringsforsøk:
Når blod samler seg i lungene, kjenner pasienten tung pust – spesielt ved anstrengelse eller når man ligger flatt. Når venetrykket stiger og væske presses ut i vevet, kommer ødemene. Når hjertet slår raskere og kraftigere uten å lykkes, fører det til økt oksygenbehov – og til slutt: tretthet, redusert utholdenhet og svikt i flere organer.
Behandling – å bremse kompensasjonen
Moderne behandling av hjertesvikt handler om å gjenopprette balansen. Vi forsøker ikke bare å styrke hjertet, men å stoppe de skadelige kompensasjonsmekanismene:
- ACE-hemmere og ARB demper RAAS og senker motstanden.
- β-blokkere bremser sympatikus og beskytter hjertet mot overstimulering.
- Diuretika fjerner væske og avlaster trykket i hjertet.
- Aldosteronantagonister og nyere legemidler som SGLT2-hemmere bidrar til ytterligere stabilisering.
Sammen bidrar disse tiltakene til å redusere symptomer, bremse sykdomsutviklingen og bedre livskvaliteten.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3