Ekstra- og intracellulære ionekonsentrasjoner
I hjertemuskulaturen er balansen mellom ioner kritisk for normal funksjon. De tre viktigste ionene i denne sammenhengen er natrium (Na⁺), kalium (K⁺) og kalsium (Ca²⁺).
- Ionekonsentrasjoner i cellen:
- Kalium (K⁺) har høy konsentrasjon intracellulært (104–180 mmol/L) og lav konsentrasjon ekstracellulært (5.4 mmol/L). Dette opprettholdes av Na⁺/K⁺-pumpen.
- Natrium (Na⁺) har lav intracellulær konsentrasjon (5–34 mmol/L) og høy ekstracellulær konsentrasjon (140 mmol/L).
- Kalsium (Ca²⁺) har en svært lav intracellulær konsentrasjon (0.0002 mmol/L), men en høyere ekstracellulær konsentrasjon (3 mmol/L).
- Disse konsentrasjonsforskjellene er avgjørende for å generere og regulere aksjonspotensialet i hjertet.
Ioners rolle i aksjonspotensialet
Aksjonspotensialet er en elektrisk signalmekanisme som styrer sammentrekningen av hjertemuskulatur.
- Kalium (K⁺) er viktig for å gjenopprette membranpotensialet under repolarisering.
- Natrium (Na⁺) bidrar til den raske depolariseringen, som er starten på aksjonspotensialet.
- Kalsium (Ca²⁺) spiller en nøkkelrolle i platåfasen, som gjør at hjertemuskelen får tilstrekkelig tid til å trekke seg sammen.
Tabell: Ionaktiviteter i pattedyrhjerte
| Ion | Intracellulær konsentrasjon | Intracellulær aktivitet | Ekstracellulær konsentrasjon | Ekstracellulær aktivitet |
|---|---|---|---|---|
| Natrium (Na⁺) | 5–34 mmol/L | 8 | 140 mmol/L | 110 |
| Kalium (K⁺) | 104–180 mmol/L | 100 | 5.4 mmol/L | 4 |
| Kalsium (Ca²⁺) | 0.0002 mmol/L | 0.0002 | 3 mmol/L | 1 |
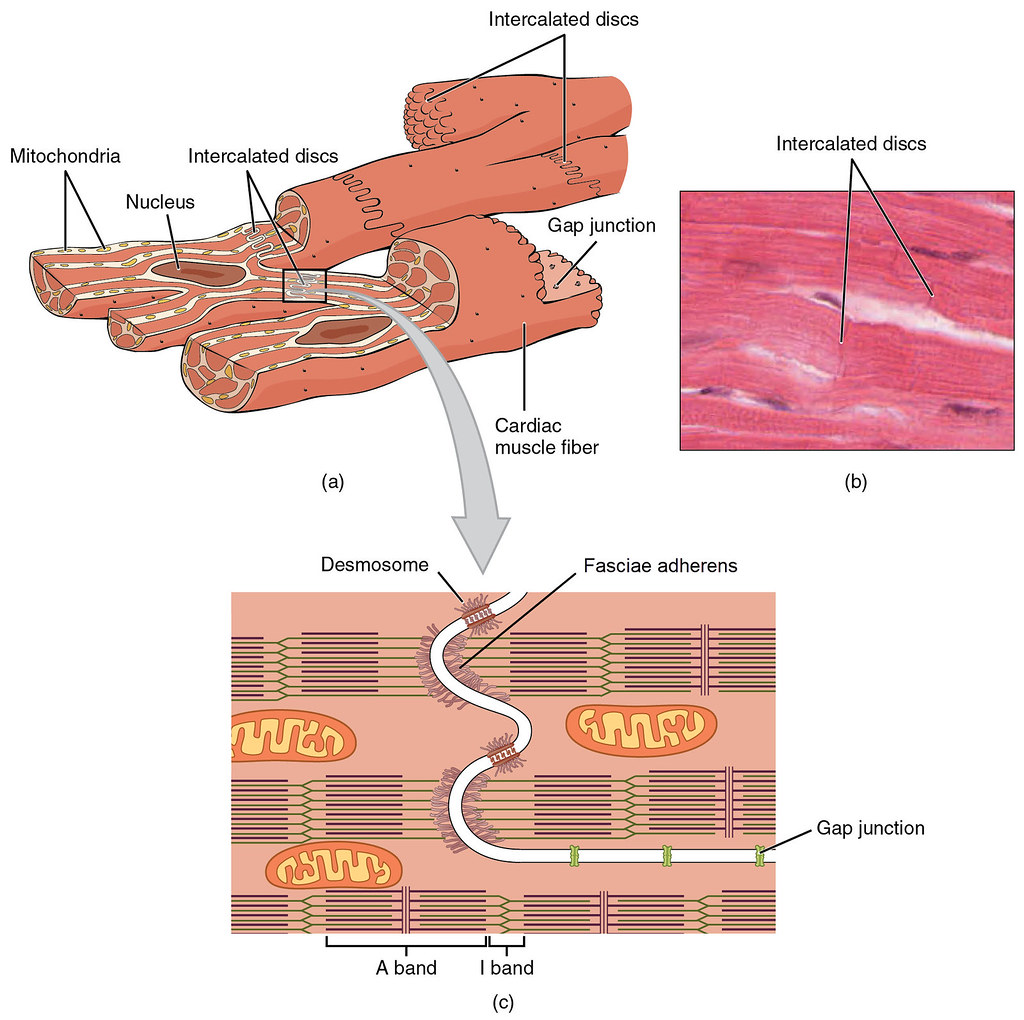
Struktur av hjertemuskulatur
Hjertemuskelceller (kardiomyocytter) er tverrstripede og inneholder én sentral kjerne, mange mitokondrier og velutviklet sarkoplasmatisk retikulum.
Cellene er korte og forgrenede, og danner et tett koblet nettverk som gjør at hele hjertet kan trekke seg sammen koordinert.
Intercalated discs – spesialiserte celleforbindelser
Disse strukturene (interkalerte skiver) er tydelig synlige i mikroskop og finnes der én hjertemuskelcelle møter en annen. De er avgjørende for hjertets funksjon og inneholder tre typer celleforbindelser:
- Desmosomer: Binder cellene mekanisk sammen og forhindrer at de rives fra hverandre under kontraksjon.
- Fasciae adherens: Fester de kontraktile elementene (aktinfilamenter) fra én celle til en annen og overfører kraften mellom cellene.
- Gap junctions: Små kanaler som tillater elektriske signaler (ioner) å spre seg direkte fra én celle til neste. Dette muliggjør synkron sammentrekning av hjertemuskelen – hjertet slår som én enhet.
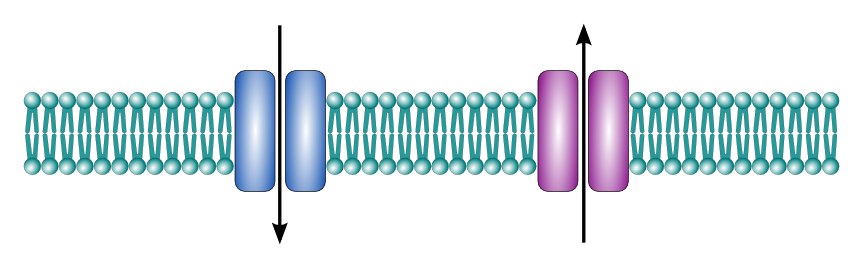
Regulering av ionekanaler – portvakter i cellemembranen
I kroppen vår er kommunikasjon mellom celler helt avgjørende. For at cellene skal kunne sende og motta signaler, må de raskt kunne endre sitt elektriske miljø. Dette gjøres gjennom små spesialiserte proteiner i cellemembranen – ionekanaler – som slipper ioner som natrium, kalium og kalsium inn og ut av cellen. Men disse kanalene står ikke åpne hele tiden. De åpnes og lukkes i respons på bestemte signaler, og dette styres av tre hovedmekanismer.
Spenningstyrte kanaler – elektrisk regulering
Noen kanaler åpnes som respons på endringer i cellens elektriske ladning, altså membranpotensialet. Disse kalles spenningstyrte eller «voltage-gated» kanaler. Når membranpotensialet endres – for eksempel når innsiden av cellen blir mindre negativ – fører det til en formendring i kanalproteinet. Det fungerer litt som en dør med en elektrisk lås: en endring i spenning «låser opp» kanalen og lar ioner strømme inn eller ut.
Et klassisk eksempel er natriumkanaler i nerveceller og muskelceller. Når en celle skal sende et elektrisk signal (et aksjonspotensial), åpnes disse kanalene og slipper natriumioner inn. Dette gjør innsiden av cellen mer positiv, og setter i gang en kjedereaksjon langs hele cellemembranen.
Ligandstyrte kanaler – kjemisk regulering
I andre tilfeller styres kanalene av bestemte kjemiske signalmolekyler, som kalles ligander. Når en slik ligand binder seg til kanalen – omtrent som en nøkkel i en lås – åpnes den. Disse kanalene kalles ligandstyrte, og de reagerer på signaler enten fra utsiden eller innsiden av cellen.
For eksempel, når en nervecelle slipper ut signalstoffet acetylkolin, vil dette stoffet binde seg til en reseptor på overflaten av en muskelcelle. Dette åpner ionekanaler som slipper natrium inn i cellen, noe som fører til at muskelen trekker seg sammen. Andre ligandstyrte kanaler styres av molekyler inni cellen, som kalsium eller cAMP, og fungerer som en del av intracellulær signaloverføring.
Mekanisk styrte kanaler – fysisk påvirkning
En tredje type ionekanal åpnes ikke av elektriske eller kjemiske signaler, men av fysisk kraft. Disse mekanisk styrte kanalene reagerer på strekk, trykk eller bøyning av cellemembranen. Slike kanaler finnes for eksempel i huden, der de registrerer berøring, vibrasjon eller trykk.
Når du trykker på huden, bøyes cellemembranen i de underliggende nervecellene. Dette aktiverer mekanosensitive kanaler, som åpnes og lar ioner strømme inn i cellen. Resultatet er et elektrisk signal som sendes til hjernen og tolkes som berøring.
Koblingen mellom elektrisk signal og kontraksjon i hjertemuskulaturen
Hjertemuskelen har en unik evne til å oversette elektriske signaler til mekanisk arbeid – et fenomen kjent som elektrokjemisk kobling. Når hjertet slår, er det resultatet av en koordinert kjedereaksjon der et elektrisk signal (aksjonspotensial) fører til en økning i intracellulært kalsium, som igjen utløser selve kontraksjonen av muskelcellene.
Fra elektrisk impuls til sammentrekning
Alt begynner med et aksjonspotensial, altså en rask endring i membranpotensialet i hjertemuskelcellens cellemembran – sarkolemma.
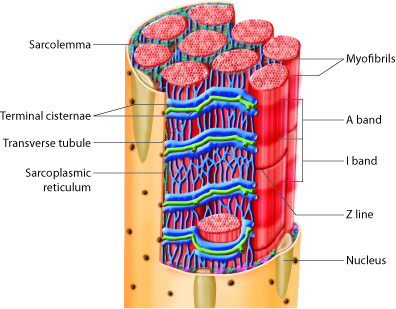
Når dette signalet sprer seg over muskelcellens overflate, åpnes spenningstyrte kalsiumkanaler i membranen, og en liten mengde kalsium strømmer inn i cellen fra det ekstracellulære rommet.
Men dette er bare starten.
Denne lille mengden kalsium fungerer som en «tenner» og aktiverer ryanodinreseptorer (RyR) i det sarkoplasmatiske retikulum (SR), som er hjertemuskelcellens indre kalsiumlager.
Dette fører til en eksplosiv frigjøring av kalsium inn i cytoplasma – en mekanisme kjent som «calcium-induced calcium release».
Kalsium – nøkkelen til kontraksjon
Når kalsiumnivået i cytoplasma øker, binder kalsium seg til proteinet troponin C på de kontraktile elementene i cellen (aktin og myosin). Dette skaper en strukturell endring som gjør at myosin kan binde seg til aktin og «dra» i filamentene – altså en kontraksjon.
Kontraksjonen fortsetter så lenge det finnes kalsium tilgjengelig i cytoplasma, og opphører når kalsium fjernes.
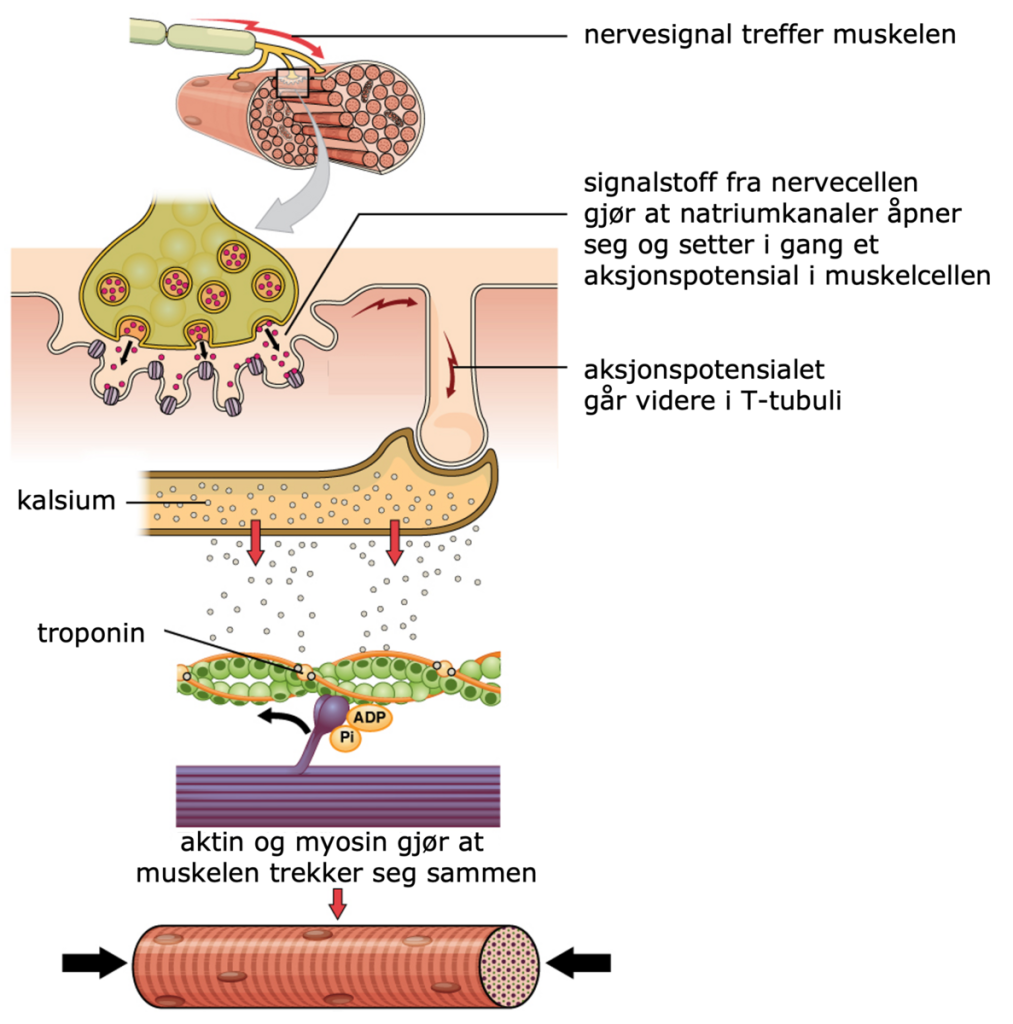
Tilbake til utgangspunktet – avslapning og ioneutveksling
For at muskelen skal slappe av, må kalsiumet fjernes fra cytoplasma. Dette skjer på to hovedmåter:
- Det meste av kalsium pumpes tilbake inn i det sarkoplasmatiske retikulum via SERCA-pumper (Ca²⁺-ATPase), slik at det kan lagres til neste aksjonspotensial.
- En mindre del pumpes ut av cellen via Na⁺/Ca²⁺-utveksleren (NCX) i cellemembranen. Denne bytter ett kalsiumion ut mot tre natriumioner og bidrar til å gjenopprette hviletilstanden.
Mitokondrier – energileverandørene
Kontraksjon er en energikrevende prosess. Hjertemuskelcellene inneholder derfor mange mitokondrier – små «kraftverk» som kontinuerlig produserer ATP. Denne energien er nødvendig både for de kontraktile proteinene og for ionepumpene som transporterer kalsium tilbake til SR eller ut av cellen.
Timing og presisjon – rytmens betydning
Hver hjertesyklus er nøye koordinert. Det elektriske signalet må komme før kalsiumfrigjøringen, som igjen må komme før kontraksjonen. Denne rekkefølgen skjer i løpet av brøkdeler av et sekund, og repeteres regelmessig med hvert hjerteslag. Dersom denne sekvensen forstyrres – enten ved elektriske ledningsforstyrrelser, kalsiumubalanse eller svikt i energitilførselen – kan det føre til rytmeforstyrrelser eller svekket pumpefunksjon.
Eksamensoppgave
De viktigste ionekanalene/strømmene i aksjonspotensialet
Aksjonspotensialet i hjertemuskelceller er en sekvens av nøye koordinerte elektriske hendelser styrt av spesifikke ionekanaler. Tabellen viser hovedkanalene og deres roller:
| Kanal | Ion | Fase | Funksjon |
|---|---|---|---|
| I_Na | Na⁺ | Depolarisering (fase 0) | Åpnes raskt, initierer aksjonspotensialet. |
| I_Ca-L | Ca²⁺ | Platåfase (fase 2) | Langsomme kanaler som opprettholder kontraksjon. |
| I_to | K⁺ | Tidlig repolarisering (fase 1) | Transient outward current som bidrar til kortvarig repolarisering. |
| I_K (I_Kr, I_Ks) | K⁺ | Repolarisering (fase 3) | Forsinkede rektifiseringsstrømmer som gjenoppretter hvilepotensialet. |
| I_K1 | K⁺ | Hvilepotensial (fase 4) | Opprettholder membranens hvilepotensial. |
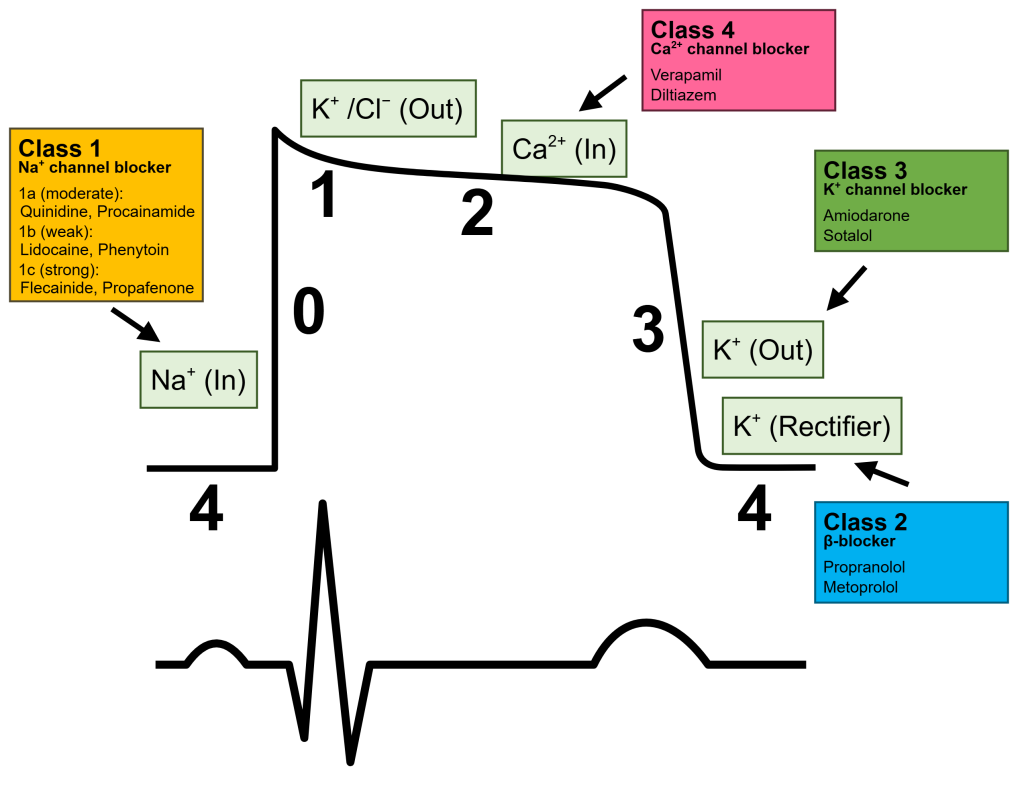
Aksjonspotensialet i hjertemuskulatur
Aksjonspotensialet i hjertemuskelceller
Hjertets aksjonspotensial skiller seg markant fra det man finner i nerveceller og skjelettmuskulatur. Mens nevroner og skjelettmuskelceller har korte aksjonspotensialer som varer bare 1–2 millisekunder, strekker aksjonspotensialet i ventrikkelmuskulatur seg over hele 200–300 millisekunder.
Denne forlengede varigheten skyldes særlig en karakteristisk platåfase, og er avgjørende for hjertets funksjon.
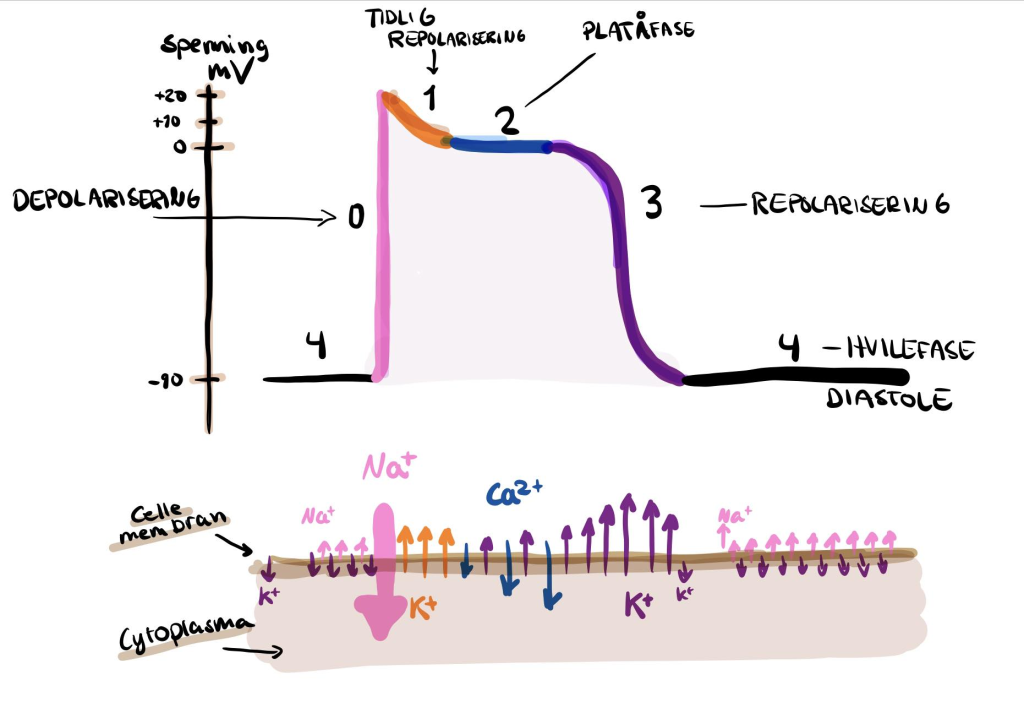
Aksjonspotensialet deles inn i fem faser, fra fase 0 til fase 4, som sammen danner grunnlaget for hjertets rytmiske og kraftfulle kontraksjoner.
Fase 0 – Depolarisering
Aksjonspotensialet starter når membranpotensialet når terskelverdien, omtrent -70 mV.
Dette åpner spenningsstyrte natriumkanaler (Nav1.5), og Na⁺ strømmer raskt inn i cellen.
Den raske innstrømningen av positiv ladning fører til en eksplosiv økning i membranpotensialet – fra rundt -90 mV til +20 mV – på mindre enn 2 millisekunder. Denne raske stigningen representerer oppstartsfasen av aksjonspotensialet, og gjør at hjertemuskelcellen går fra hvile til elektrisk aktivering på et øyeblikk.
Fase 1 – Tidlig repolarisering
Etter den brå depolariseringen lukkes natriumkanalene automatisk, og går inn i en inaktiv tilstand som de ikke forlater før cellen er tilbake i hvilepotensial.
Samtidig åpnes to typer kaliumkanaler, kalt Ito,f og Ito,s, som fører til en kortvarig utadgående strøm av K⁺.
Dette gir en liten, rask repolarisering, som utgjør overgangen til neste fase. Interessant nok varierer antallet av disse kaliumkanalene mellom ulike deler av hjertet, noe som gir regional variasjon i aksjonspotensialets form og varighet.
Fase 2 – Platåfasen
Denne fasen er unik for hjertemuskulatur.
Her åpnes L-type kalsiumkanaler (Cav1.2), og Ca²⁺ strømmer inn i cellen.
Samtidig fortsetter en moderat utstrømning av K⁺, som balanserer membranpotensialet og holder det stabilt rundt 0 mV.
Resultatet er et elektrisk platå som varer i flere titalls millisekunder. Denne fasen er kritisk for kontraksjonsprosessen.
Det innstrømmende kalsiumet utløser nemlig enda mer kalsium fra det sarkoplasmatiske retikulumet (såkalt Ca²⁺-indusert Ca²⁺-frigjøring), noe som aktiverer kontraktilt maskineri og gir hjertet evnen til å trekke seg sammen.
I tillegg bidrar kalsiumet til påfylling av intracellulære lagre.
Fase 3 – Repolarisering
Etter platåfasen lukkes kalsiumkanalene gradvis, mens flere kaliumkanaler – spesielt IKr og IKs – åpnes. Dette fører til økende K⁺-utstrømning, som gjør membranpotensialet mer negativt og bringer cellen tilbake mot hvile.
Na⁺/Ca²⁺-utveksleren (NCX) hjelper også til ved å fjerne overskudd av kalsium fra cytosol, og bidrar til å normalisere cellens indre miljø.
Fase 4 – Hvilefasen
I hvile sørger flere mekanismer for å gjenopprette og opprettholde ionebalansen. Na⁺/K⁺-ATPasen transporterer tre natriumioner ut og to kaliumioner inn per syklus, og holder den grunnleggende ionefordelingen på plass.
Samtidig tar SERCA-pumpen opp kalsium i sarkoplasmatisk retikulum, slik at det er klart for neste kontraksjon.
IK1-kanaler (inward rectifier K⁺-kanaler) bidrar til å stabilisere membranpotensialet nær -90 mV.
Det er verdt å merke seg at disse IK1-kanalene er fraværende i sinusknuten, noe som gjør at pacemakercellene kan depolarisere spontant og initiere et nytt hjerteslag. Husk dette.
Eksamensoppgave
Refraktærperioden og hjertets elektriske ledningssystem
Et sentralt trekk ved hjertets elektriske aktivitet er dets refraktærperiode – en innebygd sikkerhetsmekanisme som hindrer at hjertemuskelen overstimuleres.
Dette er avgjørende for å opprettholde rytmisk og koordinert kontraksjon, og for å hindre tetaniske tilstander som ville vært livstruende i et organ som aldri får hvile.
Den absolutte refraktærperioden begynner med aksjonspotensialets start og varer til godt inn i repolariseringsfasen. I denne perioden er hjertemuskelcellene helt uresponsive for nye signaler – selv sterke stimuli kan ikke utløse en ny kontraksjon. Dette gir hjertet nødvendig tid til å trekke seg sammen, pumpe blod og fylle seg igjen før neste slag.
Etter dette følger den relative refraktærperioden, hvor cellene gradvis gjenvinner evnen til å svare på stimuli. Nå kan et nytt aksjonspotensial genereres, men det krever sterkere stimulering enn normalt. Dette skjer mot slutten av repolariseringen, og sikrer en myk overgang tilbake til hvile og forberedelse på neste syklus.
Hjertets ledningssystem – fra signal til sammentrekning
Den elektriske aktiviteten i hjertet starter i et spesialisert område kalt sinusknuten (SA-knuten), lokalisert øverst i høyre atrium.
Sinusknuten fungerer som hjertets naturlige pacemaker og sender ut rytmiske signaler som setter hjertet i gang.
Fra SA-knuten sprer det elektriske signalet seg gjennom atriene og fører til atriekontraksjon.
Signalet fanges deretter opp av atrioventrikulærknuten (AV-knuten), som fungerer som et kort, men viktig stoppested.
AV-knuten forsinker signalet i noen tideler av et sekund, slik at ventriklene får tid til å fylles ordentlig med blod før de trekker seg sammen.
Etter dette går signalet videre gjennom His-bunten og ned i Purkinje-fibrene, som raskt sprer impulsen til alle deler av ventrikkelveggen. Resultatet er en kraftfull og synkron ventrikkelkontraksjon som pumper blodet effektivt ut i kroppen og lungene.
Denne presise og koordinerte ledningen av elektriske signaler er det som gjør at hjertemuskelen kan arbeide som én helhet, til tross for at den består av millioner av individuelle celler.
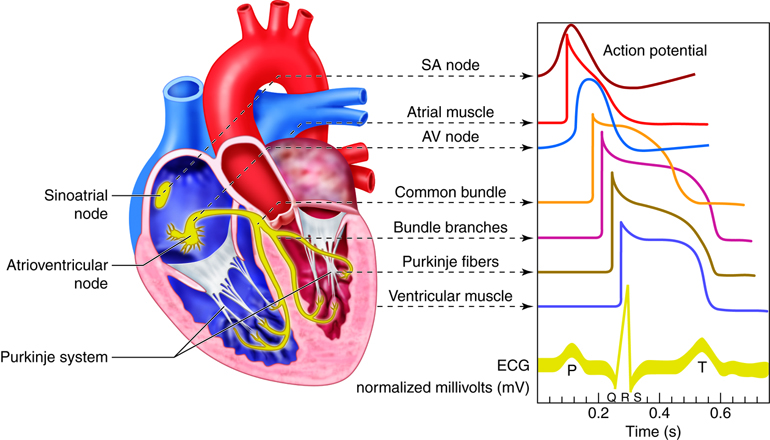
Aksjonspotensialet i ulike hjertetyper – skreddersydd for oppgaven
Hjertets celletyper er spesialisert både i funksjon og i elektriske egenskaper. Selv om alle hjertemuskelceller deler noen felles trekk, har hver type utviklet sitt eget aksjonspotensial, tilpasset sin rolle i hjerteledningssystemet og i kontraksjonen.
Sinusknuten – hjertets pacemaker
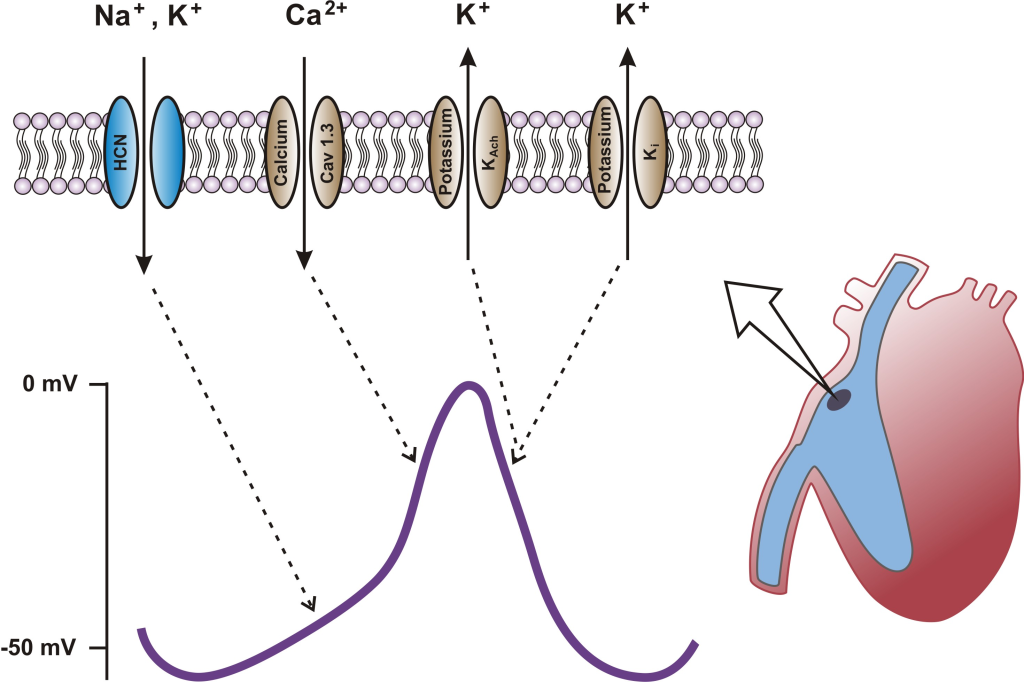
Cellene i sinusknuten (SA-knuten) har en unik evne: de depolariserer spontant og rytmisk uten ytre stimuli.
Dette er mulig fordi de mangler raske natriumkanaler, og i stedet bruker langsomme kalsiumkanaler (I_Ca-L) for å initiere aksjonspotensialet.
Depolariseringen går derfor tregere enn i muskelceller, men dette er en styrke, ikke en svakhet – det gir en jevn og kontrollert rytme.
Et karakteristisk trekk er den spontane depolariseringen i hvile, også kalt fase 4-oppadstigende membranpotensial.
Her spiller særlig den såkalte “funny current” (I_f) HCN, en nøkkelrolle.
Dette er en natriumstrøm som aktiveres av hyperpolarisering – altså i motsatt retning av vanlige depolariserende strømmer.
I_f aktiveres når cellens innside blir mer negativ – det vi kaller hyperpolarisering.
Dette skjer rett etter et hjerteslag, når membranpotensialet er på sitt laveste.
Når I_f åpnes, siver natrium sakte inn, og cellen begynner å depolariseres på nytt – som å dra opp klokken igjen før neste slag.
I tillegg deltar transiente kalsiumkanaler (I_Ca-T) i starten av depolariseringen, før I_Ca-L overtar og fullfører aksjonspotensialet.
Autonom regulering skjer gjennom blant annet I_K(ACh), en kaliumstrøm aktivert av acetylkolin.
Denne strømmen reduserer depolariseringshastigheten og senker hjertefrekvensen – hjertets måte å “bremse ned” på når det får signaler fra det parasympatiske nervesystemet.
AV-knuten – hjertets trafikklys
AV-knuten har en annen spesialitet: den forsinker signalet fra atriene før det slippes videre til ventriklene. Denne forsinkelsen er helt nødvendig for at ventriklene skal få tid til å fylles med blod før de trekker seg sammen.
Cellene her er små, og depolariseringen er langsom, delvis på grunn av færre raske ionekanaler. I tillegg har AV-knuten to ledningsbaner:
- Rask bane leder signalet raskt, men har lang refraktærperiode.
- Langsom bane leder tregere, men kan gjenoppta ledning raskere.
Denne doble banestrukturen kan bli klinisk viktig ved re-entry-aritmier (som AVNRT), der signalet sirkulerer unormalt mellom de to banene.
Atriale celler – raske og effektive
Aksjonspotensialet i atriale muskelceller ligner det i ventriklene, men har en kortere platåfase. Dette skyldes sterkere fase 3 kaliumstrømmer som avslutter aksjonspotensialet raskere. Dette gir rask atriekontraksjon og effektiv overføring av blod til ventriklene.
His-bunten og Purkinje-fibrene – høyhastighetsledere
Etter AV-knuten fortsetter signalet i His-bunten, som leder impulsen inn i høyre og venstre gren, før det raskt sprer seg gjennom Purkinje-fibrene. Disse cellene er spesialisert for høy hastighet, og leder signalet med opptil 4 m/s – det raskeste i hjertet. Dette sikrer at ventrikkene trekker seg sammen nesten samtidig og kraftfullt.
Purkinje-fibrene har mange gap junctions og er store i diameter, noe som reduserer elektrisk motstand og tillater rask ledning.
Ventrikkelceller – kraft og presisjon
Ventrikkelmuskelcellene har et langt aksjonspotensial med en uttalt platåfase (fase 2). Dette gir tid til full kontraksjon og koordinert tømming av blod ut i sirkulasjonen.
Den langsommere ledningen (ca. 0,5 m/s) sørger for at depolariseringen sprer seg fra endokard til epikard – en bevegelse som speiler mekanikken i ventrikkelkontraksjonen.
Eksamensoppgave
Natrium-kalium-pumpen – hjertets elektrokjemiske grunnmur
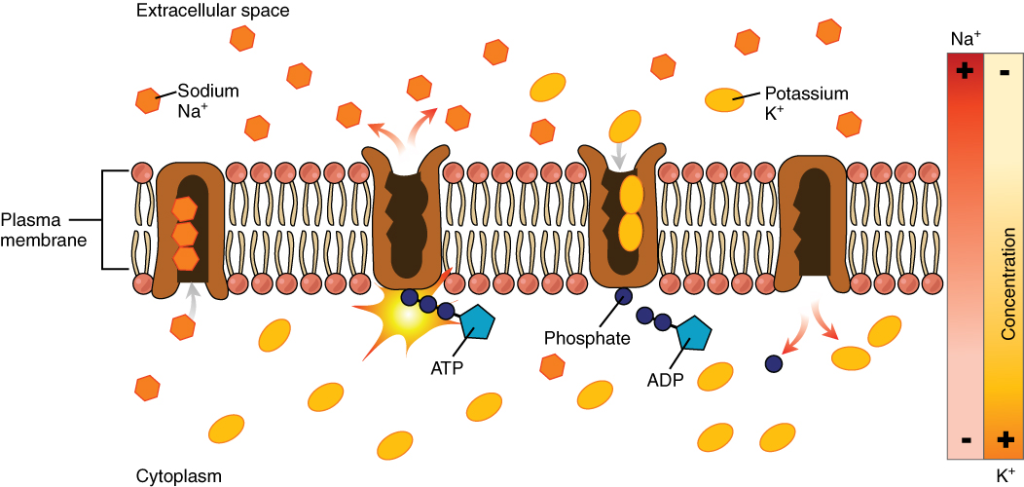
For at hjertemuskelcellene skal kunne generere og lede elektriske signaler, må det være en stabil balanse mellom ionene på innsiden og utsiden av cellemembranen. Denne balansen ivaretas av natrium-kalium-pumpen, også kalt Na⁺/K⁺-ATPasen – et enzym som aktivt transporterer natriumioner ut av cellen og kaliumioner inn.
Pumpen virker ved å bruke energi fra ATP. For hvert molekyl ATP som spaltes, fraktes tre natriumioner ut av cellen og to kaliumioner inn. Dette skaper og opprettholder den negative elektriske spenningen inne i cellen, som er nødvendig for at aksjonspotensialer – hjertets elektriske signaler – skal kunne oppstå. Uten denne pumpen ville cellen gradvis miste evnen til å sende signaler, og hjertets rytme ville kollapse.
Virkemåten er trinnvis, men skjer kontinuerlig og effektivt: Natrium binder seg til pumpen fra innsiden. Når ATP spaltes, endres pumpens form, og natrium slippes ut. Deretter binder kalium seg på utsiden, og pumpen vender tilbake til sin opprinnelige form og slipper kalium inn i cellen. Resultatet er en stabil ionefordeling som både bidrar til hvilemembranpotensialet og gjør cellen klar for neste elektriske impuls.
Denne pumpens aktivitet er også avgjørende for andre transportsystemer i cellen. For eksempel utnytter mange andre transportproteiner den elektrokjemiske gradienten pumpen skaper, til å frakte glukose, kalsium og andre viktige molekyler. Derfor er Na⁺/K⁺-ATPasen ikke bare viktig for hjertets elektriske stabilitet, men også for næringstilførsel og signaloverføring.
Regulering av hjertets rytme – samspill mellom gass og brems
Hjertets rytme styres i utgangspunktet av sinusknuten – et lite område i høyre forkammer som spontant genererer elektriske impulser.
Men det er ikke slik at hjertet slår i et konstant tempo hele døgnet. I stedet finjusteres rytmen kontinuerlig etter kroppens behov gjennom påvirkning fra det autonome nervesystemet.
Når kroppen er i hvile, dominerer den parasympatiske aktiviteten. Dette nervesystemet fungerer som en brems og senker hjertefrekvensen ved hjelp av signalstoffet acetylkolin.
Acetylkolin virker på egne reseptorer i sinusknuten og åpner spesielle kaliumkanaler som gjør membranpotensialet mer negativt – altså hyperpolarisert.
Samtidig hemmes produksjonen av cAMP, et signalmolekyl som vanligvis øker hjertets tempo. Resultatet er langsommere spontan depolarisering, og hjertet slår sjeldnere – ofte ned mot 40 slag per minutt hos godt trente mennesker.
Når kroppen derimot trenger mer blod og oksygen, som under fysisk aktivitet eller stress, aktiveres det sympatiske nervesystemet. Da frigjøres noradrenalin, som binder seg til β₁-reseptorer i sinusknuten.
Dette aktiverer enzymet adenylyl syklase, som igjen øker mengden cAMP. Økt cAMP aktiverer proteinkinase A, som fosforylerer spesifikke ionekanaler og øker strømmen av både natrium og kalsium inn i cellen. Natrium kommer særlig inn via såkalte “funny current”-kanaler – spesielle kanaler som åpner seg når membranpotensialet blir mer negativt enn normalt. Dette fører til at pacemakercellene når terskelverdien raskere og fyrer oftere. Resultatet er en raskere hjerterytme – typisk opp mot 180–200 slag per minutt hos unge, friske individer.
Dette samspillet mellom brems og gass – mellom parasympatisk og sympatisk aktivitet – gjør hjertet til en utrolig fleksibel pumpe. Det slår rolig og økonomisk i hvile, men kan akselerere dramatisk når behovet oppstår. På den måten er hjertet alltid i stand til å møte kroppens krav – uansett om du hviler, løper, blir redd, eller sover.
Takykardi – når hjertet slår for raskt
Takykardi er en tilstand der hjertet slår unormalt raskt, vanligvis over 100 slag per minutt i hvile. Dette kan skyldes ulike forstyrrelser i hjertets elektriske system, og mekanismene bak takykardi kan grovt deles inn i fire hovedkategorier: reentry, fokal aktivitet, økt automatisitet og trigget aktivitet.
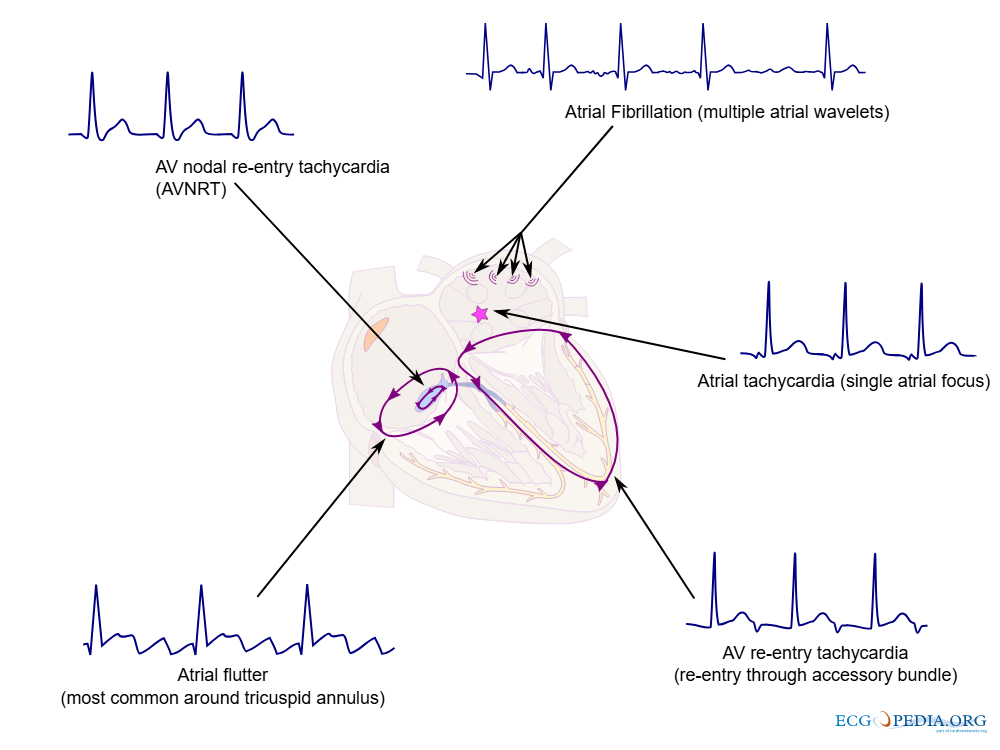
Reentry – elektrisk rundkjøring
Den vanligste årsaken til takykardi er reentry, der et elektrisk signal fanges i en sirkulær bane og går i ring rundt et anatomisk eller funksjonelt hinder i hjertet. I stedet for å spre seg normalt gjennom hjertemuskelen, fortsetter signalet å aktivere det samme området gjentatte ganger. Dette kan føre til rask og vedvarende aktivering av hjertet. Reentry-mekanismer er spesielt vanlige ved rytmeforstyrrelser i både forkamre (f.eks. atrieflutter) og hjertekamre (f.eks. ventrikkeltakykardi).
Fokal aktivitet – en overivrig pacemaker
Ved fokal takykardi oppstår rytmeforstyrrelsen fra ett enkelt punkt i hjertet som begynner å sende ut raske elektriske signaler. Dette punktet kan overstyre hjertets normale pacemaker (sinusknuten), og resultatet blir en rask hjerterytme. Fokal aktivitet kan være forårsaket av medfødte elektriske forstyrrelser, betennelser eller arrvev etter infarkt. Slike ektopiske fokus kan ligge hvor som helst i atriene eller ventriklene.
Økt automatisitet – celler som starter på egenhånd
Automatisitet er cellers evne til å starte elektriske impulser spontant. Normalt er det sinusknuten som står for denne aktiviteten, men ved økt automatisitet kan andre celler i hjertet også begynne å fyre av elektriske signaler. Dette kan skyldes økt stimulering fra det sympatiske nervesystemet, endringer i ionekanaler eller elektrolyttforstyrrelser. Disse impulsene kan trigge raske rytmer, særlig i atriene.
Trigget aktivitet – ekstra signaler fra ustabile celler
Noen ganger kan hjerteceller sende ut uønskede ekstrasignaler, enten under eller rett etter et normalt aksjonspotensial. Dette kalles trigget aktivitet, og det finnes to typer:
- Tidlige etterdepolariseringer (EAD): Oppstår før cellen har fullført sin repolarisering. Dette skjer oftest ved forlenget aksjonspotensial, som ved elektrolyttforstyrrelser eller bruk av visse medikamenter.
- Sene etterdepolariseringer (DAD): Oppstår etter at aksjonspotensialet er avsluttet. Disse skyldes ofte opphopning av kalsium inne i cellen, som igjen fører til ustabilitet i membranpotensialet.
Ventrikkeltakykardi – farlig rytme i hjertekamrene
Ventrikkeltakykardi (VT) er en alvorlig rytmeforstyrrelse hvor de elektriske signalene i hjertekamrene løper løpsk, ofte som følge av en reentry-mekanisme. I stedet for at signalet spres systematisk via His–Purkinje-systemet, går det i ring rundt et skadet område i hjertekammerveggen – som ved arrvev etter et tidligere infarkt.
Denne kontinuerlige elektriske sløyfen får ventriklene til å slå så raskt at de ikke rekker å fylle seg skikkelig med blod mellom slagene. Konsekvensen blir redusert slagvolum og dårligere blodforsyning til vitale organer. Pasienten kan oppleve svimmelhet, brystsmerter eller besvime – og i verste fall kan VT utvikle seg til ventrikkelflimmer og hjertestans dersom det ikke behandles raskt.
Hvordan hemme reentry-mekanismer medikamentelt?
To hovedstrategier for å forhindre reentry:
- Forsinke overledning:
- Medikamenter som blokkerer natriumkanaler (eks. flekainid) reduserer overledningshastigheten. Forhindrer at signalene fullfører reentry-sirkelen.
- Forlenge refraktærtid:
- Medikamenter som blokkerer kaliumkanaler (eks. sotalol) forlenger repolariseringen.
- Øker den effektive refraktærtiden, noe som gjør det umulig for signaler å reise rundt.
Lang QT-tid syndrom
Hva er lang QT-tid syndrom?
Lang QT-tid syndrom er en hjertesykdom der hjertet bruker for lang tid på å lade seg opp igjen mellom hvert hjerteslag. Dette kalles forlenget repolarisering av hjertemuskulaturen.
Når vi ser på et EKG (hjertediagram), måler vi denne tiden som QT-intervallet. Dette intervallet viser hvor lang tid hjertet bruker på både å trekke seg sammen (depolarisering) og å lade seg opp igjen (repolarisering).
Når denne tiden blir for lang, kan det være farlig fordi det kan føre til unormal hjerterytme (arytmier). En spesielt farlig type arytmi som kan oppstå kalles torsades de pointes, som kan være livstruende fordi hjertet ikke klarer å pumpe blod effektivt.
Årsaker til lang QT-tid
- Ionekanaldysfunksjon – Problemer med hjertets elektriske system:
- For mye natrium (Na⁺) strømmer inn i hjertecellene når de skal lade seg opp igjen. Dette er som å helle vann i et glass som allerede er fullt.
- For lite kalium (K⁺) strømmer ut av cellene, noe som gjør at opplading tar lengre tid enn normalt.
- Genetiske mutasjoner:
- Dette er feil i arvematerialet som påvirker hjertets ionekanaler. De vanligste typene (LQT1, LQT2 og LQT3) påvirker hvordan kalium og natrium beveger seg inn og ut av hjertecellene.
- Ervervede årsaker – Ting som kan skje i løpet av livet:
- Noen medisiner kan blokkere kaliumkanalene og dermed forstyrre hjertets elektriske system.
- Ubalanse i kroppens salter (elektrolytter) som kalium og magnesium kan også forårsake problemet.
Mekanisme
- Når hjertet bruker for lang tid på å lade seg opp igjen, kan det oppstå uønskede elektriske signaler som kalles tidlige etterdepolariseringer (EAD):
- Disse uønskede signalene kan starte nye hjerteslag før hjertet er klart, som kan føre til farlige rytmeforstyrrelser.
- Dette skjer særlig når kaliumkanalene ikke fungerer som de skal, eller når natriumkanalene forblir åpne lenger enn de burde.
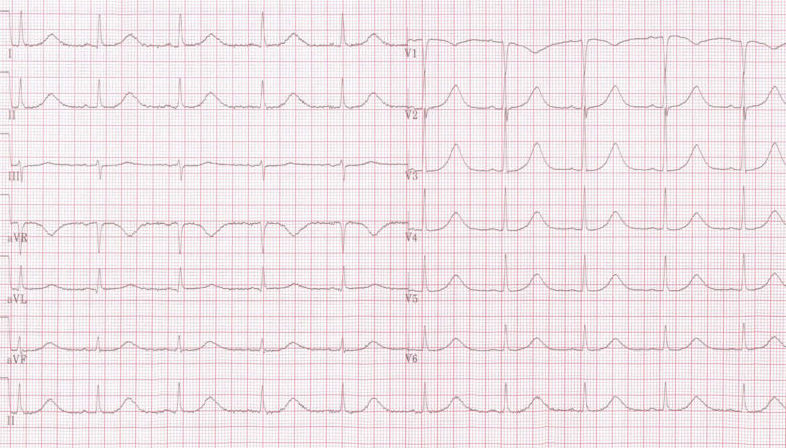
EKG-funn
- QT-tiden målt på EKG er forlenget.
- Den nedre figuren viser en episode av torsades de pointes, karakterisert av polymorf ventrikeltakykardi med en vridende morfologi.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3
❓ Test deg selv
Obs, tomt! Kommer etterhvert <3
Legg gjerne til tilbakemeldinger, rettelser eller spørsmål under!
Legg igjen en kommentar