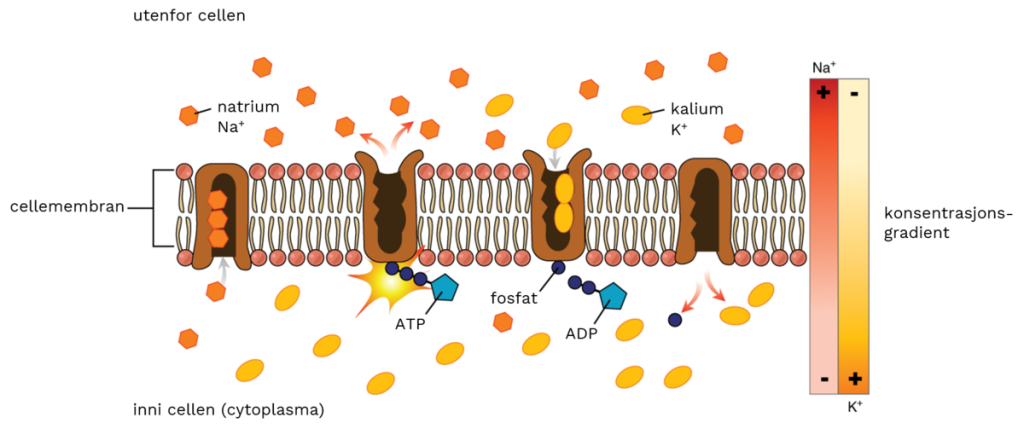
Prinsipper for transmembran transport
Cellemembranen er ikke bare en fysisk barriere; den er en selektiv portvakt som nøye regulerer hva som slipper inn og ut av cellen. For at cellen skal fungere, må den kunne ta opp næringsstoffer, kvitte seg med avfallsstoffer, regulere ionebalanser og reagere på signaler fra omgivelsene. Dette krever presis og kontrollert transport over membranen.
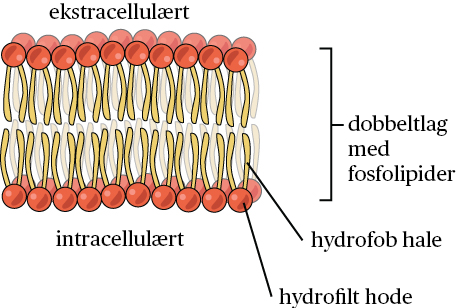
Fosfolipidlaget som utgjør membranens kjerne er i seg selv ugjennomtrengelig for de fleste vannløselige stoffer. Bare små, upolare molekyler som oksygen og karbondioksid kan bevege seg fritt gjennom det hydrofobe indre av membranen. Derfor trenger de fleste stoffer hjelp for å krysse denne barrieren, og det er her membranproteiner kommer inn.
Disse proteinene fungerer som spesialiserte porter og transportører som gjør det mulig å frakte ulike molekyler over membranen.
Transporten kan skje på to grunnleggende måter: med eller mot molekylets konsentrasjonsgradient.
Når et stoff beveger seg fra et område med høy konsentrasjon til et område med lavere konsentrasjon, sier vi at det følger konsentrasjonsgradienten. Denne formen for transport krever ingen energi og betegnes som passiv. Motsatt har vi aktiv transport, som krever tilførsel av energi – vanligvis i form av ATP – fordi molekylet må presses mot sin naturlige gradient, altså fra lav til høy konsentrasjon.
Transportproteiner kan fungere på ulike måter. Noen danner vannfylte kanaler som åpnes og lukkes for bestemte ioner, som natrium eller kalsium. Andre, som bærerproteiner, binder seg til molekylet som skal transporteres, og gjennomgår en formendring som gjør det mulig å frakte stoffet over membranen. Enkelte proteiner fungerer som pumper, der de aktivt bruker energi for å flytte ioner eller andre molekyler dit de trengs. Uansett hvilken mekanisme som brukes, er det viktig å forstå at disse proteinene er høyt spesialiserte – hver type transportprotein kjenner igjen og håndterer bare et begrenset sett med molekyler.
For ladede partikler, som ioner, spiller ikke bare konsentrasjonen en rolle – også den elektriske ladningsforskjellen mellom innsiden og utsiden av cellen påvirker transporten.
Innsiden av cellen er vanligvis svakt negativt ladet sammenlignet med utsiden, og dette elektriske potensialet kan enten tiltrekke eller frastøte ioner. Transporten av slike ladede stoffer påvirkes altså både av konsentrasjonsforskjellen og av den elektriske spenningen over membranen. Samlet kalles dette den elektrokjemiske gradienten, og det er denne gradienten som bestemmer hvordan og i hvilken retning ioner beveger seg.
Om du vil lese mer om cellemembran og permeabilitet, gå hit: Lipider og membraner
Passiv transport
Transport over cellemembranen kan skje på flere måter, og en av de mest grunnleggende mekanismene er passiv transport. Dette er transport som ikke krever energi fra cellen. I stedet utnytter cellen de naturlige bevegelsene til molekyler som søker balanse – de beveger seg fra områder med høy konsentrasjon til områder med lavere konsentrasjon. Det skjer spontant, akkurat som mennesker som sprer seg ut i et rom for å unngå trangt kaos: der det er mange, vil de søke seg mot der det er færre.
Passiv transport deles inn i simpel diffusjon og fasilitert diffusjon, og inkluderer også osmose, som er en spesialisert form for diffusjon av vann.
Simpel diffusjon
Noen stoffer er små og fettløselige nok til å bevege seg rett gjennom det hydrofobe lipidlaget i cellemembranen, uten hjelp fra proteiner. Dette gjelder for eksempel gasser som oksygen (O₂) og karbondioksid (CO₂), samt fettløselige stoffer som hormoner.
Etter at vi har pustet inn oksygenrik luft, diffunderer oksygen fritt over cellemembranen og inn i cellene, der det brukes i mitokondriene. Samtidig diffunderer CO₂, et avfallsprodukt, ut av cellene og transporteres til lungene for utpust.
Fasilitert diffusjon
Større eller polare molekyler, som glukose eller ioner, kan ikke krysse det hydrofobe lipidlaget alene.
I stedet må de bruke spesialiserte transportproteiner. Dette er fortsatt passiv transport – det krever ikke energi – men det foregår gjennom egne «porter» i membranen.
Bærerproteiner (transportører)
Bærerproteiner binder seg til et spesifikt molekyl, som for eksempel glukose, og endrer form (konformasjon, noter deg dette ordet) slik at molekylet kan fraktes fra én side av membranen til den andre. Transporten skjer med konsentrasjonsgradienten – altså fra høy til lav konsentrasjon.
Eksempel: GLUT2
GLUT2 finnes blant annet i lever, tarm og bukspyttkjertel, og fungerer som en bidireksjonell glukosetransportør.
Etter et måltid, når glukosenivået i blodet er høyt, diffunderer glukose passivt inn i levercellene via GLUT2.
I fasteperioder kan den samme transportøren slippe glukose ut av cellen for å opprettholde blodsukkeret. GLUT2 har lav affinitet for glukose, noe som gjør den perfekt for situasjoner med høye konsentrasjoner – den slipper glukose raskt gjennom.
Kanaler og ionekanaler
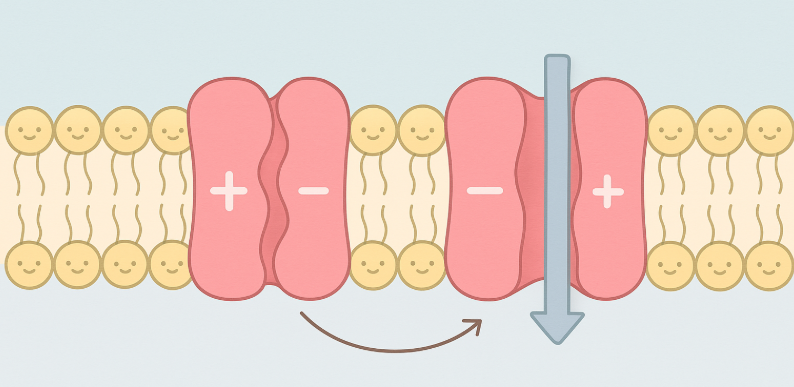
I stedet for å binde og frakte molekyler én etter én, som bærerproteiner gjør, fungerer ionekanaler som vannfylte porer. De åpner og lukker seg for spesifikke ioner, og lar dem strømme raskt gjennom membranen.
Det finnes flere typer:
- Aquaporiner: Slipper vannmolekyler raskt og selektivt gjennom. Viktig for å regulere vannbalansen i celler og vev.
- Ionekanaler: Spesialiserte for bestemte ioner som Na⁺, K⁺, Ca²⁺ og Cl⁻. De fleste er “gated”, altså de åpnes kun ved spesifikke stimuli: spenning (spenningsstyrte), ligandbinding (ligandstyrte), eller mekanisk trykk (mekanisk aktiverte).
- Gap junctions: Direkte forbindelser mellom naboceller som tillater utveksling av ioner og små molekyler. Viktig for elektrisk kobling, f.eks. i hjertet.
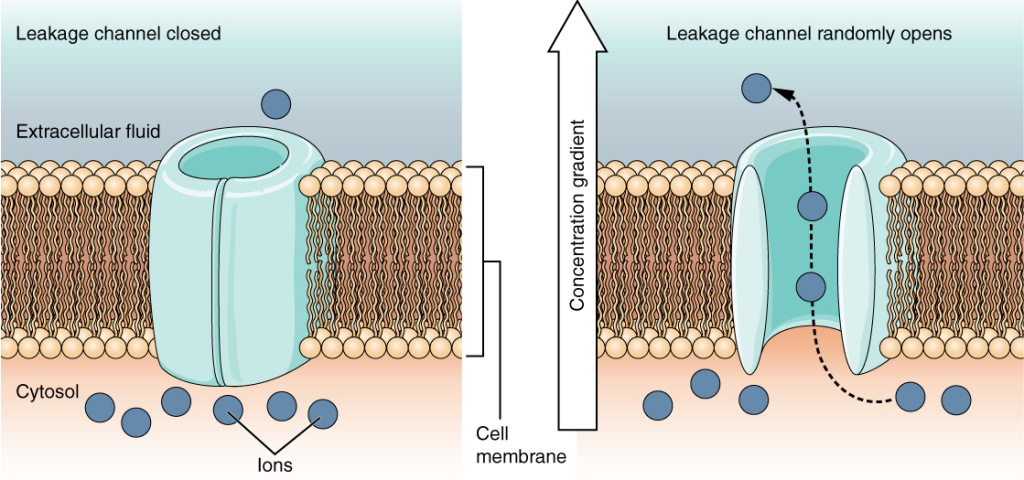
Eksempel: K⁺-lekkasjekanalen
K⁺-lekkasjekanaler lar kalium sakte lekke ut av cellen.
Dette er avgjørende for å opprettholde cellens hvilemembranpotensial – altså den elektriske spenningen over membranen når cellen er i ro.
Kalium er mye mer konsentrert inne i cellen (ca. 140 mM) enn utenfor (ca. 5 mM), og når det lekker ut, etterlater det negativ ladning bak seg. Dette skaper en elektrisk gradient, som er viktig for cellens evne til å sende elektriske signaler, særlig i nerveceller.
Viktig her er også Na⁺/K⁺-pumpen, som aktivt opprettholder denne gradienten ved å pumpe Na⁺ ut og K⁺ inn (mer om dette under aktiv transport).
Membranpotensial og elektrokjemisk gradient
Når det er ulik fordeling av ladede partikler (ioner) på hver side av membranen, oppstår det et elektrisk potensial – en spenningsforskjell.
Innsiden av cellen er vanligvis negativ i forhold til utsiden, og dette hvilepotensialet er viktig for mange cellefunksjoner, spesielt i nerve- og muskelceller.
Transporten av ioner påvirkes derfor ikke bare av hvor det er mest av dem (konsentrasjonsgradient), men også av elektriske krefter. Samlet kalles dette den elektrokjemiske gradienten – en kombinasjon av kjemisk og elektrisk drivkraft.
Osmose – diffusjon av vann
Osmose er bevegelsen av vann over en semipermeabel membran fra et område med lav konsentrasjon av løste stoffer (høy vannkonsentrasjon) til et område med høy konsentrasjon av løste stoffer (lav vannkonsentrasjon). Vannet forsøker å utjevne konsentrasjonsforskjellen.
Vann beveger seg gjennom cellemembranen hovedsakelig via aquaporiner. Dette er egne kanaler for vann.
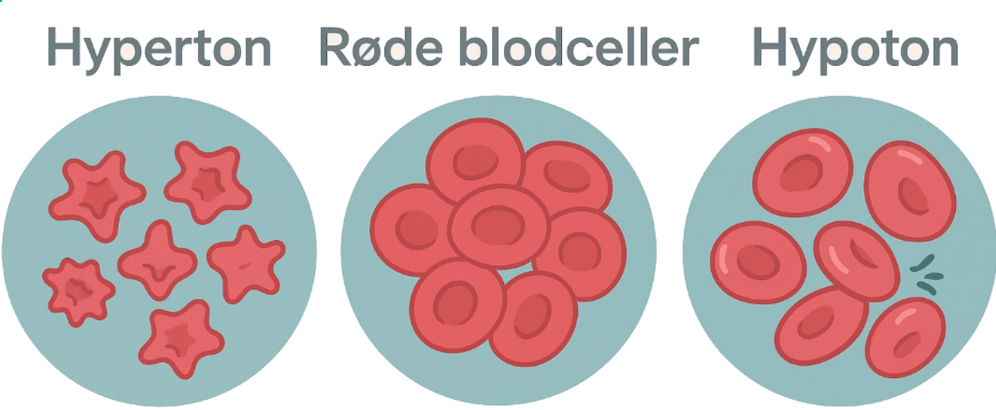
Røde blodceller i en hypoton løsning (for eksempel rent vann) tar opp vann og sveller – noen ganger til de sprekker. I en hyperton løsning (f.eks. sterkt saltvann), mister de vann og krymper. Osmotisk balanse er altså kritisk for cellens overlevelse.
Aktiv transport – mot strømmen, med energi
Primær aktiv transport
Noen ganger holder det ikke for cellen å la molekyler følge sine naturlige bevegelser. I stedet må cellen jobbe aktivt for å opprettholde livsnødvendige forskjeller i konsentrasjon mellom innsiden og utsiden.
Dette skjer gjennom aktiv transport – en type transport som krever tilførsel av energi, vanligvis i form av ATP. I motsetning til passiv transport, som følger konsentrasjonsgradienten, går aktiv transport mot gradienten.
Molekylene presses fra et område med lav konsentrasjon til et område med høyere konsentrasjon, ofte for å bygge opp eller opprettholde elektrokjemiske gradienter som cellen er helt avhengig av.
Den mest kjente og kanskje viktigste pumpen i cellemembranen er natrium-kalium-pumpen, eller Na⁺/K⁺-ATPasen.
Dette er en ATP-drevet pumpe som hele tiden flytter tre natriumioner ut av cellen og to kaliumioner inn, for hvert ATP som forbrukes.
Denne pumpen sørger for at natriumkonsentrasjonen holdes høy utenfor cellen og lav inni, mens kalium holdes høyt inni og lavt utenfor.
Forskjellene er betydelige – natrium er typisk 10–30 ganger mer konsentrert ekstracellulært, mens kalium er 10–30 ganger mer konsentrert intracellulært. Dette skaper en tydelig konsentrasjonsgradient, men også et elektrisk potensial – fordi det pumpes ut flere positive ladninger enn det pumpes inn.
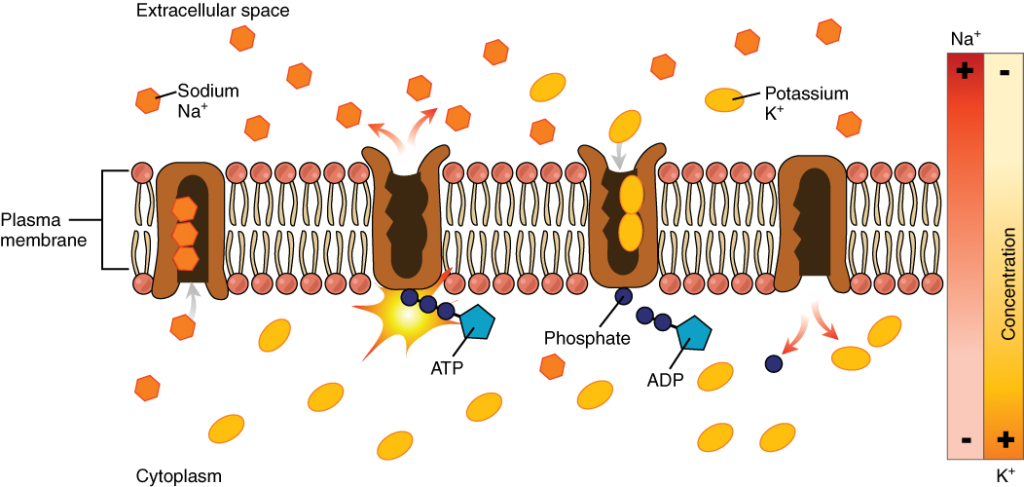
Pumpens funksjon er avgjørende for å opprettholde det negative hvilepotensialet i celler, spesielt i nerve- og muskelceller.
Det er også helt sentralt for osmotisk balanse – dersom ionene ikke aktivt ble holdt på plass, ville vann strømme ukontrollert inn i cellen, som til slutt kunne svelle og sprekke. Det anslås at en betydelig andel av cellens samlede energiforbruk går med til å drive nettopp denne pumpen.
Sekundær aktiv transport
Energi kan også brukes indirekte for å transportere stoffer – dette kalles sekundær aktiv transport.
Her brukes ikke ATP direkte, men energien som ble brukt til å bygge opp en konsentrasjonsgradient – typisk for natrium – brukes videre til å frakte andre molekyler.
Når natrium strømmer tilbake inn i cellen, ned sin gradient, kobles denne bevegelsen til transporten av et annet molekyl. Dersom begge stoffene går i samme retning, kalles det symport. Dersom de går i motsatt retning, kalles det antiport.
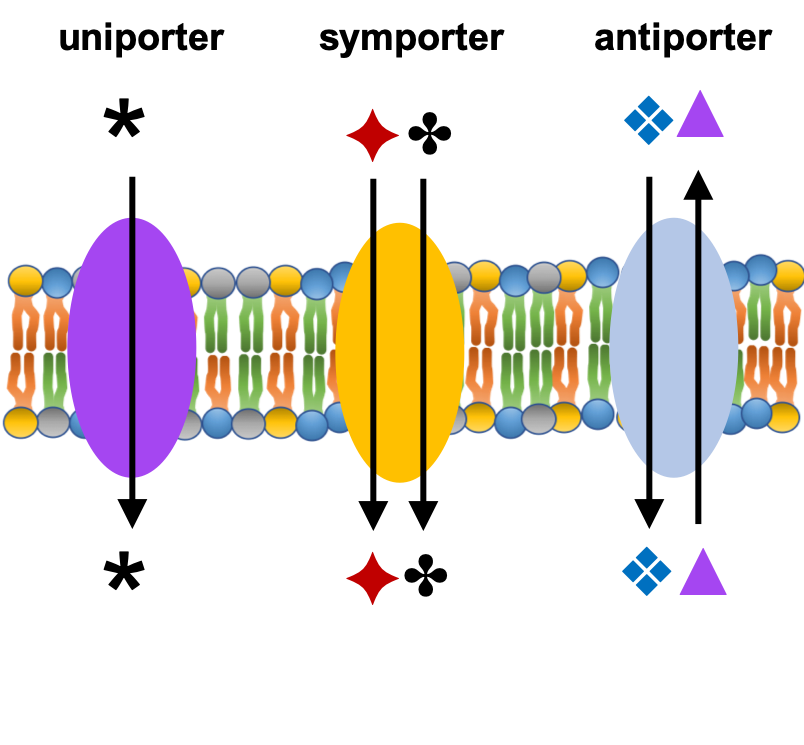
Et godt eksempel på symport finner vi i tarmen, der natrium-glukose-kotransporten er avgjørende for å kunne ta opp glukose fra tarmlumen, spesielt når glukosekonsentrasjonen i tarmen er lav.
Transportøren binder både et natriumion og et glukosemolekyl på den ene siden av membranen. Når begge er bundet, skjer en konformasjonsendring, og molekylene slippes inn i cellen.
Energi brukes ikke direkte i denne prosessen, men den er avhengig av at natriumgradienten opprettholdes – noe som skjer via Na⁺/K⁺-pumpen i en annen del av membranen. Dette er faktisk ganske viktig i forhold til hvordan glukose blir tatt opp i tarmen.
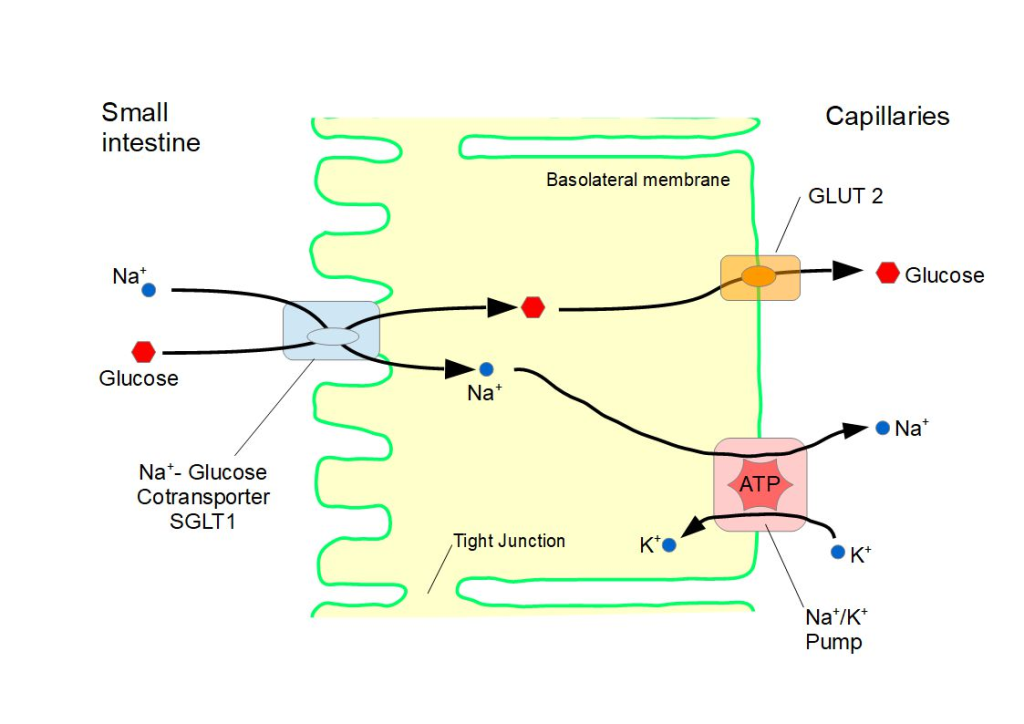
Forskjellige transportører for ulike behov
Glukose kan altså både transporteres passivt – via bærerproteiner som GLUT2 – og aktivt, gjennom sekundær aktiv transport.
Det er ikke tilfeldig. Når glukosekonsentrasjonen er høy, som etter et måltid, er passiv diffusjon gjennom GLUT2 mer enn nok. Men når tarmen er tom og glukose er lavt, trenger kroppen fortsatt å hente det lille som finnes. Da trer den Na⁺-drevne glukosekotransporten inn og sørger for effektivt opptak.
Dette illustrerer hvorfor cellen trenger flere typer transportører for samme stoff – de dekker ulike behov under ulike fysiologiske forhold. Den aktive transporten gir cellen kontroll. Den gjør det mulig å bygge opp og bevare asymmetrier som danner grunnlaget for elektriske signaler, osmotisk balanse og energilagring. Det er motstanden mot likevekt som holder cellen levende.
Ionekanaler og nervesignaler
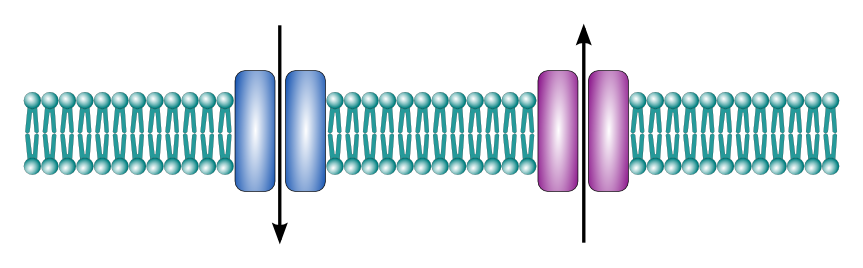
Celler er ikke bare små kjemiske fabrikker – de er også elektriske enheter. Dette gjelder spesielt for nerveceller og muskelceller, som må kunne sende raske signaler over lange avstander. Denne elektriske aktiviteten er mulig takket være ionekanaler – spesialiserte membranproteiner som tillater hurtig og selektiv passasje av ioner som natrium, kalium og kalsium. Ionekanalene er avgjørende for å generere og formidle elektriske signaler, og reguleres strengt av både elektriske og kjemiske stimuli.
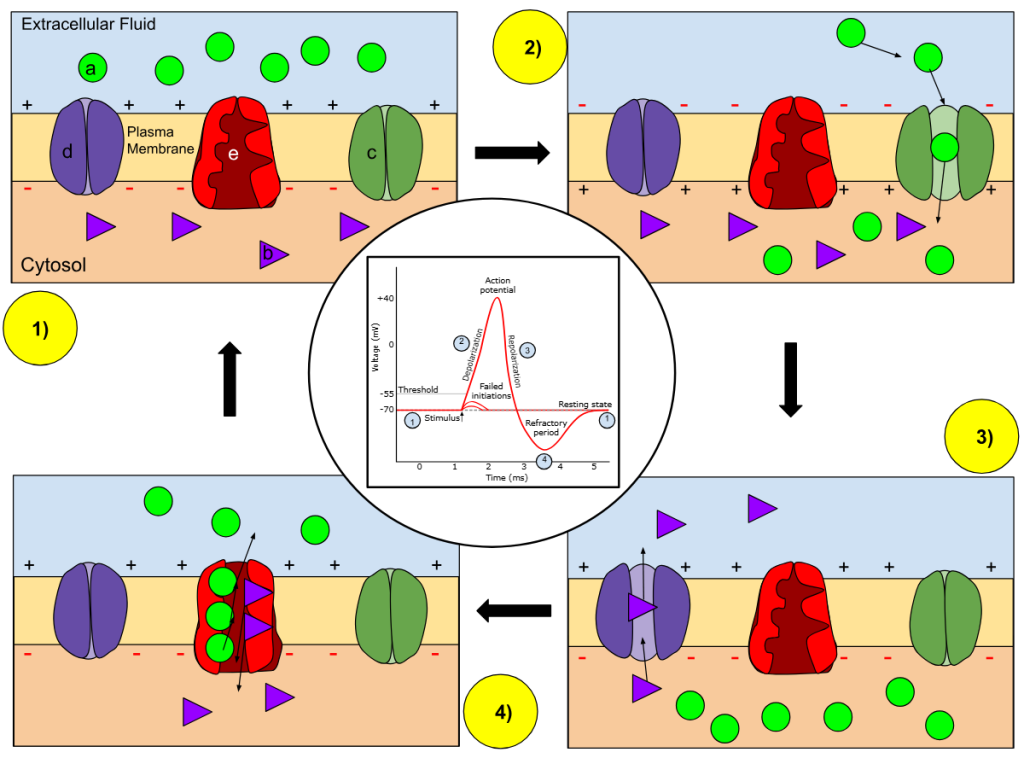
Spenningsstyrte ionekanaler og aksjonspotensial
Når en celle er i hvile, opprettholdes en elektrisk spenning over membranen – det såkalte hvilepotensialet – som vanligvis ligger på rundt -60 mV.
Denne negative ladningen skyldes hovedsakelig at K⁺-ioner lekker ut gjennom K⁺-lekkasjekanaler, mens Na⁺-ioner holdes ute av Na⁺/K⁺-pumpen.
Når en nervecelle stimuleres, skjer en rask endring i membranens spenning: spenningsstyrte natriumkanaler åpnes, og Na⁺ strømmer inn i cellen.
Innsiden blir mer positiv, og dette kalles depolarisering. Membranpotensialet kan stige helt til +40 mV i løpet av millisekunder.
Etter denne raske endringen lukkes natriumkanalene og går inn i en inaktivert tilstand.
Samtidig åpnes spenningsstyrte kaliumkanaler, og K⁺ strømmer ut av cellen. Dette bringer membranpotensialet tilbake mot det negative hvilenivået i en prosess kalt repolarisering. Dermed er cellen klar til å sende et nytt signal, men det krever at ionefordelingen først gjenopprettes, noe som igjen skjer takket være Na⁺/K⁺-pumpen.
Signalet sprer seg langs aksonet som en bølge av depolarisering etterfulgt av repolarisering, styrt av åpning og lukking av spenningsstyrte ionekanaler. Denne formen for elektrisk signaloverføring er selve fundamentet for hvordan hjernen, nervesystemet og muskulaturen kommuniserer.
Fra elektrisk til kjemisk signal – kalsium og synapser
Når aksjonspotensialet når enden av et nevron, altså nerveenden, må signalet overføres til neste celle. Her endres signaltypen: fra elektrisk til kjemisk. Spenningsstyrte kalsiumkanaler åpnes, og Ca²⁺ strømmer inn i nerveenden.
Den økte kalsiumkonsentrasjonen stimulerer synaptiske vesikler – små blærer fylt med signalstoffer, nevrotransmittere – til å smelte sammen med membranen og frigjøre innholdet sitt ut i synapsespalten.
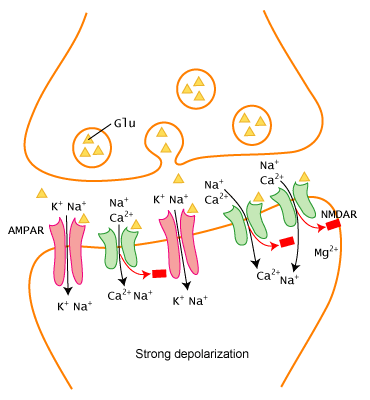
Disse nevrotransmitterne binder seg så til reseptorer på mottakercellen. Mange av disse reseptorene er ligandstyrte ionekanaler. Når en nevrotransmitter binder seg, åpnes kanalen, og ioner strømmer inn i målcellen. Dersom tilstrekkelig mange ionekanaler åpnes, kan det føre til at målcellen selv depolariseres og sender sitt eget aksjonspotensial videre. Slik føres informasjonen fra celle til celle – først som et elektrisk signal, så som et kjemisk signal, og deretter elektrisk igjen.
Les mer om dette her: Membranpotensial og aksjonspotensial
Ulike typer ionekanaler
Ionekanaler finnes i flere varianter, med ulike kontrollmekanismer:
Spenningsstyrte ionekanaler åpnes og lukkes som respons på endringer i membranpotensialet. Disse finnes særlig i nerve- og muskelceller og er ansvarlige for aksjonspotensialet.
Ligandstyrte kanaler aktiveres når bestemte molekyler – ligander – binder seg til dem. Ligandene kan være nevrotransmittere som glutamat eller acetylkolin, som binder seg fra utsiden, eller sekundære budbringere som virker fra innsiden.
Mekanisk aktiverte kanaler åpnes som følge av fysisk deformasjon av cellemembranen, for eksempel ved strekk eller trykk. Slike kanaler finnes blant annet i hårcellene i det indre øret, hvor lydbølger åpner kanalene og starter det elektriske signalet som tolkes som lyd i hjernen.
Aquaporiner, som jeg så vidt nevnte i sta, utgjør en egen klasse av vannkanaler.
De slipper selektivt vannmolekyler gjennom, men hindrer ioner og andre stoffer. Dette gjør det mulig å raskt regulere vannbalanse og osmotisk trykk i både enkeltceller og hele vev.
Ionekanaler og effektivitet
I motsetning til bærerproteiner, som endrer form for hvert molekyl de frakter, kan ionekanaler forbli åpne og tillate tusenvis av ioner å strømme gjennom hvert sekund. Dette gjør dem ideelle for raske prosesser som signaloverføring. Selv om de fleste kanaler er «gated», altså de krever en form for aktivering for å åpnes, trenger de ikke endre form for hvert enkelt ion. Det gjør dem langt mer effektive enn mange andre transportmekanismer.
Det er denne effektiviteten og selektiviteten som gjør ionekanaler til noen av de viktigste komponentene i det levende nervesystemet.
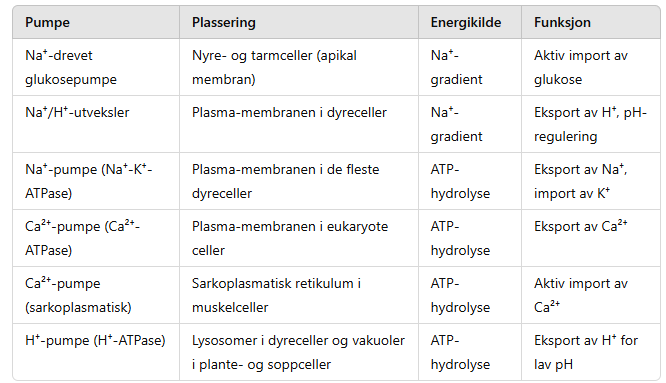
Viktige transmembranpumper:
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3
❓ Test deg selv
Obs, tomt! Kommer etterhvert <3