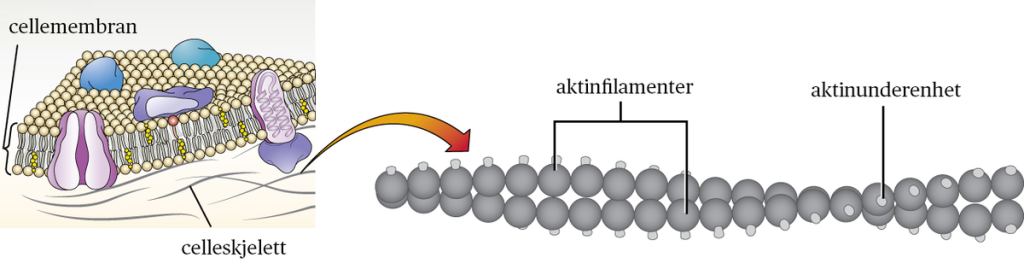
Cytoskjelettet er et nettverk av ulike fibre som gir cellen form, styrke, bevegelse og fungerer som transportsystem. Det består av tre hovedtyper fibre: intermediære filamenter, mikrotubuli, og aktinfilamenter.
Intermediære filamenter
Bygd opp av ulike typer fibrøse proteiner, for eksempel keratin. Intermediære filamenter har navnet sitt intermediær fordi de er tykkere enn aktin og tynnere enn myosinfilamenter. Det er de sterkeste filamentene vi har i cellen, og de overlever det meste. Det forklarer hvorfor negler og hår feks. ikke bryter så lett ned, selv om mennesket ikke lenger lever.
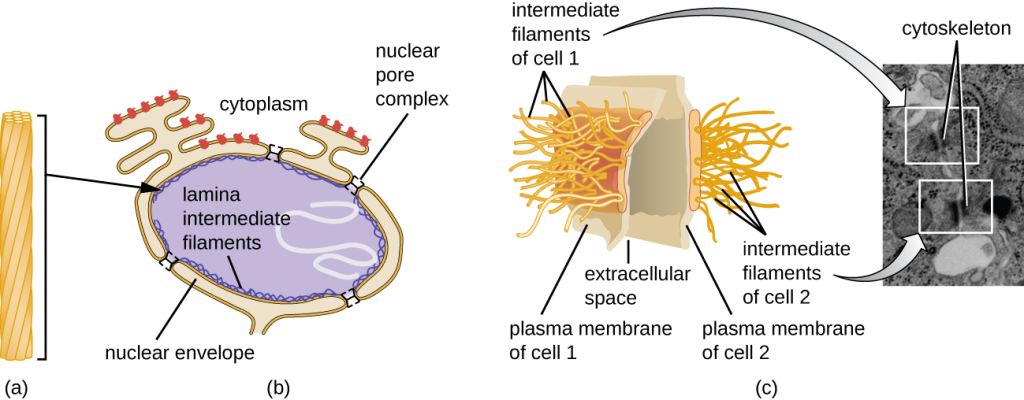
Intermediære filamenter finnes som et nettverk i cytoplasma, rundt hele kjernen og ut til membranen. Det finnes også på innsiden av kjernen! Dette heter Nukleær lamina: Dette er et nettverk av intermediære filamenter som ligger på innsiden av kjernemembranen. Det gir støtte og struktur til cellekjernen. Laminer, en spesiell type intermediære filamenter, danner denne typen lamina.
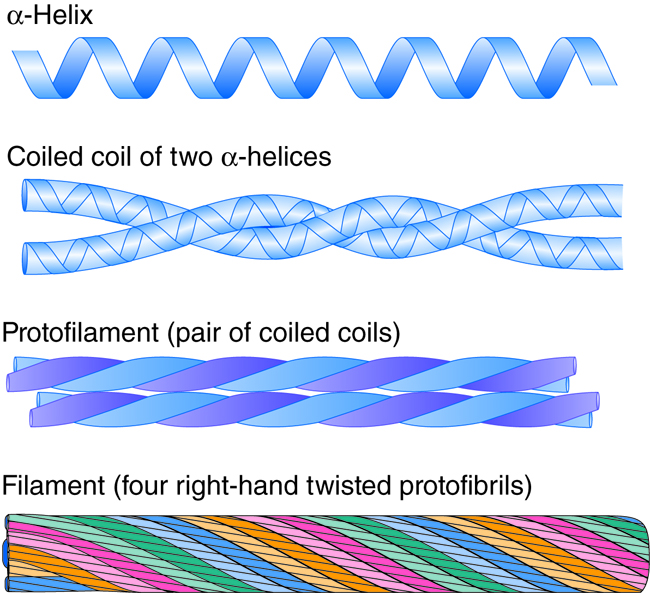
- Oppbygning: Intermediære filamenter er bygd opp nesten som tau, som er tvistet rundt hverandre. Det gir de mye styrke. Alfa-heliks dimerer danner tetramere som går i grupper på åtte. Denne strukturen er fleksibel og sterk.
- Så det er tydelig: Gir celler og vev mekanisk styrke. Støtter kjernemembranen og beskytter celler mot mekanisk stress, spesielt i hud- og muskelceller.
- De har en N terminal og en C terminal, men de har ingen polar side, noe som skiller intermediære filamenter fra de to andre typene.

De fire hovedklassene av intermediære filamenter
Selv om strukturen er felles, finnes det ulike typer intermediære filamenter som er tilpasset spesifikke celletyper og funksjoner. De kan deles inn i fire hovedklasser:
1. Keratinfilamenter – kroppens mest utbredte
Keratin er den vanligste typen intermediære filament og finnes i alle epitelceller, fra hud til slimhinner. Det er også hovedkomponenten i hår, negler, horn, fjær og lignende strukturer hos dyr. I huden danner keratin et sterkt nettverk som forankres i desmosomer – celle-celle-kontakter som binder epitelceller sammen. Dette gjør at mekanisk stress fordeles jevnt gjennom cellelaget, noe som beskytter huden mot sprekker og skader.
Keratinfilamentene strekker seg fra den ene siden av cellen til den andre, og fungerer som fleksible, men seige kabler. Dette gir huden både elastisitet og styrke.
Et tydelig eksempel på hvor viktig keratin er, ser man i den genetiske hudsykdommen Epidermolysis bullosa simplex. Her fører mutasjoner i keratin-genene til at filamentene ikke dannes som de skal. Resultatet er at huden mister sin strukturelle støtte – bare mildt trykk kan føre til blemmer, hudavskalling og sår.
2. Vimentin og vimentinrelaterte filamenter
Disse filamentene finnes hovedsakelig i bindevev, muskelceller og gliaceller (støtteceller i nervesystemet). Vimentin gir cellene form og forankrer organeller som kjerne og mitokondrier, og spiller en viktig rolle i å opprettholde celleintegritet under stress og bevegelse. De vimentinrelaterte filamentene omfatter blant annet desmin i muskelceller og GFAP i astrocytter.
3. Nevrofilamenter
Disse finnes i nerveceller, hvor de danner tette bunter langs aksonene – de lange utløperne som leder elektriske signaler. Nevrofilamenter bestemmer i stor grad tykkelsen på aksonet og dermed også ledningshastigheten. De gir styrke og stabilitet til nevronet, og er avgjørende for normal nervefunksjon.
4. Nukleær lamina
Rett innenfor kjernemembranen danner spesialiserte intermediære filamenter kalt laminer et tett nettverk som stabiliserer cellekjernens form. I tillegg deltar lamina i viktige prosesser som DNA-replikasjon og celledeling. Mutasjoner i laminer kan gi alvorlige genetiske sykdommer, inkludert visse former for muskeldystrofi og progeria (en sjelden, tidlig aldringssykdom).
Keratin – kroppens fleksible forsterkning
Blant alle de intermediære filamentene er det én type som utmerker seg i utbredelse og betydning: keratin.
Keratinfilamenter finnes i alle epitelceller, og er særlig rikelig i hud, hår og negler. Hos dyr finner man det også i fjær, horn og klør.
Det er dette filamentet som gir huden dens fleksibilitet, styrke og evne til å motstå ytre påkjenninger.
Keratinfilamentene dannes inne i epitelceller og forankres i desmosomer, som er spesialiserte cellekontakter mellom naboceller.
Disse desmosomene fungerer som knutepunkter der keratinfilamentene fra én celle kobles sammen med filamentene i nabocellen. På denne måten dannes det et sammenhengende, fleksibelt nettverk som binder cellene til hverandre og fordeler mekanisk stress.
Når huden strekkes eller utsettes for trykk, er det dette keratinnettverket som sørger for at belastningen fordeles jevnt utover, i stedet for at en enkelt celle ryker.
Man kan tenke på det som en vev av sterke kabler som holder hudlaget intakt.
Et sårbart bevis: Epidermolysis bullosa simplex
At keratin er viktig, blir tydelig i sykdommen Epidermolysis bullosa simplex.
Dette er en genetisk tilstand der mutasjoner i keratin-genene fører til at filamentene ikke dannes riktig.
Uten det støttende nettverket som vanligvis beskytter huden, blir cellelaget sårbart for selv de minste belastninger.
Hos pasienter med denne sykdommen kan et lett trykk, et gnikk fra klær eller en svak støt føre til at hudlagene løsner fra hverandre. Resultatet er blemmer, sår og hudavskalling – ofte fra helt hverdagslige bevegelser. Denne tilstanden er et kraftig eksempel på hvor livsnødvendig keratin er for å opprettholde hudens mekaniske stabilitet.
Mikrotubuli
Mikrotubuli er lange, hule rør laget av protein, og utgjør en av de tre hovedtypene i cytoskjelettet. Der aktinfilamenter gir form og bevegelse, og intermediære filamenter gir styrke, er mikrotubuli spesialister på struktur, organisering og transport. De danner et dynamisk nettverk inne i cellen som fungerer både som reisverk og motorvei for intracellulær transport – og de spiller avgjørende roller i blant annet celledeling og dannelse av cilier og flageller.
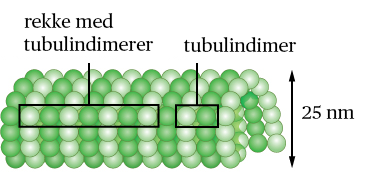
Struktur: Tubulindimer og protofilamenter
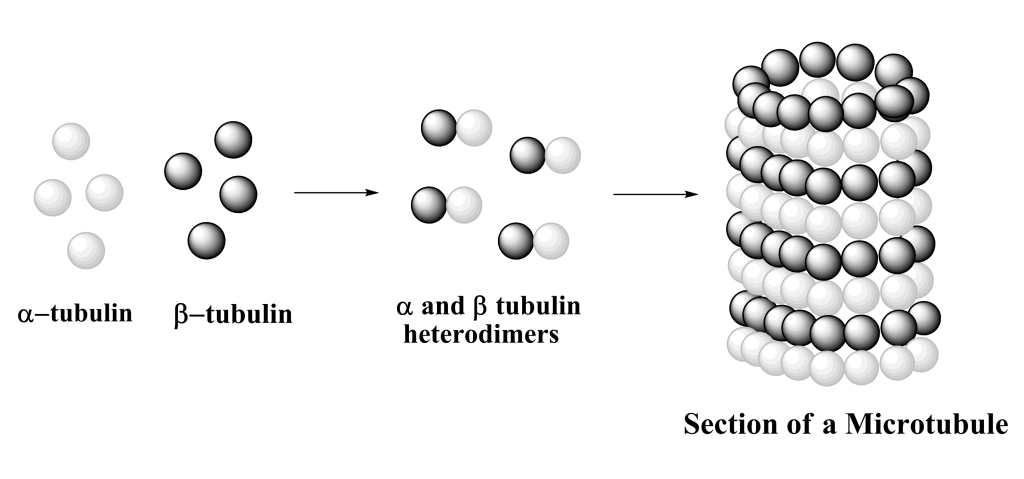
Mikrotubuli bygges opp av små protein-enheter kalt tubulindimerer, som består av to nært beslektede proteiner: alfa-tubulin og beta-tubulin. Disse er bundet sammen ved ikke-kovalente bindinger og oppfører seg som én funksjonell enhet.
Dimerene legger seg ende mot ende for å danne lange, lineære kjeder kalt protofilamenter. Tretten slike protofilamenter legger seg parallelt i en sirkel og danner en hul, rørformet struktur med en lumen i midten – det vi kjenner som en mikrotubulus.
Hver protofilament har en innebygd polaritet, fordi alfa-tubulin alltid vender mot én ende og beta-tubulin mot den andre. Dette gir mikrotubulus en minus-ende (alfa-tubulin) og en pluss-ende (beta-tubulin), og det er i pluss-enden at vekst og forlengelse primært skjer.
Vekst og utspring: Sentrosomet som kommandosentral
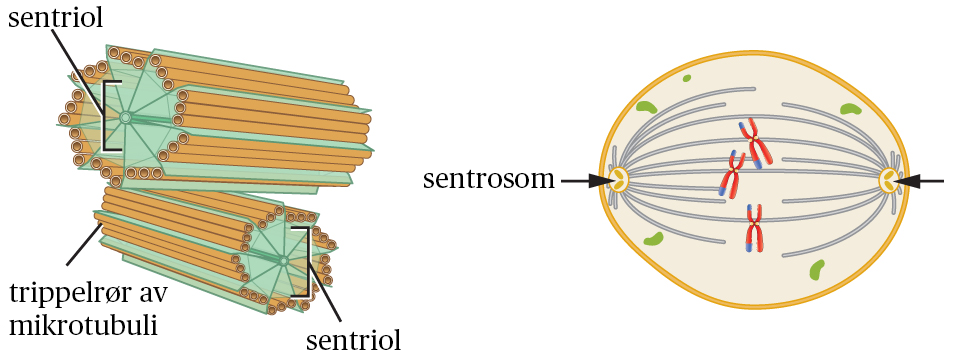
De fleste mikrotubuli i cellen vokser ut fra en sentral struktur nær cellekjernen kalt sentrosomet – også kjent som et mikrotubuli-organiserende senter (MTOC). Dette er startpunktet for mikrotubulivekst.
Sentrosomet består av:
- To perpendikulært orienterte sentrioler
- En omkringliggende, amorf matrix av proteiner
- Gamma-tubulinringer, som finnes i hundretall og fungerer som nukleasjonssteder hvor nye mikrotubuli begynner å vokse
I sentrosomet er mikrotubuli forankret med sin minus-ende, mens pluss-enden vokser ut i cytoplasmaet der den kan nå frem til cellemembranen, organeller og andre strukturer.
Dynamisk ustabilitet – mikrotubulienes fleksible natur
En av mikrotubuliens mest bemerkelsesverdige egenskaper er det som kalles dynamisk ustabilitet.
Dette betyr at de kan bygge seg opp og brytes ned raskt, nærmest som et stillas som tilpasses etter behov.
I praksis skjer dette ved at tubulindimerer legges til i pluss-enden (polymerisering), eller fjernes igjen (depolymerisering).
Denne fleksibiliteten er essensiell for at mikrotubuli skal kunne reorganiseres raskt, som under celledeling, der de må bygge den mitotiske spindelen på få minutter. Samtidig kan mikrotubuli stabiliseres ved at de festes til strukturer i cellen – som cellemembran, organeller eller spesialiserte proteiner. En stabil mikrotubulus vil da ikke lenger depolymerisere spontant.
Dynamisk ustabilitet – regulert av GTP-hydrolyse
Den dynamiske ustabiliteten til mikrotubuli styres av en nøye balansert kjemisk prosess: hydrolysen av GTP bundet til beta-tubulin.
Dette er en energisk favorisert reaksjon, der GTP (guanosin-trifosfat) brytes ned til GDP (guanosin-difosfat) og fosfat – på samme måte som hydrolyse av ATP frigjør energi i andre biologiske prosesser.
Hver frie tubulindimer bærer med seg en GTP bundet til beta-tubulin.
Når dimeren inkorporeres i den voksende enden av mikrotubulien, hydrolyseres GTP relativt raskt til GDP.
Men det finnes et viktig unntak: hvis polymeriseringen skjer raskt nok, rekker ikke hydrolysen å følge med.
Resultatet blir at enden av mikrotubulien består av en klynge med GTP-bundet tubulin – kjent som en GTP-cap.
Denne GTP-capen stabiliserer mikrotubulien, fordi GTP-bundet tubulin danner sterkere bindinger enn GDP-bundet tubulin.
Så lenge capen er til stede, fortsetter mikrotubulien å vokse.
Men denne balansen er skjør.
Hvis GTP hydrolyseres raskere enn nye dimerer legges til, vil GTP-capen forsvinne. Uten den stabiliserende effekten fra capen blir enden av mikrotubulien ustabil, og hele strukturen kan raske trekkes tilbake og forkortes. Dette kalles en katastrofe, og markerer starten på depolymerisering. Mikrotubulien kan senere gjenoppbygge seg selv i en prosess kalt redning.
Denne evnen til å bygge seg opp og bryte seg ned igjen på sekunder gjør mikrotubuli spesielt nyttige i dynamiske prosesser som celledeling – men også i spesialiserte celler der mikrotubuli må stabiliseres for å utføre mer varige oppgaver.
Stabilisering og transport langs mikrotubuli
Selv om mikrotubuli ofte oppfører seg dynamisk, finnes det også situasjoner der de stabiliseres, særlig i celler med langvarig strukturbehov – som nevroner.
Her er mikrotubuli ikke i konstant vekst og kollaps, men danner stabile “skinner” som strekker seg gjennom hele aksonet, fra cellekroppen til endeterminalen.
Disse mikrotubuliene fungerer som transportbaner for cellens gods: organeller, vesikler og makromolekyler som skal fraktes fra én del av cellen til en annen. Men mikrotubuli gjør ikke dette arbeidet alene – de samarbeider med spesialiserte motorproteiner.
Motorproteiner – cellens transportsystem
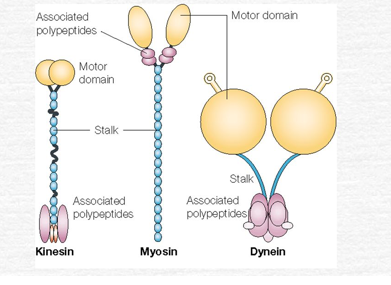
To hovedtyper av motorproteiner utfører denne transporten:
- Kinesin: beveger seg mot pluss-enden av mikrotubuli, altså utover fra cellekroppen mot enden av aksonet. Den frakter bl.a. synaptiske vesikler, enzymer og andre strukturer som skal til nerveenden.
- Dynein: beveger seg mot minus-enden, altså innover mot cellekroppen. Den returnerer avfall, resirkulerte membraner og signalmolekyler.
Man kan se for seg mikrotubuli som jernbaneskinner, og kinesin og dynein som små tog – hver med sin spesifikke retning og last.
Denne organiseringen er avgjørende for blant annet nevroners funksjon, hvor raske og presise transportmekanismer over lange avstander er helt essensielt for kommunikasjon mellom nerveceller.
Cilia og flageller
Langs overflaten av mange celler finner vi fine, hårliknende strukturer kalt cilier og flageller.
Disse utløperne spiller helt avgjørende roller i både cellebevegelse, væsketransport og signalering – og de er bygget opp av mikrotubuli.
Selv om cilia og flageller deler mye av sin indre struktur, har de ulike funksjoner i kroppen.
Der mikrotubuli inne i cellen er dynamiske og kan bygges opp og brytes ned raskt, er mikrotubuli i cilier og flageller stabilisert av spesialiserte proteiner.
Dette gir strukturen fasthet og gjør at bevegelsen blir presis og koordinert.
Cilier
Cilia er korte, hårliknende utløpere som stikker ut fra celleoverflaten. De finnes ofte i stort antall på én og samme celle, og beveger seg i en koordinert, rytmisk bølgebevegelse. Dette gjør dem ideelle for å flytte væske, slim eller celler over celleoverflaten.
Eksempler på cilia-funksjon i kroppen:
- Luftveiene: I luftrøret og bronkiene dekker cilier overflaten av epitelcellene. Sammen med slim fra begerceller danner de en viktig del av kroppens forsvar. Ciliene slår rytmisk og fører slimet – og med det partikler, mikrober og støv – oppover mot svelget, hvor det svelges eller hostes ut.
- Reproduksjonssystemet hos kvinner: I egglederne hjelper ciliene med å transportere egget fra eggstokken mot livmoren etter eggløsning. Uten fungerende cilier vil egget ikke bevege seg fremover i normal hastighet.
- Embryonal utvikling: I de tidligste stadiene av fosterutviklingen spiller spesialiserte cilier en nøkkelrolle i å etablere kroppens høyre-venstre-symmetri. Dersom disse ciliene ikke fungerer riktig, kan det føre til speilvendt organplassering, kjent som situs inversus.
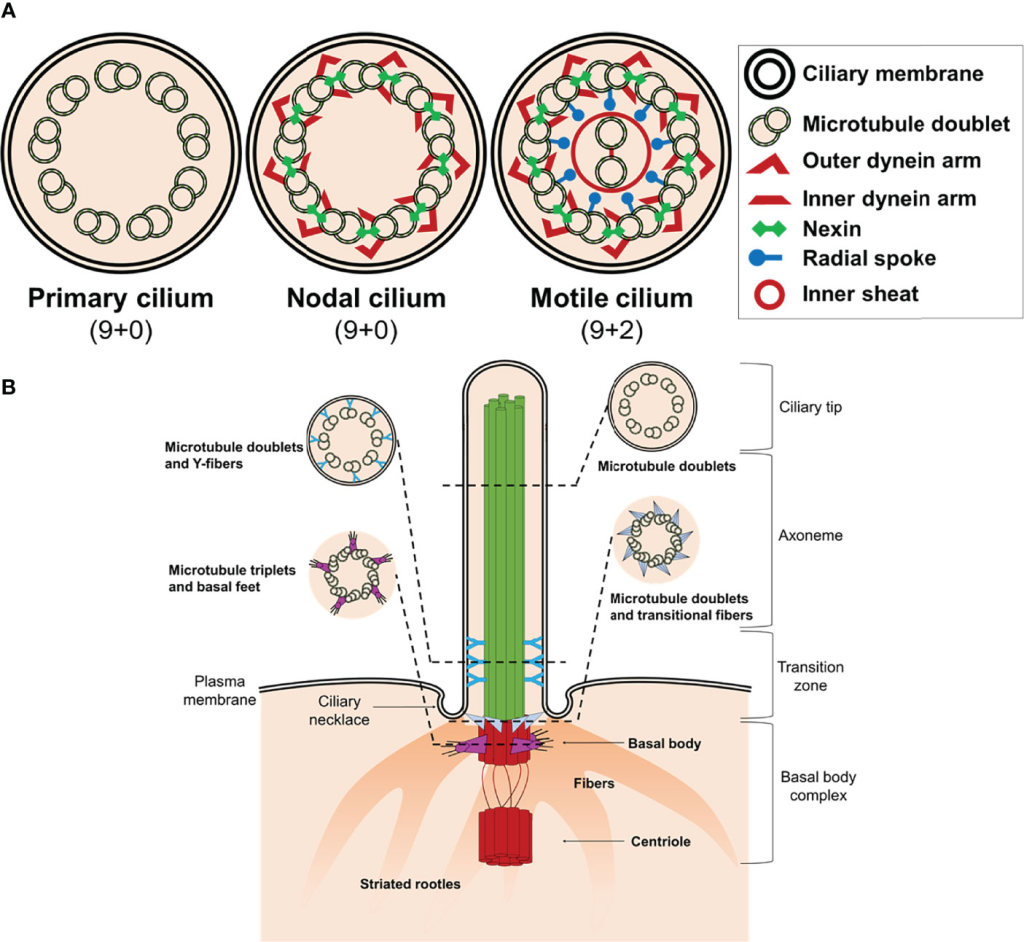
Den ikoniske 9+2-strukturen
Strukturen til cilier og flageller følger et karakteristisk mønster kalt «9+2-strukturen». Dette refererer til antallet mikrotubuli inne i selve utløperen:
- 9 ytre par av mikrotubuli ligger organisert i en sirkel
- 2 sentrale mikrotubuli ligger i midten
Rundt mikrotubuli finner vi en rekke tilleggsproteiner, blant annet dyneinarmer, som er store motorproteiner.
Dynein bruker ATP som energikilde og beveger seg langs mikrotubuli mot minus-enden.
I isolerte mikrotubuli (eksperimentelt) kan dette føre til glidning mellom mikrotubuli. Men i cilier og flageller er de ulike mikrotubuliene koblet sammen av koblingsproteiner, som gjør at dyneins bevegelse i stedet skaper bøyning.
Det er denne bølgende bevegelsen som driver cilien eller flagellen frem og tilbake.
Sykdommer relatert til ciliefunksjon
En av de mest kjente sykdommene relatert til defekte cilier er Primær ciliær dyskinesi (PCD), tidligere kjent som Kartageners syndrom.
Denne arvelige tilstanden fører til at ciliene ikke klarer å bevege seg riktig.
Resultatet er dårlig slimmobilisering i luftveiene, med gjentatte luftveisinfeksjoner, kronisk hoste og bihulebetennelser.
Flageller – bevegelse fremover
Flageller er strukturelt svært like cilier, men de er som regel lengre, og hver celle har som oftest kun én flagell.
Flageller finnes særlig i encellede organismer og i sædceller hos mennesker, hvor de gir cellen evne til å svømme.
Bevegelsen til flagellen er bølgeliknende, med repeterende bøyninger som drives av dynein. Dette skaper fremdrift og lar cellen bevege seg i væske – noe som er avgjørende for blant annet fertilitet.
I tillegg til bevegelse, kan enkelte flageller og cilier også ha sensoriske roller, der de deltar i signaloverføring og oppfattelse av miljøstimuli – en funksjon som fremdeles utforskes.
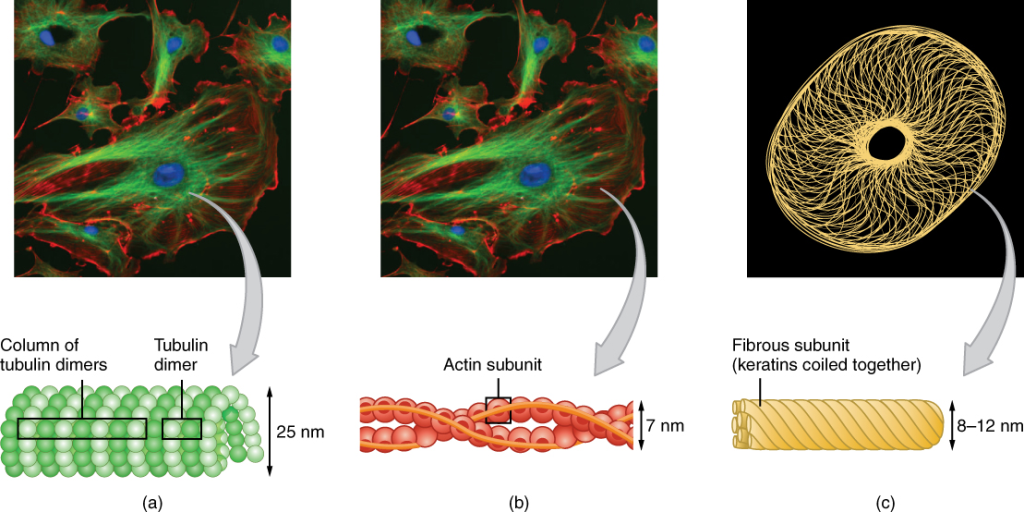
Aktinfilamenter
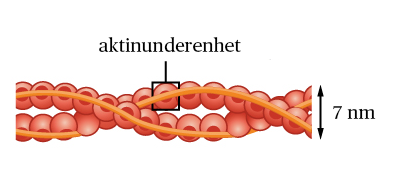
Aktinfilamenter er de tynneste, men kanskje mest dynamiske og allsidige komponentene i cytoskjelettet.
De er bygget opp av aktinproteiner og finnes masse av rett under cellemembranen, i et område som kalles cortex.
Her danner de et nettverk som gir cellen form, styrke, evne til å bevege seg – og i mange tilfeller evne til å dele seg, omfavne partikler og svare på omgivelsene.
Uten aktin ville prosesser som fagocytose, celledeling og cellevandring vært umulige.
Struktur og polaritet
Grunnenheten i aktinfilamenter er G-aktin – et globulært, ATP-bindende protein.
Når mange G-aktin-molekyler polymeriseres sammen, danner de lange, tynne tråder kjent som F-aktin (fibrillært aktin).
Disse trådene er fleksible, men samtidig sterke nok til å forme og bevege hele celler.
Aktinfilamenter har polaritet.
Det betyr at de har en pluss-ende og en minus-ende. På pluss-enden legges nye aktinmonomerer raskt til, mens minus-enden er stedet hvor de sakte fjernes. Dette gir filamentene en innebygd retning og gjør at de kan delta i dynamiske prosesser som cellebevegelse.
Polymerisering og treadmilling
Polymerisering av aktin krever energi, og hvert G-aktin-molekyl binder et ATP-molekyl før det legges til et voksende filament.
Etter at det er inkorporert i filamentet, vil ATP hydrolyseres til ADP. Dette endrer aktinmolekylets affinitet og gjør det mer sannsynlig at det løsner fra minus-enden over tid.
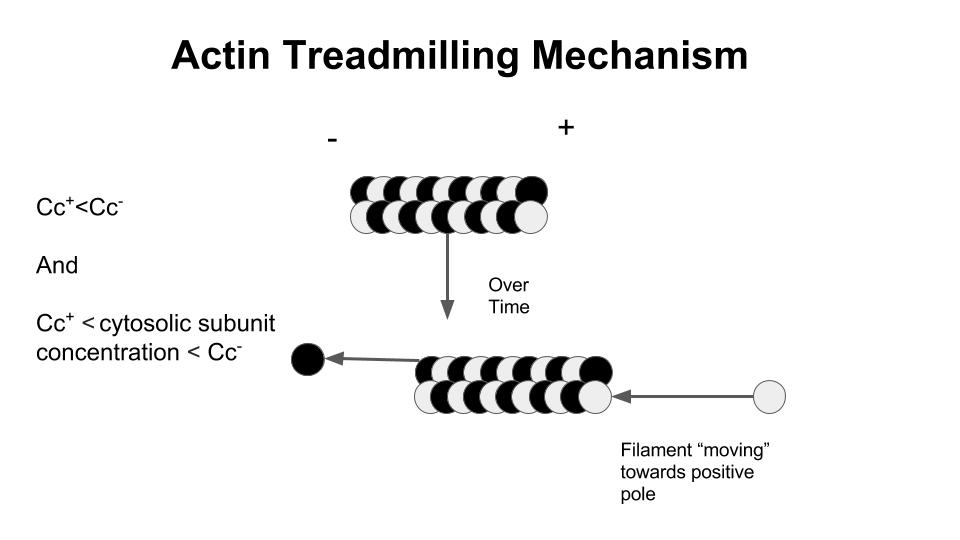
Når tilførselen av nye ATP-bundne G-aktin på pluss-enden balanseres av tapet av ADP-aktin på minus-enden, skjer det en prosess som kalles treadmilling.
Filamentet endrer da ikke lengde, men det «flytter seg» fremover ved at aktinmonomerer kontinuerlig strømmer inn i én ende og ut av den andre.
Dette er en av hovedmekanismene som gjør at aktinfilamenter kan generere bevegelse uten at enkeltmolekyler flytter seg i lengderetning.
Organisering av aktin
Hvordan aktinfilamentene organiseres, avgjør hva de gjør.
Med ulike hjelpemolekyler kan aktin danne stive søyler, fleksible nettverk eller muskel-lignende bunter som trekker seg sammen.
Kontraktile bunter, som for eksempel stressfibre i cellens indre eller den kontraktile ringen under celledeling, organiseres som stramme tauverk.
Disse strukturene kan generere kraft og forandre cellens form ved å trekke sammen filamentene.
Like under cellemembranen finner vi ofte et gel-lignende nettverk av aktin, spesielt i cellens korteks.
Dette nettverket minner om et finmasket nett og gir cellen mekanisk støtte, opprettholder formen og gjør det mulig for cellen å flate ut og «krype» langs underlaget.
I tynne utløpere kalt filopodia, organiseres aktinfilamentene i parallelle bunter.
Alle filamentene peker i samme retning, med pluss-endene ut mot tuppen. Denne strukturen gjør filopodiene til ideelle sensorer som lar cellen utforske omgivelsene – nesten som fingre i mikroskala.
Cellebevegelse – hvordan cellen kryper
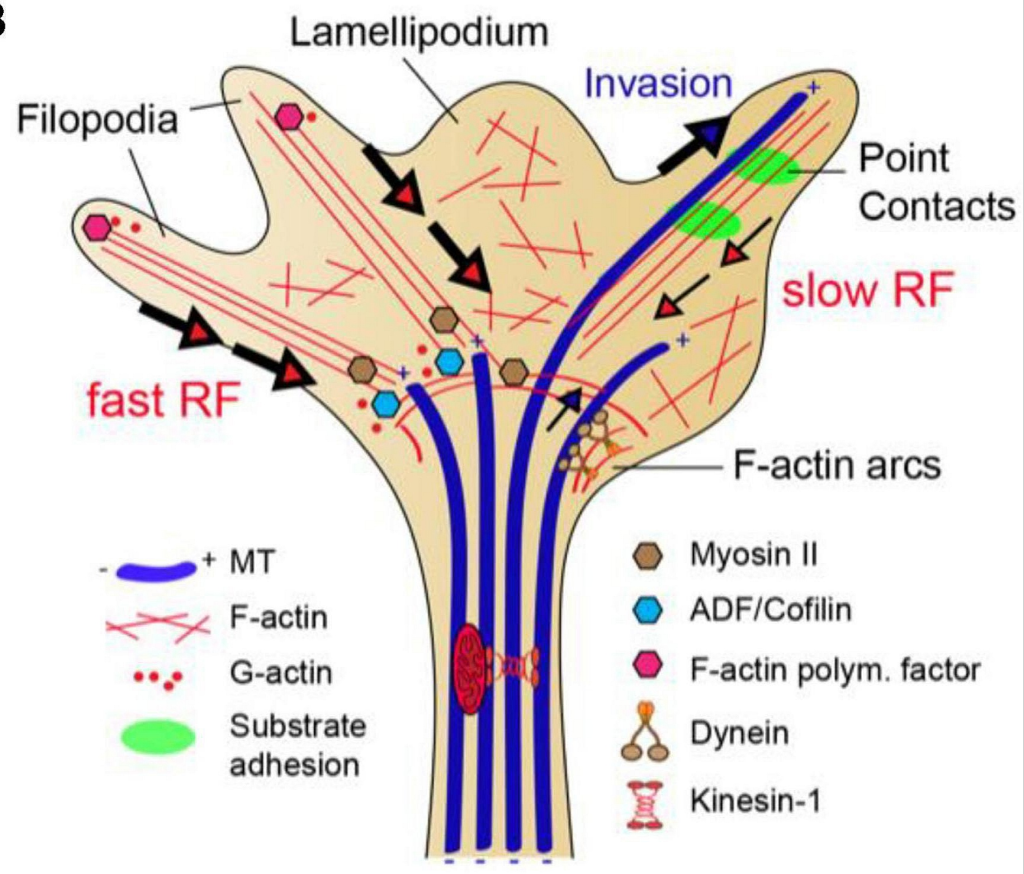
Aktinfilamentene driver cellemigrasjon gjennom et samarbeid mellom polymerisering foran og kontraksjon bak.
Først vokser filamentene raskt ved cellefronten.
Dette skyver plasmamembranen utover og danner flate utløpere som kalles lamellipodia – brede og vifteformede strukturer som legger seg som en bølge foran cellen.
Smalere og mer spesialiserte utløpere, filopodia, strekker seg ut for å sanse veien videre.
Samtidig som aktin dytter cellen fremover, trekker myosinfilamenter cytoskjelettet bakover.
Myosin fungerer som motor – og det er særlig myosin II som er viktig her.
Denne typen myosin kan binde til to aktinfilamenter og dra dem mot hverandre. Resultatet er en sammentrekning, som drar cellens bakpart fremover og lar hele cellen gli videre.
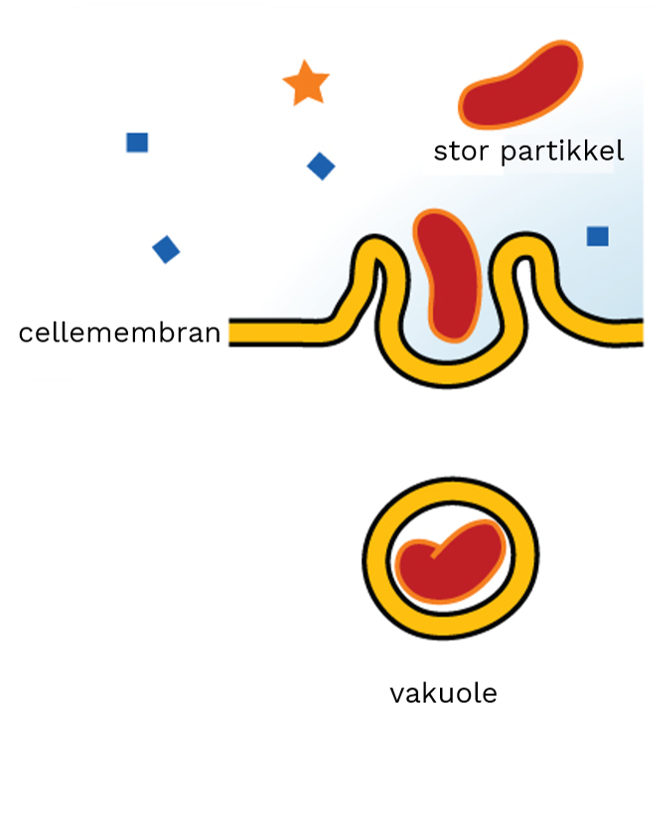
Fagocytose – når cellen griper og spiser
Ved fagocytose bruker cellen aktinfilamenter til å omslutte og «spise» partikler som bakterier eller cellefragmenter.
Plasmamembranen danner utløpere kalt pseudopodier, drevet frem av lokal aktinpolymerisering.
Denne prosessen styres av signalstoffer, som fosfoinositider, og gir cellen evnen til å raskt omslutte målet sitt.
Når partikkelen er fanget, lukkes membranen rundt og danner en fagosom, som senere kan fusjonere med lysosomer og bryte ned innholdet.
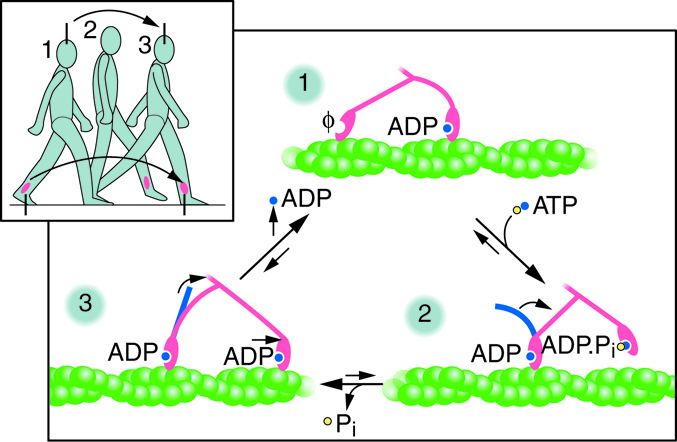
Aktin og myosin
Bevegelse og kraft i cellen er ikke aktins verk alene.
Det er samarbeidet mellom aktin og motorproteiner – særlig myosin I og myosin II – som gjør det mulig å utføre arbeid.
Myosin I har én motorenhet og en fleksibel hale.
Det beveger seg mot pluss-enden av aktin og kan frakte små vesikler eller skyve på cellemembranen.
Det fungerer som en liten tralle langs aktinfilamentet, og spiller en særlig viktig rolle i cellens kortikale områder.
Myosin II har to motorhoder og en coiled-coil hale.
Det kan danne bipolare filamenter, der motorhodene i hver ende drar i aktinfilamenter i motsatt retning.
Dette er mekanismen bak muskelkontraksjon, men også viktig i ikke-muskelceller, der det brukes i celledeling og bevegelse.
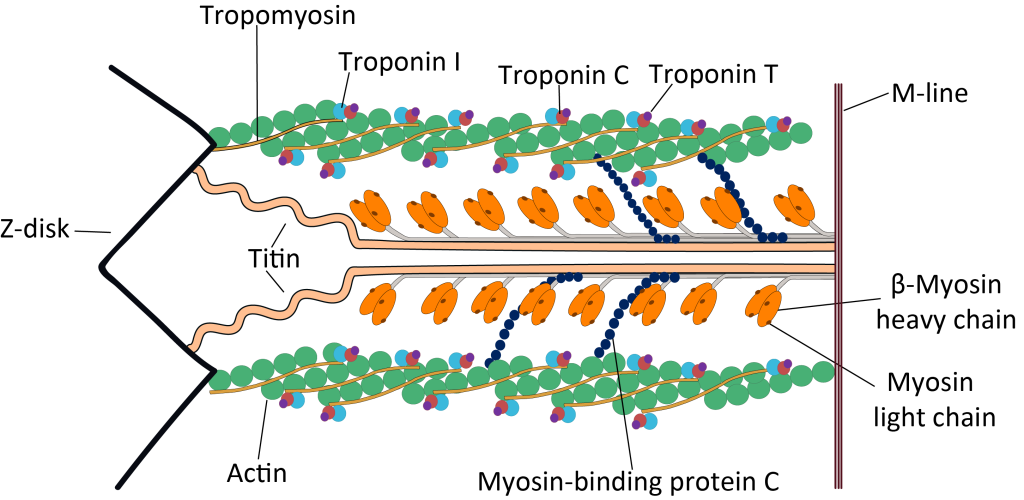
I muskelceller organiseres aktin og myosin i gjentatte enheter kalt sarcomerer, der myosin-glidning over aktin skaper kraft og forkorter muskelen.
Dette er en ekstremt presis og ATP-avhengig prosess, som muliggjør alt fra hjertebank til fingerbevegelser.
📚 Anki-kort
Her var det tomt! Kommer snart
📝 Eksamensoppgaver
Her var det tomt! Kommer snart
👨⚕️ Klinisk case
Her var det tomt! Kommer snart
❓ Test deg selv
Her var det tomt! Kommer snart