Fra glykolyse til mitokondrie
Før vi kaster oss over Krebs-syklusen, er det nyttig med en liten repetisjon av det som kom før. Glykolysen var kroppens første skritt i nedbrytningen av glukose – en prosess som skjer i cytosol og ikke krever oksygen. Vi kaller det en anaerob prosess.
Gjennom ti enzymkatalyserte reaksjoner blir ett molekyl glukose (som har seks karbonatomer) brutt ned til to molekyler pyruvat (som hver har tre karbonatomer). På veien produserer cellen 2 ATP og 2 NADH, etter at det først har blitt investert litt energi i form av ATP. Det viktige å huske, er at glykolysen både gir litt energi direkte og bygger opp energibærere som NADH, som senere skal brukes i mitokondriene for mer effektiv energiproduksjon.
Men pyruvatet vi står igjen med etter glykolysen, kan ikke uten videre gå inn i mitokondriet. For å komme dit, må det først omdannes.
Fra pyruvat til acetyl-CoA
For at pyruvat skal kunne gå videre inn i mitokondriet og inn i Krebs-syklusen, må det først konverteres til et nytt molekyl: acetyl-CoA.
Denne omdannelsen skjer i mitokondriets matrix, og er en slags «portvaktprosess» hvor cellen vurderer om pyruvat skal brukes videre i energiproduksjon eller lagres på andre måter.
Under denne reaksjonen skjer det flere ting samtidig:
- Én karbonforbindelse fra pyruvat fjernes som CO₂ (vi går fra et 3-karbon til et 2-karbon molekyl).
- Det gjenværende tokarbonfragmentet kobles til et koenzym A, som fungerer som en transportør og gjør molekylet reaktivt – klart for videre bruk i Krebs-syklusen.
- Samtidig reduseres NAD⁺ til NADH + H⁺, og dette NADH skal etter hvert brukes i elektrontransportkjeden for å produsere ATP.
Dette trinnet – overgangen fra pyruvat til acetyl-CoA – er aerob, det vil si at det krever oksygen indirekte, ettersom NADH må kunne oksideres videre i elektrontransportkjeden.
Mitokondriet – cellens kraftverk
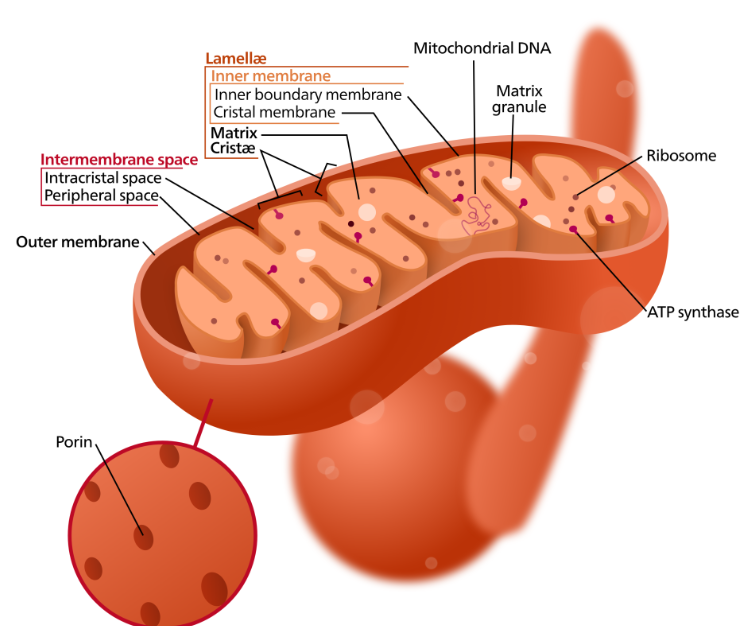
For å forstå hva som nå skjer videre med acetyl-CoA, må vi bli kjent med mitokondriet, der hele hoveddelen av cellens energiproduksjon foregår.
Ytre membran
Dette er mitokondriets yttervegg, som vender ut mot cytosol. Den er beskyttende, men samtidig semipermeabel, og inneholder poriner – små kanalproteiner som tillater transport av små molekyler og ioner. Denne membranen slipper altså gjennom ting som pyruvat og ATP-forløpere.
Intermembranrommet
Mellom den ytre og indre membranen ligger intermembranrommet. Dette er et viktig område fordi det her bygges opp en protongradient – altså en ulik fordeling av H⁺-ioner – som driver selve produksjonen av ATP i det neste steget (elektrontransportkjeden).
Indre membran
Den indre membranen er selektiv og svært lite permeabel – nesten ingenting slipper inn eller ut uten hjelp. Denne membranen er tett pakket med proteiner som inngår i elektrontransportkjeden og ATP-syntase, og den er foldet i mange kriker og kroker for å få størst mulig overflateareal. Disse foldene kalles cristae.
Matrix
Innerst i mitokondriet, innenfor den indre membranen, ligger matrix. Dette er væskeområdet der Krebs-syklusen (TCA-syklusen) skjer. Matrix inneholder også mitokondriets eget DNA (mtDNA), samt ribosomer som kan produsere noen av enzymene mitokondriet trenger selv.
Cristae er de innfoldede strukturene i den indre membranen. De er ikke der for pynt – de har en helt avgjørende funksjon: Ved å øke overflatearealet, får cellen plass til flere proteinkomplekser som utgjør elektrontransportkjeden og ATP-syntase. Mer overflate betyr flere produksjonssteder for ATP. Og mer ATP betyr mer energi til cellen.
Mitokondriets rolle i celleåndingen
Mitokondriet fungerer som cellens kraftverk.
Det er her hoveddelen av energiproduksjonen foregår – gjennom prosesser som effektivt utnytter næringsstoffer til å danne ATP, cellens energivaluta.
Celleåndingen består av flere trinn som henger tett sammen: glykolyse, dannelse av acetyl-CoA, Krebs-syklusen (TCA), elektrontransportkjeden og til slutt oksidativ fosforylering.
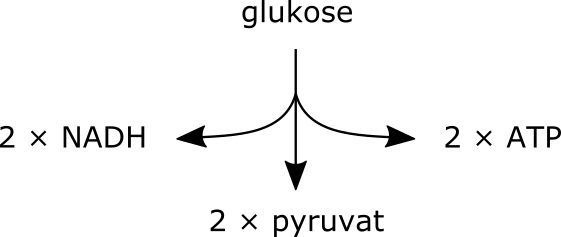
Glykolyse
Selv om glykolysen skjer utenfor mitokondriet, i cytoplasma, danner den grunnlaget for videre energiproduksjon.
Her brytes glukose ned til to molekyler pyruvat.
Prosessen er anaerob – den krever ikke oksygen – men den gir likevel netto gevinst i form av 2 ATP og 2 NADH.
Pyruvat er det sentrale produktet som enten kan brukes videre i mitokondriene eller omdannes til laktat i fravær av oksygen.
Acetyl-CoA
Acetyl-CoA er en sentral metabolitt – et mellomprodukt som forbinder kroppens energiomsetning med biosyntese.
Det fungerer som et koblingspunkt mellom nedbrytning (katabolisme) og oppbygning (anabolisme).
Når kroppen har nok energi, brukes acetyl-CoA som byggestein for syntese av fettsyrer og kolesterol.
Når energibehovet er høyt, går det i stedet inn i Krebs-syklusen for videre energiutvinning.
Hvordan dannes det?
Fra karbohydrater: Pyruvat fra glykolyse konverteres til acetyl-CoA som beskrevet.
Fra fettsyrer: Fettsyrene brytes ned via β-oksidasjon i mitokondriene og gir også acetyl-CoA.
Fra enkelte aminosyrer: Spesifikke aminosyrer kan også omdannes direkte til acetyl-CoA.
Biokjemisk struktur
Acetyl-CoA består av to deler: en acetylgruppe (to karbonatomer) og coenzym A, som fungerer som bærer.
Coenzym A er dannet fra vitamin B5 (pantotensyre), og er en essensiell komponent i energimetabolismen.
Pyruvatdekarboksylering
Etter glykolysen sitter cellen igjen med to molekyler pyruvat for hvert glukosemolekyl.
Men for at cellen skal hente ut enda mer energi, må pyruvat viderebehandles – og det kan den ikke gjøre i cytosol.
Pyruvat må inn i mitokondriet, og der må den gjennom en transformasjon: den må bli til acetyl-CoA.
Denne omdannelsen kalles pyruvatdekarboksylering og representerer overgangen mellom glykolyse og TCA-syklusen.
Pyruvatdekarboksylering skjer inne i mitokondriets matrix og utføres av et stort og komplekst enzymkompleks: pyruvat-dehydrogenase-komplekset, ofte forkortet til PDH-komplekset.
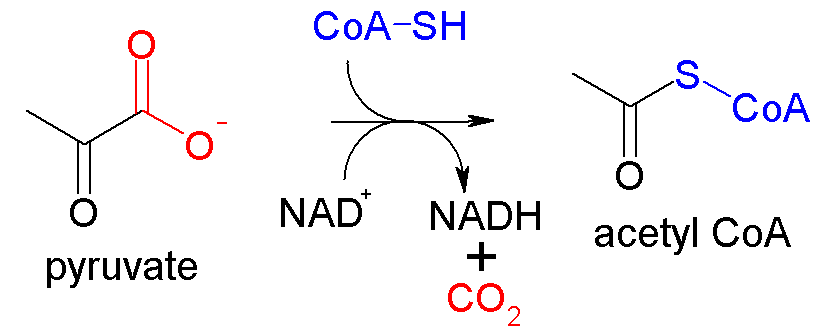
PDH-komplekset består av tre enzymer som samarbeider tett for å utføre denne omdannelsen.
Først starter det med pyruvat-dehydrogenase, som fjerner ett karbonatom fra pyruvat.
Karbonet forsvinner ut som karbondioksid (CO₂).
Det som er igjen, en tokarbonforbindelse, bindes til en kofaktor kalt tiaminpyrofosfat (TPP), og dette gir en mellomform: hydroksyetyl-TPP.
Neste enzym i rekken er dihydrolipoyl transacetylase.
Dette enzymet tar den tokarbon lange acetylgruppen og overfører den til Coenzym A. Resultatet er acetyl-CoA, et sentralt molekyl i cellens energiproduksjon.
I denne prosessen bruker enzymet en arm laget av lipoamid – et slags svingende molekyl som kan holde på acetylgruppen og overføre den dit den skal.
Til slutt må dette lipoamidet regenereres for at hele maskineriet skal kunne gå på nytt. Det skjer ved hjelp av enzymet dihydrolipoyl dehydrogenase, som overfører elektroner fra lipoamid til FAD, og deretter fra FADH₂ til NAD⁺.
Dette gir NADH – et viktig bærermolekyl for elektroner som senere skal brukes i elektrontransportkjeden.
Kofaktorene – der vitaminene gjør jobben sin
For at PDH-komplekset skal fungere, er det avhengig av fem kofaktorer, hvorav fire er avledet fra B-vitaminer.
TPP kommer fra vitamin B₁ (tiamin), CoA fra vitamin B₅ (pantotensyre), FAD fra vitamin B₂ (riboflavin) og NAD⁺ fra vitamin B₃ (niacin).
Lipoamid, selv om det ikke er et vitamin, er også essensiell i denne prosessen.
Disse kofaktorene fungerer ikke bare som hjelpemolekyler – de er direkte involvert i overføring av karbonatomer og elektroner, og dermed helt avgjørende for celleåndingens første oksidative steg.
Hva skjer når PDH ikke fungerer?
Dersom PDH-komplekset ikke virker som det skal, får ikke cellen omdannet pyruvat til acetyl-CoA.
Det betyr at pyruvat må gå en annen vei – og da dannes det i stedet melkesyre.
Dette skjer spesielt ved genetiske defekter i PDH-komplekset, eller ved mangel på B-vitaminer, særlig hos personer med dårlig ernæring eller høyt alkoholkonsum.
Konsekvensene kan være alvorlige.
Cellen mister tilgang på effektiv energiproduksjon, og går over til anaerob metabolisme. Det betyr økt melkesyre, lavere ATP-produksjon og energimangel, særlig i organer med høy energiomsetning som hjernen og musklene.
Hvordan PDH skrus av og på
Cellen regulerer PDH-komplekset ut fra energibehov.
Når energilagrene er fulle – det vil si når det er mye NADH og acetyl-CoA – skrus PDH av.
Det skjer ved hjelp av et enzym kalt pyruvat-dehydrogenase kinase (PDK), som legger til en fosfatgruppe og dermed inaktiverer komplekset.
PDK aktiveres av signaler som tyder på at cellen har nok energi, som høye nivåer av ATP, acetyl-CoA og NADH.
Men når cellen trenger energi, må PDH skrus på igjen.
Det gjør et annet enzym, pyruvat-dehydrogenase fosfatase (PDP), som fjerner fosfatgruppen og aktiverer komplekset på nytt.
PDP aktiveres blant annet av kalsiumioner – noe som er særlig viktig i muskelceller under fysisk aktivitet.
Trening og energi: PDH som kroppens energibryter
Når vi trener, må kroppen umiddelbart øke energiproduksjonen for å dekke muskelcellens behov.
En av de sentrale koblingene mellom fysisk aktivitet og cellens evne til å produsere energi er enzymkomplekset pyruvat-dehydrogenase (PDH).
Dette enzymkomplekset sørger for at pyruvat – sluttproduktet i glykolysen – omdannes til acetyl-CoA, som deretter kan gå inn i sitronsyresyklusen og bidra til produksjon av ATP.
Under fysisk aktivitet frigjøres kalsium i muskelcellene.
Dette kalsiumet fungerer som et signalmolekyl som aktiverer et annet enzym, PDP (pyruvat-dehydrogenase fosfatase).
Når PDP aktiveres, fjerner det en fosfatgruppe fra PDH-komplekset og skrur det dermed «på».
Aktivering av PDH gjør at mer pyruvat omdannes til acetyl-CoA, og kroppen får økt tilgang til drivstoff for energiproduksjon gjennom TCA-syklusen.
På denne måten fungerer PDH som en energibryter som slår seg på når cellen trenger energi, og av når det ikke er behov for mer produksjon.
Sitronsyresyklusen – cellens indre energiverk
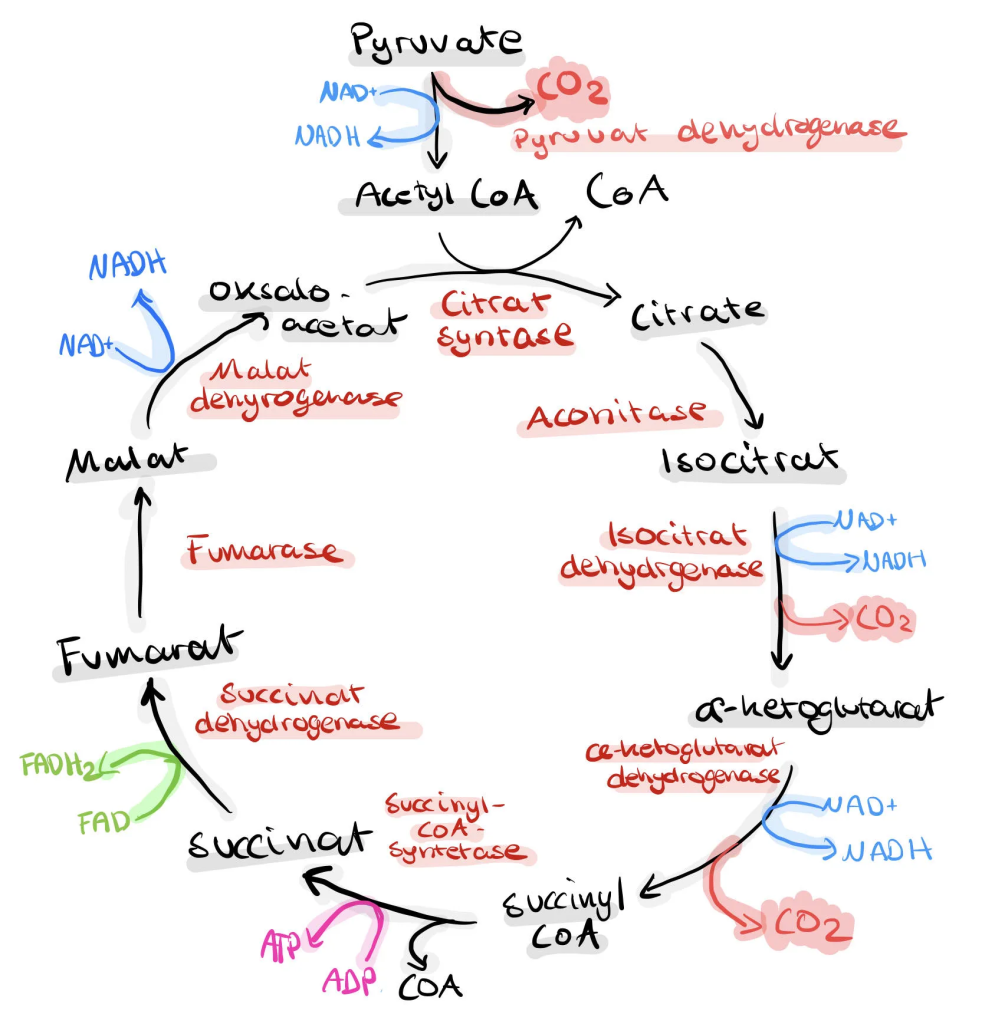
Etter at pyruvat er blitt omdannet til acetyl-CoA, er neste trinn i cellens energiproduksjon den såkalte sitronsyresyklusen – også kalt TCA-syklusen (trikarboksylsyresyklusen) eller Krebs-syklusen. Denne biokjemiske syklusen foregår i mitokondriets matrix og består av en serie enzymkatalyserte reaksjoner som trinnvis bryter ned acetyl-CoA til CO₂, samtidig som det dannes NADH og FADH₂. Disse elektronbærerne overfører energi til elektrontransportkjeden, hvor det dannes store mengder ATP.
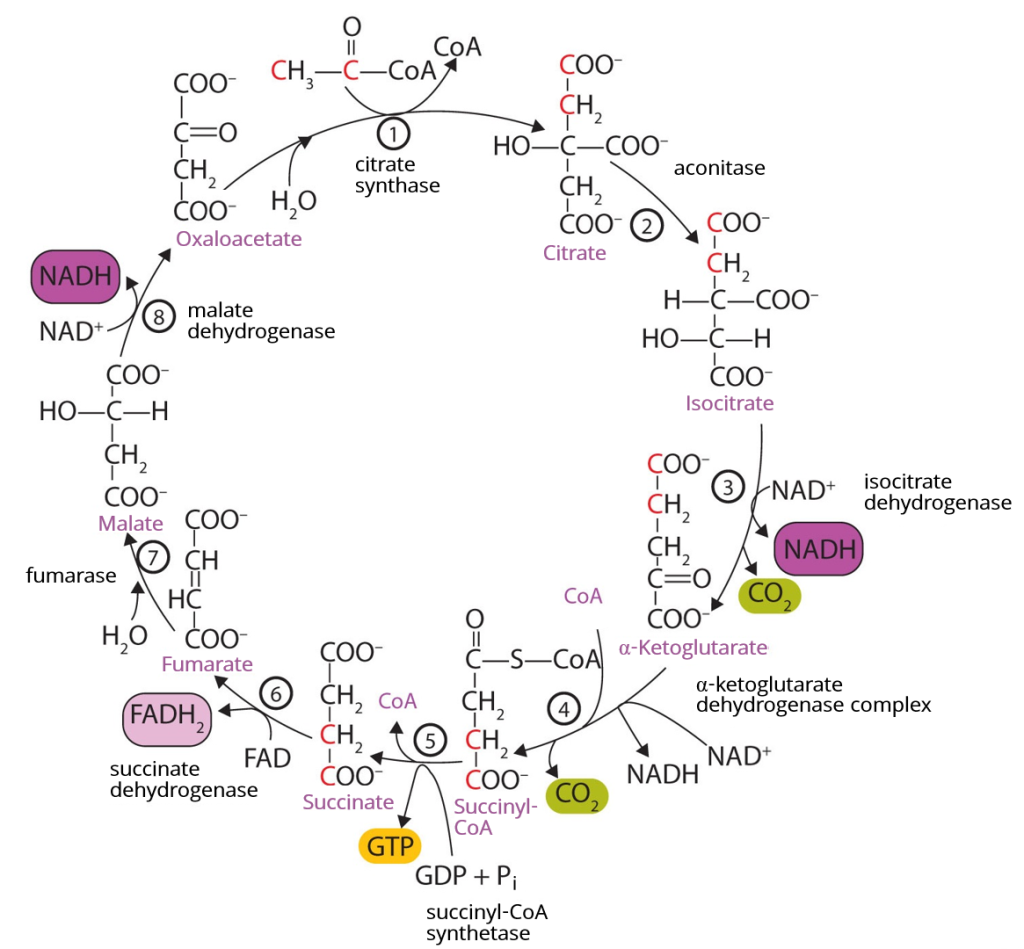
Trinnvis gjennomgang av TCA-syklusen
1. Fra Acetyl-CoA til citrat
Det første trinnet i syklusen er en kondensasjonsreaksjon der acetyl-CoA (to karbonatomer) reagerer med oksaloacetat (fire karbonatomer) og danner citrat (seks karbonatomer).
Reaksjonen katalyseres av enzymet citrate synthase. Det er denne reaksjonen som gir syklusen sitt navn: sitronsyresyklusen.
2. Fra citrat til isocitrat
Citrat omdannes til isocitrat i to trinn.
Først fjernes et vannmolekyl, og det dannes et ustabilt mellomprodukt, cis-aconitat. Deretter legges vann til igjen, men på en ny plass i molekylet, noe som resulterer i isocitrat.
Enzymet som styrer prosessen er akonitase, og det bruker et jern-svovelkompleks for å lette denne omorganiseringen av molekylet.
3. Fra isocitrat til α-ketoglutarat
Isocitrat oksideres og dekarboksyleres av enzymet isocitrat dehydrogenase.
Ett karbonatom fjernes i form av CO₂, og NAD⁺ reduseres til NADH.
Det som gjenstår er α-ketoglutarat – et femkarbonmolekyl.
Dette trinnet er viktig fordi det er det første i syklusen som både genererer energi og avgir CO₂.
4. Fra α-ketoglutarat til succinyl-CoA
I denne reaksjonen fjernes enda et karbonatom som CO₂, og energien fra denne reaksjonen brukes til å feste de gjenværende fire karbonene til Coenzym A, og det dannes succinyl-CoA.
Reaksjonen katalyseres av α-ketoglutarat dehydrogenase-komplekset, som ligner veldig på PDH-komplekset.
Det bruker også de samme fem ko-faktorene: TPP (vitamin B₁), lipoamid, FAD (B₂), NAD⁺ (B₃) og CoA (B₅). (Husk hvor viktig B-vitaminer er!)
5. Fra succinyl-CoA til succinat
Succinyl-CoA omdannes til succinat, og samtidig frigjøres CoA.
Energien som frigjøres brukes til å danne GTP (eller ATP, avhengig av celletype). Dette skjer ved såkalt substratnivåfosforylering – altså at ATP dannes direkte i selve reaksjonen uten hjelp av elektrontransportkjeden.
6. Fra succinat til fumarat
Succinat oksideres til fumarat, og enzymet succinat dehydrogenase reduserer FAD til FADH₂ i prosessen.
Dette enzymet er spesielt fordi det er det eneste enzymet i TCA-syklusen som er bundet til den indre mitokondriemembranen og fungerer også som kompleks II i elektrontransportkjeden.
7. Fra fumarat til malat
Fumarat tilføres et vannmolekyl i en reaksjon katalysert av enzymet fumarase. Produktet er L-malat, som er et firekarbonmolekyl.
8. Fra malat til oksaloacetat
I det siste trinnet oksideres malat til oksaloacetat, samtidig som NAD⁺ reduseres til NADH. Oksaloacetat er nå klar til å ta imot en ny acetylgruppe og starte syklusen på nytt.
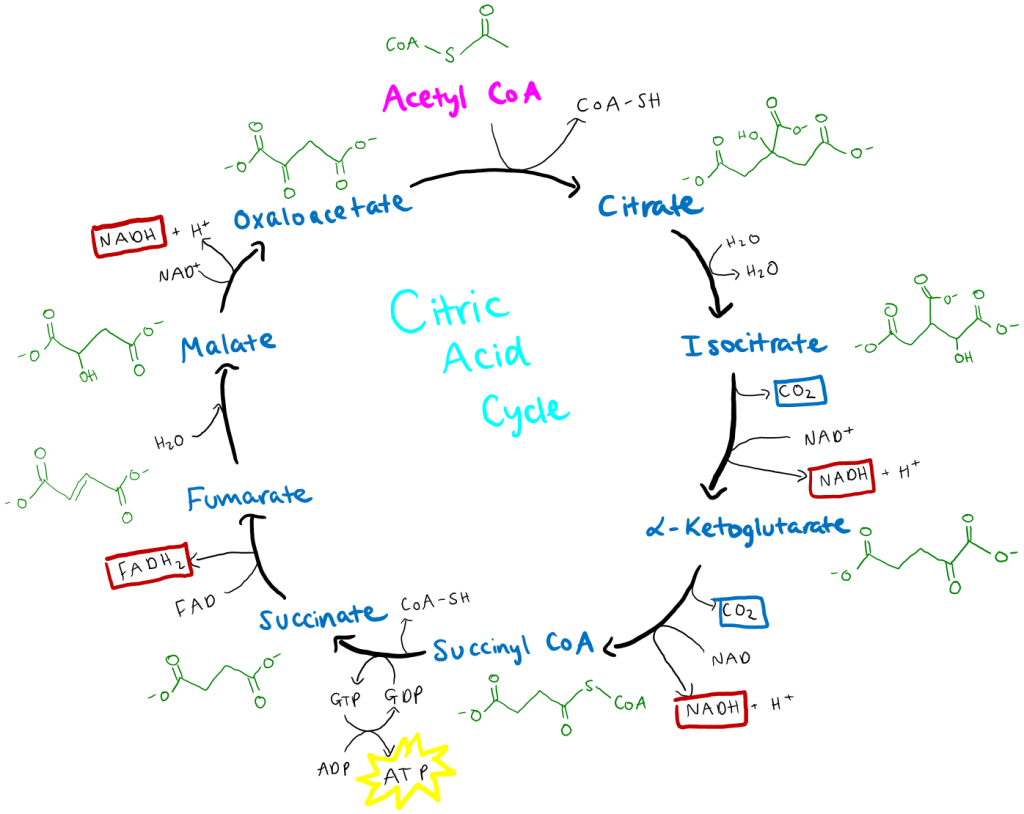
Energiregnskap for ett molekyl Acetyl-CoA
Hver runde i TCA-syklusen gir:
- 3 NADH
- 1 FADH₂
- 1 GTP (eller ATP)
- 2 CO₂
Siden hver glukosemolekyl danner to pyruvat og dermed to acetyl-CoA, gir én glukose dobbelt så mye av disse produktene fra TCA-syklusen alene – og dette før elektrontransportkjeden i det hele tatt har begynt!
Regulering av TCA-syklusen
TCA-syklusen er kroppens indre kraftverk – en kontinuerlig maskin som leverer energi til cellene. Men som med alle maskiner, må også denne justeres etter behov. Når cellen har mye energi, trappes aktiviteten ned. Når energien er lav, gires maskinen opp. Dette skjer gjennom finregulering av flere av syklusens nøkkelenzymer og ved tilgjengeligheten av startstoffene.
Energitilstand styrer farten
Et av de viktigste prinsippene for reguleringen av TCA-syklusen er balansen mellom cellens energibehov og energitilgang.
Når cellen har rikelig med energi – det vil si høye nivåer av ATP og NADH – bremser syklusen.
Enzymaktiviteten dempes, og produksjonen av nye energibærere reduseres.
Dette hindrer at cellen bruker ressurser på å lage energi som ikke trengs.
I tillegg fungerer noen av mellomproduktene som negative tilbakemeldingssignaler. For eksempel kan et overskudd av Acetyl-CoA eller Succinyl-CoA hemme tidligere trinn i syklusen, som citrate synthase og α-ketoglutarat dehydrogenase.
Dette gjør at cellen unngår å produsere unødvendige mengder av mellomprodukter og elektroner.
På den andre siden – når energinivåene er lave (lite ATP og mye ADP), og NAD⁺ er tilgjengelig – stimuleres syklusen for å produsere mer energi raskt.
Men det er ikke bare energinivåene som betyr noe.
Syklusen krever også byggesteiner for å kunne gå rundt: spesielt Acetyl-CoA og oksaloacetat. Uten disse stoffene stopper det opp.
Enzymregulering – kontrollpunktene i syklusen
Tre nøkkelenzymer i TCA-syklusen fungerer som regulatoriske porter:
1. Citrate synthase
– Dette enzymet starter syklusen ved å koble sammen Acetyl-CoA og oksaloacetat.
– Hemmes av ATP, NADH og Succinyl-CoA – som alle signaliserer at det allerede finnes nok energi i cellen.
2. Isocitrate dehydrogenase
– Dette er det første enzymet i syklusen som produserer NADH og CO₂.
– Aktiveres av ADP – et tegn på lav energi.
– Hemmes av ATP og NADH – altså når energien er tilstrekkelig.
3. α-ketoglutarat dehydrogenase
– Dette enzymet fungerer som et “sister-step” til PDH-komplekset og er svært likt både i struktur og regulering.
– Hemmes av NADH og Succinyl-CoA, som begge indikerer at cellen ikke trenger mer energi eller mellomprodukter.
Disse tre enzymene fungerer sammen som fartsdempere eller gasspedaler for syklusen, alt etter cellens behov.
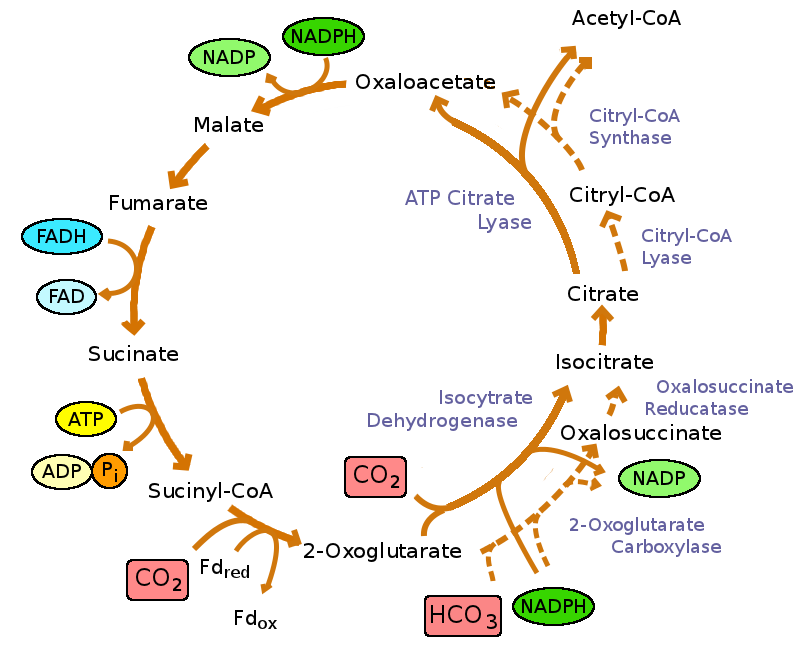
Test deg selv
Anaplerotiske reaksjoner – påfylling av mellomprodukter
TCA-syklusen er ikke bare et energiproduksjonssystem – den fungerer også som et viktig utgangspunkt for biosyntese.
Mange av mellomproduktene i syklusen, som oksaloacetat og α-ketoglutarat, blir nemlig trukket ut og brukt til å lage aminosyrer, nukleotider og andre viktige byggesteiner.
Men dette fører til et problem: Når mellomproduktene tappes, kan ikke syklusen gå like effektivt.
Her kommer anaplerotiske reaksjoner inn – det vil si reaksjoner som «fyller opp igjen» TCA-syklusen med nødvendige mellomprodukter.
Eksempler på anaplerotiske reaksjoner:
- Pyruvat → Oksaloacetat, katalysert av enzymet pyruvatkarboksylase.
- Fosfoenolpyruvat (PEP) → Oksaloacetat, katalysert av PEP-karboksylase.
- Pyruvat → Malat, katalysert av malatenzymet.
Disse reaksjonene sikrer at oksaloacetat og andre nøkkelstoffer alltid er tilgjengelige, slik at syklusen ikke stopper opp – selv når cellen bruker mellomproduktene til å lage noe annet.
Kataplerotiske reaksjoner – tapping av ressurser
Mens anaplerotiske reaksjoner fyller på syklusen, gjør kataplerotiske reaksjoner det motsatte: De fjerner mellomprodukter fra TCA-syklusen for å bruke dem i biosyntese. For eksempel:
- Malat kan konverteres til oksaloacetat → som videre danner aspartat → som igjen brukes til syntese av andre aminosyrer.
Dette er helt nødvendig for cellens overlevelse, men det skaper et behov for påfyll – som de anaplerotiske reaksjonene sørger for.
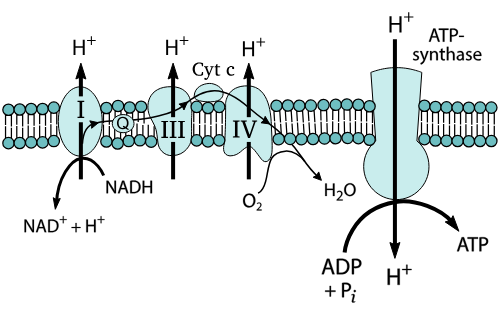
Elektrontransportkjeden og oksidativ fosforylering
Elektrontransportkjeden (ETC) er den siste fasen av celleåndingen som foregår i mitokondriene, cellens energifabrikk. ETC er en serie med proteinkomplekser som ligger i den indre mitokondriemembranen. Her overføres elektroner fra NADH og FADH₂, som produseres i glykolysen og sitronsyresyklusen, gjennom en kjede av reaksjoner. Denne prosessen driver produksjonen av ATP, cellens energibærer, gjennom en prosess kalt oksidativ fosforylering.
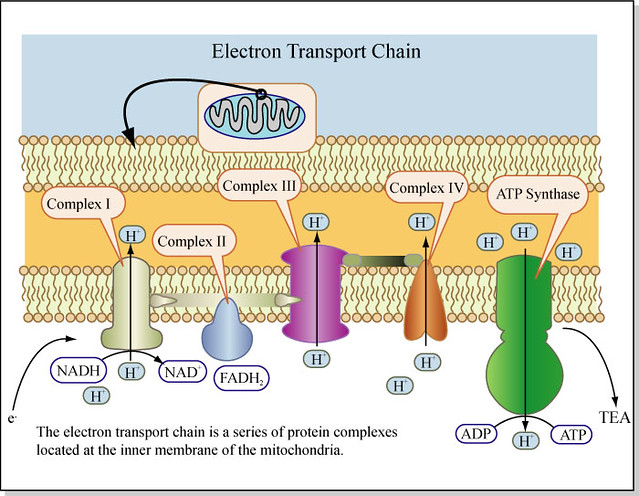
Steg i elektrontransportkjeden
Elektronoverføring:
- Elektroner fra NADH og FADH₂ sendes til elektrontransportkjeden.
- Elektronene beveger seg gjennom fire proteinkomplekser (Kompleks I–IV) i den indre mitokondriemembranen. Oksygen fungerer som den endelige elektronakseptoren og danner vann (H₂O) sammen med protoner (H⁺).
Protonpumpe og gradient:
- Energien som frigjøres når elektronene beveger seg gjennom kjeden, brukes til å pumpe protoner (H⁺) fra innsiden av mitokondriene (matrix) til mellomrommet mellom de to membranene (intermembrane space).
- Dette skaper en protongradient – en konsentrasjonsforskjell av protoner som fungerer som et energilager.
ATP-produksjon:
- Protonene (H⁺) strømmer tilbake inn i mitokondriematrixen gjennom enzymet ATP-syntase. Energien fra protonstrømmen brukes til å binde sammen ADP (adenosindifosfat) og fosfat (Pᵢ), noe som danner ATP (adenosintrifosfat).
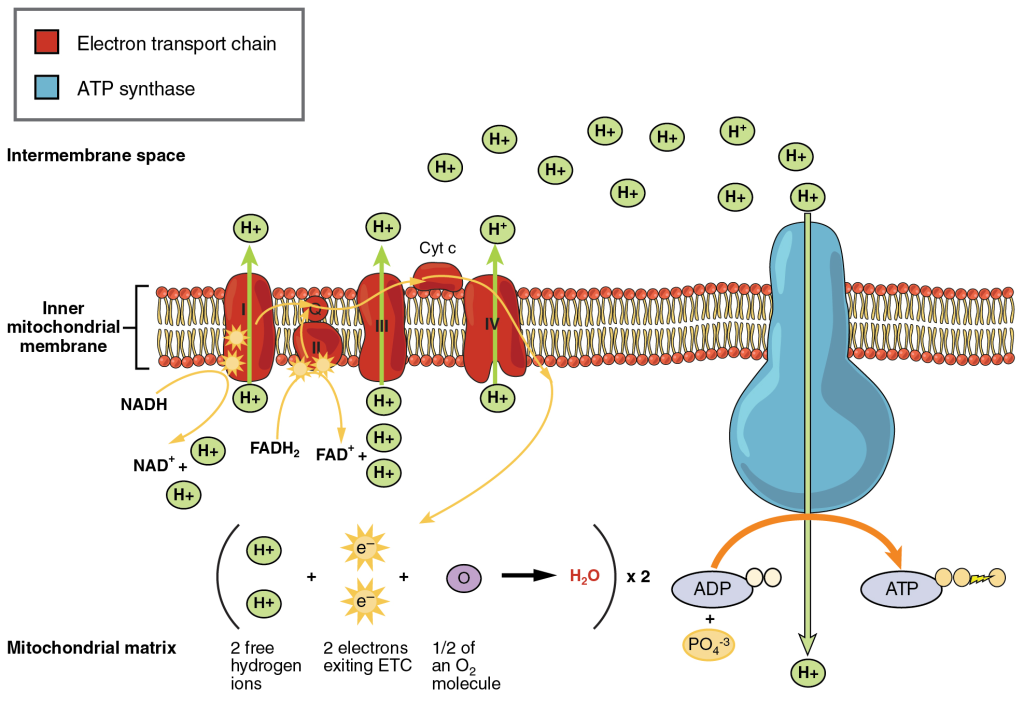
Kompleksene i ETC
Før vi snakker om kompleksene, trenger vi å vite om to viktige proteiner:
Ubiquinon (Coenzym Q10):
Ubiquinon er et lite, fettløselig molekyl som beveger seg fritt i den indre mitokondriemembranen. Det henter elektroner fra Kompleks I og II og frakter dem til Kompleks III.
Når ubiquinon tar opp elektroner, blir det redusert til ubiquinol (QH₂). Selv om ubiquinon ikke pumper protoner direkte, er det helt avgjørende for at elektrontransportkjeden skal fungere.
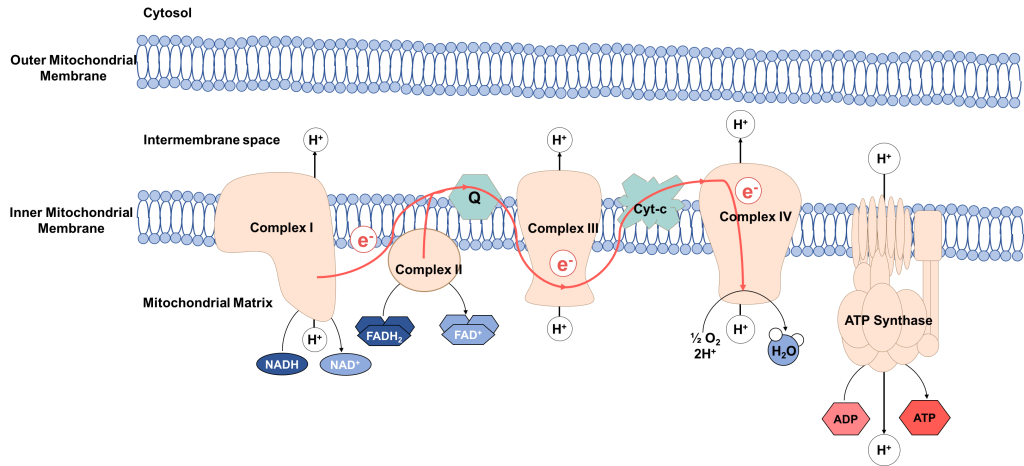
Cytokrom C:
Cytokrom C er et vannløselig protein som befinner seg i det intermembrane rommet. Det mottar elektroner fra Kompleks III og leverer dem videre til Kompleks IV. Cytokrom C transporterer ett elektron om gangen, noe som sikrer presis elektronoverføring.
Dette proteinet er viktig for at oksygen til slutt kan akseptere elektronene og danne vann.
Ubiquinon og Cytokrom C fungerer som elektronbærere som frakter elektroner mellom de store proteinkompleksene i elektrontransportkjeden. Uten dem ville energiproduksjonen i mitokondriene stoppet opp.
Kompleks I – Startpunktet i elektrontransportkjeden
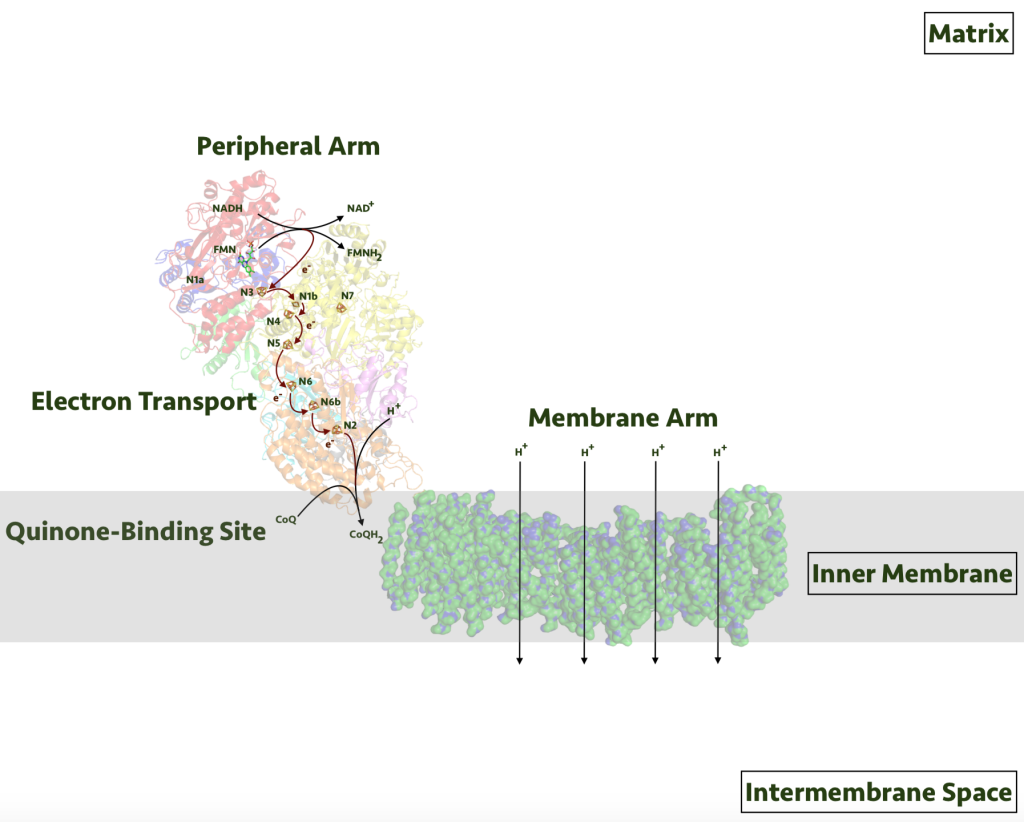
Reisen gjennom elektrontransportkjeden begynner i Kompleks I, også kjent som NADH dehydrogenase. Dette enorme proteinkomplekset er det første stoppet for elektronene som fraktes med NADH – og det er her den viktige energioverføringen starter.
Fra NADH til ubiquinon – elektronene får skyss
Når NADH ankommer Kompleks I, avgir det to elektroner (e⁻). Disse elektronene overføres først til flavinmononukleotid (FMN) – et molekyl som fungerer som en slags mottaksstasjon. FMN blir redusert til FMNH₂, og sender deretter elektronene videre nedover en serie av jern-svovelklustre (Fe-S-sentre). Disse Fe-S-kompleksene fungerer som små koblinger – de mottar, holder og videresender elektronene i en slags stafett.
Til slutt når elektronene frem til ubiquinon (koenzym Q10), som flyter fritt i den indre mitokondriemembranen. Når ubiquinon mottar elektronene, blir det redusert til ubiquinol (QH₂) – en mer energirik form. Ubiquinol tar så med seg elektronene videre til neste stopp: Kompleks III.
Hva skjer med energien?
Denne elektronoverføringen er ikke bare en transport – den frigjør også energi. Kompleks I utnytter denne energien til å pumpe fire protoner (H⁺) fra mitokondriematrixen over til det intermembrane rommet. Dette er et helt sentralt punkt i mitokondriets arbeid: Ved å flytte protoner over membranen skaper cellen en protongradient, en slags batterilading, som senere brukes til å lage ATP.
Kompleks I er altså både en elektronstransportør og en protonpumpe. Den gjør to ting samtidig:
- Overfører elektroner fra NADH til ubiquinon.
- Pumper ut protoner for å bygge opp et elektro-kjemisk spenningsfelt over den indre mitokondriemembranen.
Denne spenningsforskjellen er som en spent fjær – den lagrer energi som senere brukes i ATP-syntasen for å produsere selve energivalutaen i kroppen: ATP.
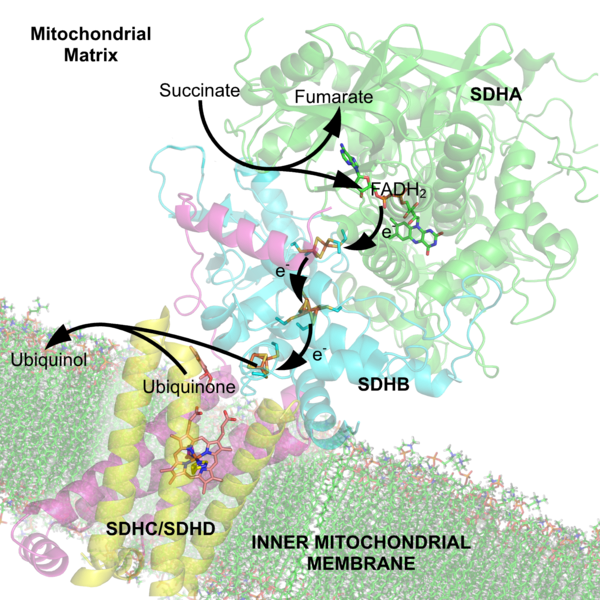
Kompleks II – Koblingen mellom TCA og elektrontransport
Kompleks II, også kalt succinat dehydrogenase, er en litt annerledes deltaker i elektrontransportkjeden. Dette er nemlig det eneste enzymkomplekset som både er del av TCA-syklusen og elektrontransportkjeden samtidig.
I TCA-syklusen omdanner enzymet succinat til fumarat, og i denne prosessen overføres elektroner til FAD, som blir til FADH₂. Det er disse elektronene som så ledes inn i elektrontransportkjeden.
FADH₂ leverer elektronene videre via en kjede av jern-svovel-sentre og til slutt til ubiquinon (Q), som igjen blir redusert til ubiquinol (QH₂) – akkurat som i Kompleks I.
Men det er én stor forskjell:
Kompleks II pumper ikke protoner. Derfor bidrar det ikke direkte til å bygge opp protongradienten som driver ATP-produksjonen, og det forklarer også hvorfor FADH₂ gir mindre ATP enn NADH (ca. 1,5 ATP per FADH₂ sammenlignet med 2,5 per NADH).
Kompleks II fungerer derfor som en elektronoverfører som kobler metabolismen i TCA-syklusen direkte til elektrontransportkjeden – og er helt essensiell for å utnytte energien fra FADH₂.
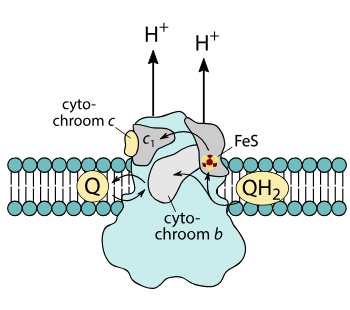
Kompleks III – Mellomstasjonen for elektroner
Kompleks III, også kjent som cytokrom bc₁-komplekset, er et viktig bindeledd i elektrontransportkjeden. Her overføres elektroner fra ubiquinol (QH₂) til cytokrom c, et lite løselig protein som frakter elektronene videre til Kompleks IV.
Når ubiquinol ankommer Kompleks III, donerer det to elektroner:
- Det første elektronet går via jern-svovel-proteinet og cytokrom c₁ til cytokrom c, som bærer det videre.
- Det andre elektronet tar en omvei gjennom cytokrom b-kompleksene (bL og bH) før det hjelper til med å regenerere ubiquinon (Q) i en prosess som kalles Q-syklusen.
Samtidig pumpes fire protoner (H⁺) ut i det intermembrane rommet. Dette bidrar til å opprettholde den protongradienten som driver ATP-produksjonen.
Med dette fungerer Kompleks III som både en elektronoverfører og protonpumpe, og sikrer at cellens energiproduksjon går som den skal.
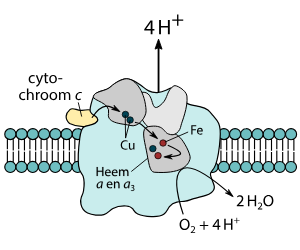
Kompleks IV (Cytokrom c oksidase):
Kompleks IV, også kjent som cytokrom c oksidase, er det siste proteinkomplekset i elektrontransportkjeden. Det spiller en kritisk rolle i cellens energiomsetning ved å bruke oksygen som den endelige elektronakseptoren.
Historien begynner med at fire elektroner (4e⁻) blir overført fra fire cytokrom c-proteiner (Cyt c) til Kompleks IV.
Elektronene beveger seg gjennom ulike kofaktorer, inkludert CuA, heme a, og CuB-heme a₃-senteret, før de når sitt endelige mål.
På dette punktet møter elektronene oksygen (O₂), som fungerer som den siste elektronakseptoren.
Oksygen kombinerer seg med elektroner og protoner (H⁺) fra matriks for å danne vann (H₂O). Totalt bruker denne prosessen fire protoner fra matriks for vannproduksjon.
Samtidig brukes energien fra elektronoverføringen til å pumpe fire protoner (4H⁺) ut i det intermembrane rommet. Dette skaper en protongradient som driver syntesen av ATP i neste steg, katalysert av ATP-syntase.
Kompleks IV fungerer som cellens «motor» som avslutter elektrontransporten, produserer vann, og bidrar til opprettholdelsen av en protongradient som er essensiell for energiproduksjon.
ATP-syntase
ATP-syntase (Complex V) fungerer som en energimaskin i cellene. Den bruker strømmen av protoner (H⁺) som er samlet i det intermembrane rommet i mitokondriene, til å lage ATP.

Hvordan virker det?
- Protonstrøm gjennom F₀-komplekset: Protonene flyter tilbake inn i mitokondriematrixen gjennom F₀, som fungerer som en protonkanal. Denne strømmen av protoner får en roterende enhet i F₀ til å snurre.
- Når rotoren snurrer, overfører den bevegelsen til γ-aksen i F₁-komplekset. Dette fører til endringer i formen på tre β-subenheter i F₁.
- Tre steg i ATP-produksjon:
- Løst binding (L): β-subenheten binder ADP og fosfat med høy affinitet.
- Stram binding (T): Energien fra rotasjonen tvinger ADP og fosfat til å danne ATP.
- Åpen binding (O): ATP frigjøres fra subenheten.
For hver full rotasjon av γ-aksen (360°) dannes tre ATP-molekyler. Ved normale fysiologiske forhold kan denne «maskinen» lage opptil 300 ATP-molekyler per sekund.
Regulering av ATP-syntese:
Produksjonen styres av tilgangen på ADP og fosfat. Når cellen bruker opp ATP, øker mengden ADP, som igjen driver mer ATP-produksjon. Lavt oksygennivå kan bremse prosessen, fordi elektrontransportkjeden ikke kan pumpe nok protoner.
Når cellen bruker mye energi, som når du løper eller trener, bruker den opp ATP (energi). Dette gjør at det blir mer ADP (brukte ATP-molekyler) i cellen. Dette er et tegn for cellen om at den må lage mer energi.
- Elektrontransportkjeden jobber raskere: Cellen skrur opp farten på maskineriet som lager energi i mitokondriene, slik at den kan lage mer ATP.
- Mer pyruvat brukes: Pyruvat, som er sluttproduktet av glykolysen (nedbrytning av sukker), går inn i sitronsyresyklusen (TCA-syklusen) for å produsere de nødvendige komponentene som driver energiproduksjonen.
- Glykolyse går raskere: For å få mer pyruvat, bryter cellen raskere ned glukose (sukker) gjennom glykolysen.
Alt dette skjer automatisk for å sikre at cellen har nok energi når den trenger det.
Resultat av ETC og oksidativ fosforylering
- For hvert glukosemolekyl som brytes ned, produseres ca. 30–32 ATP i cellen.
- Dette inkluderer:
- ATP fra glykolysen.
- ATP fra sitronsyresyklusen.
- ATP produsert via elektrontransportkjeden.
Oppsummering i enkle trinn
- Elektroner fra NADH og FADH₂ går gjennom proteinkomplekser (Kompleks I-IV).
- Protoner pumpes ut, og det dannes en gradient.
- ATP-syntase bruker protonmotorkraften til å lage ATP fra ADP og fosfat.
- Oksygen fanger opp elektronene til slutt og danner vann.
ATP-syntase
Dypest inne i hver celle ligger mitokondriene – cellens egne kraftverk. Og i hjertet av disse kraftverkene finner vi en molekylær maskin som er like elegant som den er livsnødvendig: ATP-syntase. Dette enzymkomplekset, også kalt kompleks V, er ansvarlig for å lage nesten all ATP i kroppen – det universelle energimolekylet som driver alt fra muskelkontraksjoner til nervecellesignaler og proteinsyntese.
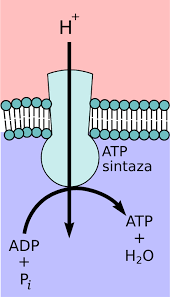
Energi lagres som en protongradient
ATP-syntase er drevet av en protongradient som bygges opp av elektrontransportkjeden. Når NADH og FADH₂ leverer elektroner til kjeden, brukes energien til å pumpe protoner (H⁺) fra mitokondriematrixen og ut i det intermembrane rommet. Dette skaper en slags energisk «vanntrykk» – en protongradient med høyt trykk utenfor og lavt trykk inni mitokondriet.
Denne forskjellen i protonkonsentrasjon representerer potensiell energi – et slags lagret «fall» som ATP-syntase bruker som drivkraft.
En snurrende maskin
ATP-syntase består av to hoveddeler: en som er innebygd i membranen og en som stikker ut i mitokondriematrixen.
- F₀-komplekset er den membranbundne delen som fungerer som en protonkanal. Her strømmer protonene inn fra det intermembrane rommet.
- F₁-komplekset er enzymdelen som stikker ut i matrixen og produserer selve ATP.
Når protonene strømmer gjennom F₀-delen, settes en rotor i bevegelse. Denne rotasjonen overføres til γ-aksen, som stikker inn i F₁-delen. Bevegelsen forårsaker at de tre β-subenhetene i F₁ endrer form – og nettopp disse formendringene er det som driver selve ATP-produksjonen.
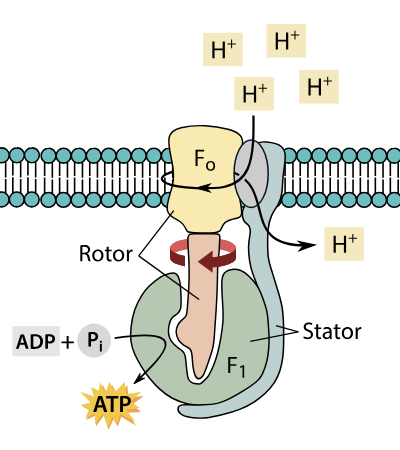
Tre steg – én rotasjon, tre ATP
ATP-syntase produserer ett ATP-molekyl for hver tredjedel av en rotasjon. De tre β-subenhetene går gjennom følgende tre trinn i tur og orden:
- Løs binding (L): ADP og uorganisk fosfat (Pi) bindes.
- Stram binding (T): Energi fra rotasjonen driver sammenkoblingen av ADP og Pi til ATP.
- Åpen binding (O): Det ferdige ATP-molekylet slippes fri.
For hver full rotasjon (360°) av γ-aksen, dannes tre ATP-molekyler. I raske celler som arbeider hardt, kan ett ATP-syntase-kompleks lage opptil 300 ATP i sekundet
Regulering – energi på forespørsel
ATP-produksjonen styres nøye etter kroppens behov. Når cellen har brukt mye energi og ADP-nivået øker, stimuleres ATP-syntasen til å produsere mer. Det er altså etterspørselen som driver produksjonen.
Men systemet er også avhengig av oksygen. Dersom oksygenmangel oppstår – for eksempel ved respirasjonssvikt – stopper elektrontransportkjeden opp, protongradienten svekkes, og ATP-produksjonen bremser eller stanses.
Et koordinert energiløft
Når energibehovet i cellen øker, for eksempel under fysisk aktivitet, skjer en rekke tilpasninger samtidig:
- Glykolysen akselererer for å produsere mer pyruvat.
- Pyruvat omdannes til acetyl-CoA og går inn i TCA-syklusen.
- TCA-syklusen produserer mer NADH og FADH₂.
- Elektrontransportkjeden jobber raskere og pumper flere protoner.
- ATP-syntase får mer drivstoff – og spinner raskere for å dekke behovet.
Alt dette skjer sømløst og automatisk – en fantastisk koordinering som sikrer at cellene får nok energi til enhver tid.
Total ATP-produksjon per glukosemolekyl
Samlet sett gir ett glukosemolekyl:
- 2 ATP fra glykolysen
- 2 ATP (eller GTP) fra TCA-syklusen
- Ca. 26–28 ATP fra elektrontransportkjeden og ATP-syntase
→ Totalt 30–32 ATP per glukose.
Shuttle-mekanismer – hvordan NADH fra glykolysen kommer seg inn i mitokondriene
Under glykolysen i cytosol dannes det NADH, et viktig molekyl som bærer med seg høyenergielektroner. For at disse elektronene skal bidra til ATP-produksjon i elektrontransportkjeden (ETC), må de på en eller annen måte komme seg inn i mitokondriene. Men her oppstår et lite logistikkproblem: NADH i seg selv kan ikke krysse den indre mitokondriemembranen.
Løsningen? Kroppen benytter seg av smarte «shuttle»-systemer – biokjemiske mekanismer som overfører elektronene fra NADH over membranen ved hjelp av transportmolekyler. Det finnes to slike systemer, og hvilken som brukes avhenger av vevstype og energibehov.
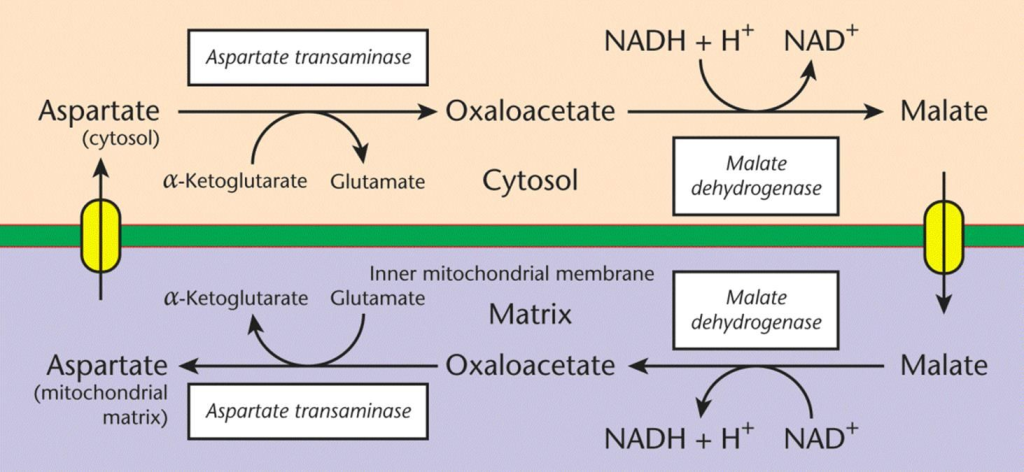
Malat–aspartat-shuttle (aktiv i hjerte, lever og nyre)
Denne shuttlen er effektiv og ATP-rik, og brukes i organer som er avhengige av høy energiproduksjon.
Slik fungerer den:
- I cytosol reduseres oksaloacetat (OAA) til malat ved hjelp av NADH. NADH gir fra seg elektroner og blir til NAD⁺.
- Malat transporteres inn i mitokondriene via en malat–α-ketoglutarat antiport.
- Inne i mitokondriene oksideres malat tilbake til oksaloacetat, og NADH gjenoppstår – nå på riktig side av membranen.
- Elektronene fra det regenererte NADH mates inn i elektrontransportkjeden via kompleks I, som gir maksimalt ATP-utbytte.
- Oksaloacetat omdannes til aspartat, som fraktes ut til cytosol igjen for å gjenta syklusen.
Resultat: For hvert NADH-molekyl som sendes via malat-aspartat-shuttlen, får vi ca. 2,5 ATP.
Glyserol-3-fosfat-shuttle (aktiv i skjelettmuskler og hjerne)
Denne shuttlen er rask, men mindre effektiv, og brukes i vev som trenger høy omsetningshastighet heller enn maksimal ATP-utbytte.
Slik fungerer den:
- I cytosol reduseres dihydroksyacetonfosfat (DHAP) til glyserol-3-fosfat ved hjelp av NADH.
- Glyserol-3-fosfat beveger seg til den ytre mitokondriemembranen, hvor det oksideres tilbake til DHAP av et enzym som heter mitokondriell glyserol-3-fosfat-dehydrogenase.
- I denne prosessen overføres elektronene til FAD, som danner FADH₂.
- FADH₂ leverer elektronene direkte til kompleks II i elektrontransportkjeden – altså forbi kompleks I.
Resultat: For hvert NADH-molekyl brukt i glyserol-3-fosfat-shuttlen, produseres det ca. 1,5 ATP – mindre enn ved malat-aspartat, fordi kompleks I hoppes over.
Hvorfor to shuttler?
- Organer som hjerte og lever prioriterer maksimal ATP-produksjon og bruker derfor malat–aspartat-shuttlen.
- Muskler og hjerne trenger rask energi og bruker glyserol-3-fosfat-shuttlen, selv om det gir lavere ATP-utbytte.
Valget av shuttle påvirker dermed hvor mye netto ATP man får per glukosemolekyl. Det klassiske tallet på 30–32 ATP per glukose tar hensyn til at ulike vev bruker ulike shuttler.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3