Oksygentransport i blodet
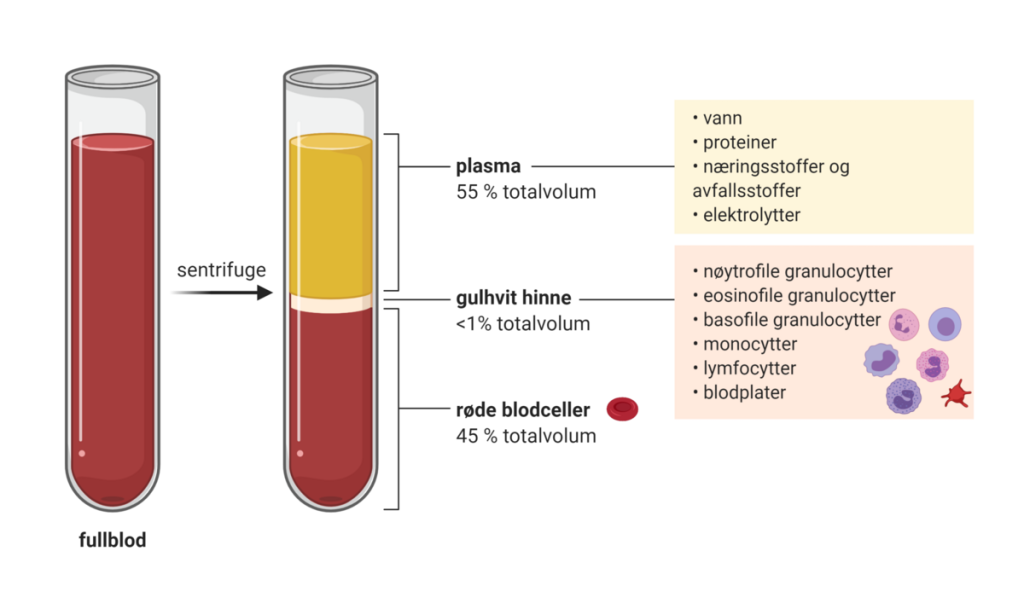
Oksygen er livsviktig for cellenes energiproduksjon, men det kan ikke fraktes effektivt gjennom kroppen alene. For å sikre god oksygentilførsel til alle kroppens vev og organer, transporteres oksygen i blodet på to hovedmåter: enten oppløst i plasma eller bundet til hemoglobin i de røde blodcellene.
Oksygen oppløst i plasma
En liten mengde oksygen løses direkte i blodplasmaet – den væskefylte delen av blodet. Denne oppløste fraksjonen følger Henry’s lov, som sier at mengden gass som løses i en væske er proporsjonal med gassens partialtrykk.
Det betyr at jo høyere oksygentrykk det er i lungene, jo mer oksygen løses opp i blodet.
Men denne mekanismen er svært begrenset:
Ved en normal oksygenverdi i arterieblodet (PaO₂ ≈ 13,3 kPa), løses bare rundt 0,3 ml O₂ per 100 ml blod.
Dette utgjør bare 1–2 % av kroppens totale oksygentransport i hvile, og er derfor i seg selv en utilstrekkelig mekanisme for å dekke oksygenbehovet. For å kompensere, måtte hjertet ha pumpet over 1000 liter blod i minuttet – noe som er fysiologisk umulig.
Oksygen bundet til hemoglobin
Den klart viktigste transportformen for oksygen er via hemoglobin (Hb), et jernholdig protein som finnes i de røde blodcellene.
Struktur og funksjon
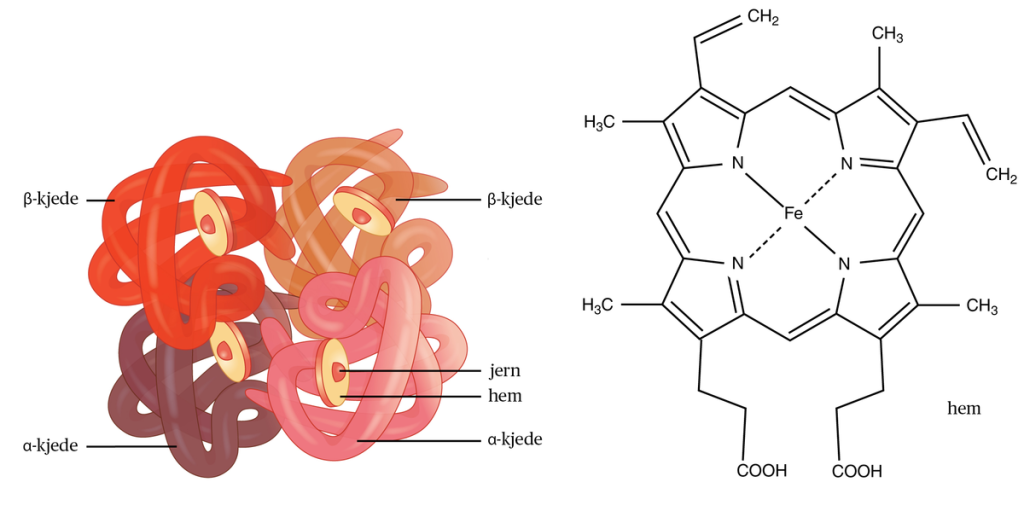
Hvert hemoglobinmolekyl består av fire proteinkjeder (to alfa- og to betakjeder), og hver av disse bærer en hemegruppe med et jernatom i sin reduserte form (Fe²⁺). Det er dette jernet som binder oksygen – og fordi det er fire jernatomer per hemoglobin, kan hvert molekyl binde fire oksygenmolekyler.
Denne bindingen er reversibel, noe som gjør hemoglobin ideelt til å ta opp oksygen i lungene og slippe det av i vevet der det trengs.
Transportkapasitet
Et gram hemoglobin kan binde omtrent 1,39 ml O₂.
Med normal hemoglobinkonsentrasjon i blodet (ca. 15 g/100 ml), kan blodet binde omtrent 20,9 ml O₂ per 100 ml blod. Dette er mer enn 70 ganger mer enn hva som kan transporteres i oppløst form, og gjør effektiv oksygentransport mulig.
Men bindingen av oksygen avhenger også av oksygenmetningen (SaO₂) – altså hvor stor andel av hemoglobinets bindingsplasser som faktisk er okkupert av oksygen. Hos friske personer er SaO₂ typisk 95–99 % i arterieblod og 60–80 % i veneblod.
Viktige faktorer som påvirker oksygentransporten
- Mengde hemoglobin i blodet
Jo høyere Hb, desto mer oksygen kan blodet frakte. Ved anemi har man lav Hb, og selv om metningen er normal, vil total oksygentransport være redusert. Ved kronisk lungesykdom kan kroppen forsøke å kompensere ved å øke Hb-produksjonen. - Oksygenmetning (SaO₂)
Lav SaO₂ betyr at færre hemoglobinmolekyler er lastet med oksygen. Dette kan skyldes nedsatt lungefunksjon, dårlig ventilasjon-perfusjon-forhold, eller diffusjonsproblemer over alveoleveggen. - Minuttvolum (hjertets pumpekapasitet)
Selv om oksygeninnholdet i blodet er lavt, kan økt hjerteaktivitet kompensere midlertidig ved å øke mengden blod – og dermed oksygen – som leveres til vevet per minutt. - Hemoglobinets oksygenaffinitet
Hemoglobin binder oksygen med varierende styrke avhengig av forholdene. Dette vises i oksygenets dissosiasjonskurve, som påvirkes av blant annet pH, temperatur og konsentrasjonen av 2,3-DPG (et stoff som finnes i erytrocytter). Lav pH (acidose), høy temperatur og høy 2,3-DPG svekker bindingen og letter oksygenavgivelse til vev – kjent som Bohr-effekten.
Methemoglobinemi – når hemoglobin ikke fungerer
Under visse forhold kan jernet i hemoglobinet oksideres fra Fe²⁺ til Fe³⁺, og danne methemoglobin.
Dette molekylet kan ikke binde oksygen, og reduserer dermed blodets oksygentransportkapasitet. Normalt holdes nivåene lave av egne enzymatiske systemer, som methemoglobinreduktase.
Oppsummering
| Transportform | Andel av totalt O₂ | Mekanisme | Viktighet |
|---|---|---|---|
| Oppløst i plasma | 1–2 % | Fysisk løst (Henry’s lov) | Lite bidrag |
| Bundet til Hb | 98–99 % | Reversibel binding til Fe²⁺ i hemegruppene | Hovedtransport |
For effektiv oksygentransport er det altså ikke nok at vi puster – kroppen er helt avhengig av at hemoglobinet fungerer som det skal.
Oksyhemoglobinets dissosiasjonskurve
For å forstå hvordan oksygen transporteres fra lungene til vevet, må vi forstå forholdet mellom oksygentrykket i blodet og hvor mye av hemoglobinet som er mettet med oksygen. Dette forholdet illustreres gjennom den såkalte oksyhemoglobinets dissosiasjonskurve, som er en grafisk fremstilling av sammenhengen mellom partialtrykket av oksygen (PO₂) og hemoglobinets metningsgrad (SaO₂).
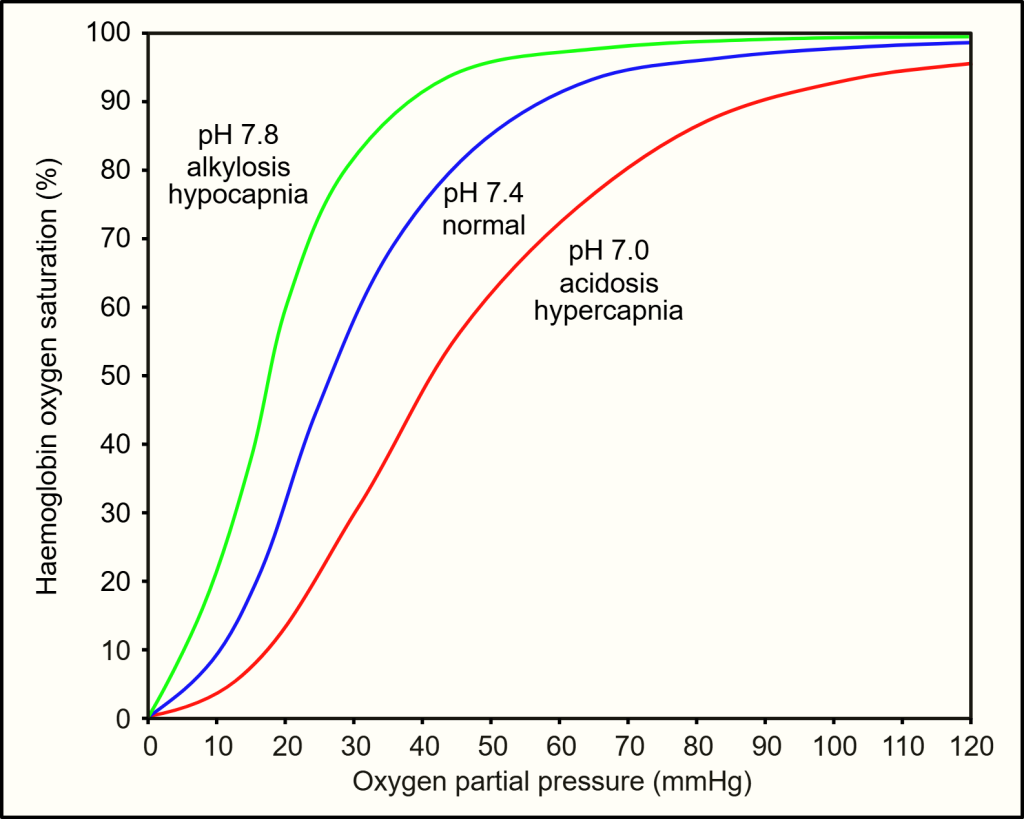
Kurvens form – en S-kurve med stor betydning
Dissosiasjonskurven er sigmoid (S-formet), noe som gjenspeiler den kooperative bindingen mellom hemoglobin og oksygen:
Når det første oksygenmolekylet binder seg til en av hemgruppene i hemoglobin, endres hemoglobinets tredimensjonale struktur.
Dette gjør at de tre gjenværende hemegruppene får økt affinitet for oksygen. Jo flere oksygenmolekyler som allerede er bundet, jo lettere binder de neste seg. Dette fenomenet kalles kooperativ binding.
På samme måte, når oksygen begynner å løsne fra hemoglobin i vevet, blir det også lettere for de resterende molekylene å slippe taket.
Denne doble mekanismen – sterk binding i lungene og lett frigjøring i vevet – gjør hemoglobin svært effektivt som oksygentransportør.
Hva forteller kurvens ulike deler?
1. Plateau (øverste del av kurven):
I området hvor PO₂ er rundt 10–13 kPa, er hemoglobinet nesten fullstendig mettet med oksygen – typisk rundt 98 % i arterielt blod.
Dette er området som gjelder i lungene.
Her skjer det nesten ingen endring i metningsgrad selv om PO₂ øker, for eksempel ved å gi pasienten ren oksygen.
Dette gir en beskyttelseseffekt mot oksygentoksisitet – selv om vi puster inn mer oksygen, binder hemoglobinet ikke mer enn det trenger.
2. Bratt del (midt på kurven):
I området hvor PO₂ synker til mellom 8 og 4 kPa, faller metningsgraden raskt.
Her er hemoglobinet mer «villig» til å slippe fra seg oksygen.
Dette skjer i vevet, hvor oksygentrykket er lavere enn i lungene.
Dette området er fysiologisk kritisk: små reduksjoner i PO₂ gir store endringer i SaO₂, og dermed i hvor mye oksygen som er tilgjengelig for vevet.
Det er her kroppen regulerer oksygentilførselen mest aktivt.
Ved PO₂ rundt 5,3 kPa, som er typisk for venøst blod, har hemoglobinet fortsatt rundt 77 % metning.
Det betyr at bare ca. 25 % av oksygenet avgis ved hver runde – resten holdes i reserve for økt behov, som ved fysisk aktivitet.
3. Nederste del (under 4 kPa):
Her begynner kurven å flate ut igjen, og hemoglobinet holder på oksygenet sterkere – selv om det fortsatt er i lavt trykkmiljø.
Dette skjer ved alvorlig hypoksi, hvor kroppen forsøker å ekstrahere mest mulig oksygen. Likevel vil mye av metabolismen her måtte foregå anaerobt, fordi tilførselen ikke dekker behovet.
P50 – et mål på oksygenaffinitet
Et sentralt punkt på kurven er P50 – dette er det oksygentrykket hvor 50 % av hemoglobinet er mettet. Hos friske voksne er dette vanligvis rundt 3,5 kPa. Hvis P50 øker, betyr det at hemoglobinet har lavere affinitet for oksygen (det slipper oksygen lettere); hvis P50 synker, har det høyere affinitet (det holder bedre på oksygenet).
Hemoglobinets molekylære tilstander: T- og R-form
Hemoglobin finnes i to hovedformer:
- T-form (tense): Lav affinitet for oksygen, finnes hovedsakelig i deoksygenert blod.
- R-form (relaxed): Høy affinitet for oksygen, finnes når oksygenet binder seg.
Bindingen av det første oksygenmolekylet fører til en overgang fra T-form til R-form, og dette forsterker den kooperative bindingen som gir den karakteristiske S-kurven.
Tall og klinisk betydning
| Parameter | Arterielt blod | Venøst blod |
|---|---|---|
| PO₂ | 13,3 kPa | 5,3 kPa |
| SaO₂ | 98 % | 77 % |
| O₂-innhold | 21 ml/100 ml | 16 ml/100 ml |
| A–VDO₂ (forskjell) | ~5 ml/100 ml | — |
Forskjellen mellom arterielt og venøst oksygeninnhold representerer det oksygenet som vevet faktisk forbruker – og er et viktig mål for oksygentilførselen.
Forskyvning av dissosiasjonskurven
Kurven kan skifte mot venstre eller høyre, avhengig av fysiologiske forhold. Disse forskyvningene har stor klinisk betydning fordi de påvirker oksygentransport og -levering til vev.
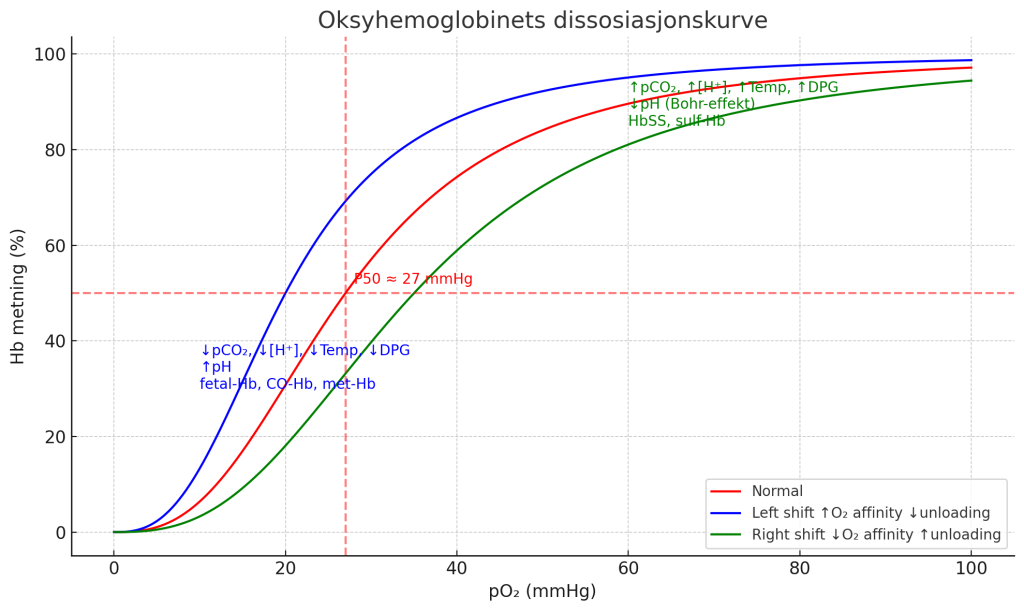
Forskyvning av oksyhemoglobinets dissosiasjonskurve
Oksyhemoglobinets dissosiasjonskurve beskriver forholdet mellom oksygenets partialtrykk (PO₂) og hemoglobinets metningsgrad (SaO₂).
Denne kurven har en karakteristisk S-form (sigmoid), som reflekterer hemoglobinets kooperative oksygenbinding: Når ett oksygenmolekyl binder seg til hemoglobin, øker affiniteten for de neste molekylene.
Under normale fysiologiske forhold gir kurven en høy metning i lungene (ved høyt PO₂) og god oksygenfrigjøring i vevene (ved lavere PO₂). Men ulike faktorer – som pH, temperatur, CO₂-nivå og intracellulære komponenter som 2,3-DPG – kan føre til at kurven forskyves mot høyre eller venstre. Slike forskyvninger har stor klinisk betydning fordi de påvirker hvor lett eller vanskelig hemoglobin gir fra seg oksygen til vevet.
Venstreforskyvning – økt affinitet for oksygen
Når kurven forskyves mot venstre, betyr det at hemoglobin har økt affinitet for oksygen. Det holder altså bedre på oksygenmolekylene, og slipper dem ikke like lett. Resultatet blir at oksygen avgis mindre effektivt til vevet, selv om metningen i blodet kan være høy. Dette er uheldig i situasjoner hvor vev har økt oksygenbehov, siden oksygen ikke frigjøres tilstrekkelig.
Flere forhold kan føre til venstreforskyvning:
- Lav temperatur: Nedkjøling stabiliserer hemoglobinets oksygenbundne form (R-formen), og gjør at oksygen bindes sterkere. Ved hypotermi kan derfor vevene motta mindre oksygen, til tross for normal SaO₂.
- Lavt CO₂-nivå (hypokapni): Når det er lite CO₂ i blodet, reduseres mengden H⁺-ioner og karbaminohemoglobin. Dette fører til økt affinitet mellom hemoglobin og oksygen – en effekt som motsvarer det vi ser i Bohr-effekten.
- Redusert mengde 2,3-DPG: 2,3-difosfoglyserat er et stoff i røde blodceller som reduserer oksygenets binding til hemoglobin. Ved lave nivåer – for eksempel ved lagring av blod – bindes oksygenet sterkere, og kurven forskyves mot venstre.
- Høy pH (alkalose): Økt pH reduserer antallet frie H⁺-ioner i blodet. Dette fører til at hemoglobinet lettere beholder sitt oksygen, og vanskeligere avgir det i vev med lavt PO₂.
Til sammen fører disse faktorene til at hemoglobin avgir mindre oksygen enn normalt, noe som kan være særlig problematisk under forhold som økt vevsmetabolisme, fysisk aktivitet eller sjokk.
Høyreforskyvning – redusert affinitet for oksygen
Når kurven forskyves mot høyre, betyr det at hemoglobin har redusert affinitet for oksygen. Ved samme PO₂-nivå vil metningsgraden (SaO₂) være lavere enn normalt, fordi oksygenet slippes lettere. Dette er en gunstig fysiologisk tilpasning i situasjoner hvor vev trenger mer oksygen, som ved fysisk aktivitet eller feber.
Høyreforskyvning skyldes:
- Økt temperatur: Høy kroppstemperatur, som ved feber eller anstrengelse, destabiliserer den oksygenbundne R-formen av hemoglobin, og favoriserer den deoksygenerte T-formen. Dette letter oksygenfrigjøringen i arbeidende vev.
- Høyt CO₂-nivå (hyperkapni): Når CO₂-nivået stiger, dannes det mer karbonsyre (H₂CO₃), som dissosierer til H⁺ og bikarbonat (HCO₃⁻). Dette senker pH og fører til høyreforskyvning via Bohr-effekten – en viktig mekanisme for å øke oksygentilførselen i vev med høyt CO₂-produksjon.
- Økt 2,3-DPG: Høye nivåer av 2,3-difosfoglyserat, som sees ved anemi, høydeopphold eller kronisk hypoksi, stabiliserer T-formen av hemoglobin og reduserer oksygenets bindingsevne. Dette gjør at oksygen slippes lettere der det trengs mest.
- Lav pH (acidose): Surere miljøer (flere H⁺-ioner) svekker bindingen mellom hemoglobin og oksygen. Dette gjør at hemoglobin lettere gir fra seg oksygen i vev som er metabolske aktive eller iskemiske.
Klinisk betydning
Disse forskyvningene i dissosiasjonskurven har stor betydning i klinikken. For eksempel vil en venstreforskyvning redusere oksygentilførselen til vev – noe som er uheldig ved sepsis, hypotermi eller blodoverføringer med lagret blod. Høyreforskyvning, derimot, er ofte en gunstig tilpasning og kan være livsviktig i stressituasjoner, som ved fysisk aktivitet, febersykdom, acidose eller anemi.
Derfor er det viktig å vurdere ikke bare PaO₂ og SaO₂, men også de underliggende forholdene som påvirker hemoglobinets oksygenbindingskurve – spesielt ved tolking av oksygeneringsstatus og respons på oksygentilførsel.
Bohr-effekten – et smart oksygenbytte
Kroppen har en elegant mekanisme for å sørge for at oksygen slippes akkurat der det trengs mest – nemlig i vev som arbeider hardt, som muskler under fysisk aktivitet. Denne mekanismen kalles Bohr-effekten.
Når musklene arbeider, produserer de både karbondioksid (CO₂) og melkesyre (laktat).
Dette senker pH i det lokale vevet og øker CO₂-trykket.
Hemoglobin reagerer på dette ved å slippe lettere taket på oksygen, altså redusere sin affinitet.
Dette gjør at mer oksygen frigis akkurat der det er størst behov.
Mekanismen bak dette er at H⁺-ioner og CO₂ binder seg til hemoglobinets aminosyrer og endrer strukturen, slik at hemoglobinet holder mindre godt på O₂.
Bohr-effekten fører altså til en høyreforskyvning av oksyhemoglobinets dissosiasjonskurve, noe som betyr at hemoglobinet avgir oksygen lettere ved samme oksygentrykk. På den måten er effekten en fysiologisk tilpasning til økt metabolsk aktivitet – oksygenet leveres der det trengs, uten at kroppen må øke sirkulasjonen dramatisk.
2,3-DPG – kroppens langsiktige finjustering
I tillegg til Bohr-effekten finnes det en annen viktig faktor som påvirker hemoglobinets oksygengrep: 2,3-difosfoglyserat (2,3-DPG).
Dette er et stoff som produseres i røde blodceller og binder seg til hemoglobin.
Når 2,3-DPG-nivået øker, reduseres hemoglobinets affinitet for oksygen, som igjen gjør det lettere å frigjøre oksygen i vevet.
Dette gir også en høyreforskyvning av dissosiasjonskurven.
Økt 2,3-DPG-produksjon skjer ved kronisk hypoksi, som ved langvarig høydeopphold, kronisk lungesykdom eller anemi.
I motsetning til Bohr-effekten, som virker umiddelbart, er dette en mer langsom tilpasning – det tar timer til dager før nivåene justeres.
Klinisk sett er dette viktig fordi 2,3-DPG brytes ned i lagret blod. Transfusjoner med gammelt blod kan derfor gi redusert oksygentilførsel til vev, selv om blodet har normal hemoglobinkonsentrasjon. Dette er et viktig hensyn ved større blodtransfusjoner.
Karbonmonoksidforgiftning – det usynlige oksygenproblemet
Karbonmonoksid (CO) er en gass uten lukt, farge eller smak – men med hundre ganger høyere affinitet for hemoglobin enn oksygen. Når CO binder seg til hemoglobin, dannes karboksyhemoglobin, som ikke bare blokkerer O₂-binding, men også gjør at oksygen som allerede er bundet, ikke slippes løs til vevet.
Dette gir en dobbel effekt: redusert oksygeninnhold i blodet og dårligere oksygenavgivelse.
På dissosiasjonskurven ser vi dette som en venstreforskyvning.
Resultatet er alvorlig hypoksi – spesielt farlig for hjerne og hjerte.
Behandlingen er rask tilførsel av rent oksygen (80–100 %) via maske eller trykkammer. Dette fortrenger CO fra hemoglobinet og gjenoppretter oksygentransporten.
Cyanose – det synlige tegnet på oksygenmangel
Cyanose betyr blålig misfarging av hud og slimhinner og skyldes økt mengde deoksygenert hemoglobin i kapillærene. Man skiller mellom:
- Sentral cyanose, som skyldes lav oksygenmetning i hele kroppen – vanlig ved lunge- og hjertesykdom.
- Perifer cyanose, som er et resultat av redusert sirkulasjon i ytterledd, som fingre og tær.
For at cyanose skal bli synlig, må mengden deoksy-Hb være minst 3–5 g/100 ml blod. Dette forklarer hvorfor cyanose er sjeldent ved anemi, hvor total Hb er lav, og vanligere ved polycytemi, hvor det er mer Hb tilgjengelig for deoksygenering.
Transport av CO₂ – fra vev til lunger
CO₂ er et avfallsstoff som må fraktes fra cellene og ut via lungene. Kroppen bruker tre ulike transportformer for å løse dette:
- Løst i plasma (ca. 10 %)
CO₂ er mye mer løselig i blod enn oksygen og kan derfor fraktes direkte oppløst i blodet. Likevel har denne formen begrenset kapasitet. - Bundet til proteiner (ca. 20 %)
CO₂ binder seg til aminogrupper på hemoglobin og andre proteiner og danner karbaminoforbindelser. Deoksy-Hb binder mer CO₂ enn oksy-Hb – dette kalles Haldane-effekten. - Omdannet til bikarbonat (HCO₃⁻) (ca. 70 %)
Dette er den viktigste transportformen. I erytrocyttene omdannes CO₂ og H₂O til H₂CO₃ (karbonsyre) ved hjelp av enzymet karbonsyreanhydrase, som deretter dissosierer til H⁺ og HCO₃⁻. Bikarbonatet transporteres ut av erytrocyttene i bytte mot kloridioner (Cl⁻) – dette kalles kloridskiftet.
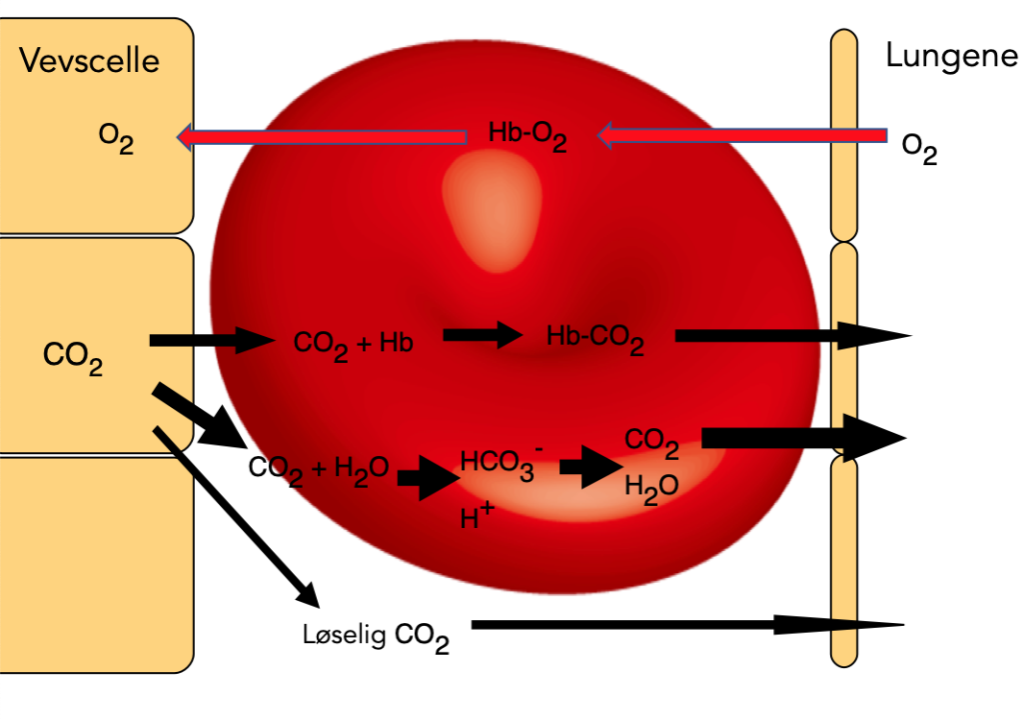
Haldane-effekten – oksygen inn, CO₂ ut
Haldane-effekten beskriver hvordan oksygenbinding til hemoglobin reduserer dets evne til å binde CO₂ og H⁺. Dette er en smart mekanisme som gjør at:
- I lungene, hvor O₂ trykk og metning er høy, vil CO₂ lettere slippes – hemoglobin gir slipp på både CO₂ og H⁺.
- I vevet, hvor O₂ trykk og metning er lav, vil hemoglobin lettere binde både CO₂ og H⁺, og dermed hjelpe til med transporten.
Dette er altså det motsatte av Bohr-effekten, som handler om hvordan CO₂ påvirker O₂-binding.
CO₂-dissosiasjonskurven – stabil og lineær
I motsetning til oksygenkurven, er CO₂-kurven mer lineær og bratt. Det betyr at CO₂-transport ikke er like følsom for små trykkendringer. Likevel påvirkes den av O₂-innholdet:
- Når hemoglobin er deoksygenert (som i vev), bindes mer CO₂.
- Når hemoglobin er mettet med O₂ (som i lunger), frigjøres mer CO₂.
Denne venstre- og høyreforskyvningen i CO₂-kurven styres av Haldane-effekten og gjør at CO₂ kan fraktes effektivt én vei – fra celler til lunger – akkurat som oksygen går motsatt vei.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Interaktiv pasientcase: Kristian, 24
❓ Test deg selv
Obs, tomt! Kommer etterhvert <3