Ventilasjons–perfusjonsforholdet (V/Q-ratio)
Definisjon og betydning
Ventilasjons–perfusjonsforholdet, ofte omtalt som V/Q-forholdet, beskriver balansen mellom ventilasjonen (V), altså tilførselen av luft til alveolene, og perfusjonen (Q), blodstrømmen gjennom de tilhørende kapillærene.
Dette forholdet er helt avgjørende for effektiv gassutveksling i lungene.
For at oksygen (O₂) skal kunne diffundere inn i blodet og karbondioksid (CO₂) skal fjernes, må det være en viss balanse mellom mengden luft som når alveolene og mengden blod som strømmer gjennom de omkringliggende kapillærene.
Dersom denne balansen forstyrres, vil det ha direkte konsekvenser for både oksygenering og CO₂-eliminasjon.
Man kan sammenligne ventilasjon og perfusjon med et system der fargestoff (O₂) tilføres via luftstrømmen, mens vannstrømmen (blod) fører det bort.
Hvor konsentrert fargen blir, avhenger av forholdet mellom tilførselen (V) og strømmen (Q).
På samme måte vil alveolens innhold av oksygen og CO₂ bestemmes av V/Q-forholdet.
Mekanismen bak V/Q-forholdet
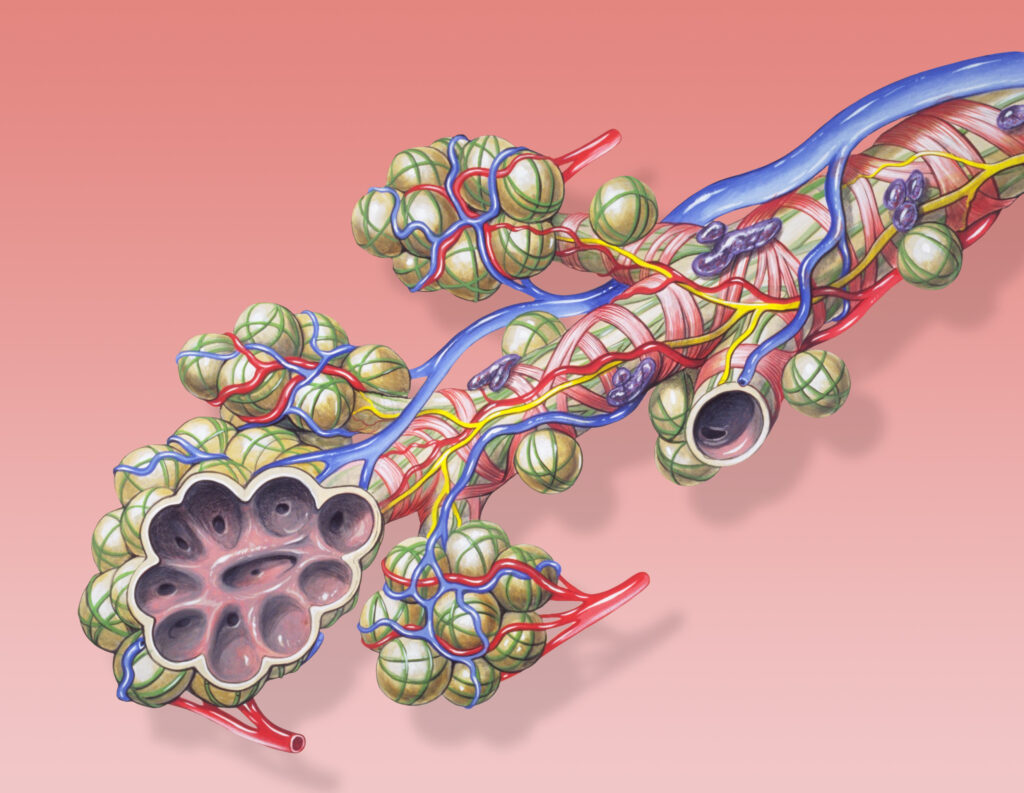
Hver funksjonell enhet i lungene – en alveole med tilhørende kapillærnett – fungerer som en gassutvekslingsenhet.
I denne enheten må både luft og blod være til stede i riktige mengder for at gassutveksling skal fungere optimalt.
Dersom ventilasjon foregår uten tilstrekkelig blodtilførsel, eller omvendt, blir resultatet enten ineffektiv oksygentilførsel eller redusert CO₂-fjerning.
Det er altså ikke tilstrekkelig med bare luft eller bare blod – det er forholdet mellom de to som avgjør hvor godt lungene fungerer som gassutvekslingsorgan.
Optimal gassutveksling og V/Q-mismatch
Den mest effektive gassutvekslingen skjer når ventilasjon og perfusjon er like store, altså når V/Q = 1.
I praksis varierer dette noe i ulike deler av lungene, og det gjennomsnittlige V/Q-forholdet hos friske mennesker ligger rundt 0,8.
Dette skyldes at perfusjonen (Q) normalt er noe større enn ventilasjonen (V). Typiske verdier er:
- 💨 Ventilasjon (V): ca. 4 liter per minutt
- 🩸 Perfusjon (Q): ca. 5 liter per minutt
Dette representerer en tilstand der ventilasjon og blodgjennomstrømning er godt matchet, og dermed gir optimal oksygenering og karbondioksidfjerning.
Når denne balansen forstyrres, oppstår det vi kaller en V/Q-mismatch – altså en ubalanse mellom ventilasjon og perfusjon.
Dette deles gjerne inn i to hovedtyper:
1. Høyt V/Q-forhold – “dødromsventilasjon”
Her er ventilasjonen høy i forhold til perfusjonen.
Dette betyr at det kommer inn rikelig med luft i alveolen, men det er lite eller ingen blodstrøm til området.
Resultatet er at luft ventileres, men det skjer ingen effektiv gassutveksling, fordi det ikke finnes nok blod til å ta opp oksygenet eller avgi CO₂.
Slike høye V/Q-enheter oppstår typisk ved:
- Lungeemboli (blodpropp blokkerer blodstrømmen)
- Pulmonal hypertensjon
Konsekvensen blir økt ventilasjonsarbeid, reduksjon i CO₂-eliminasjon og ineffektiv oksygenutnyttelse, til tross for at luft når alveolene.
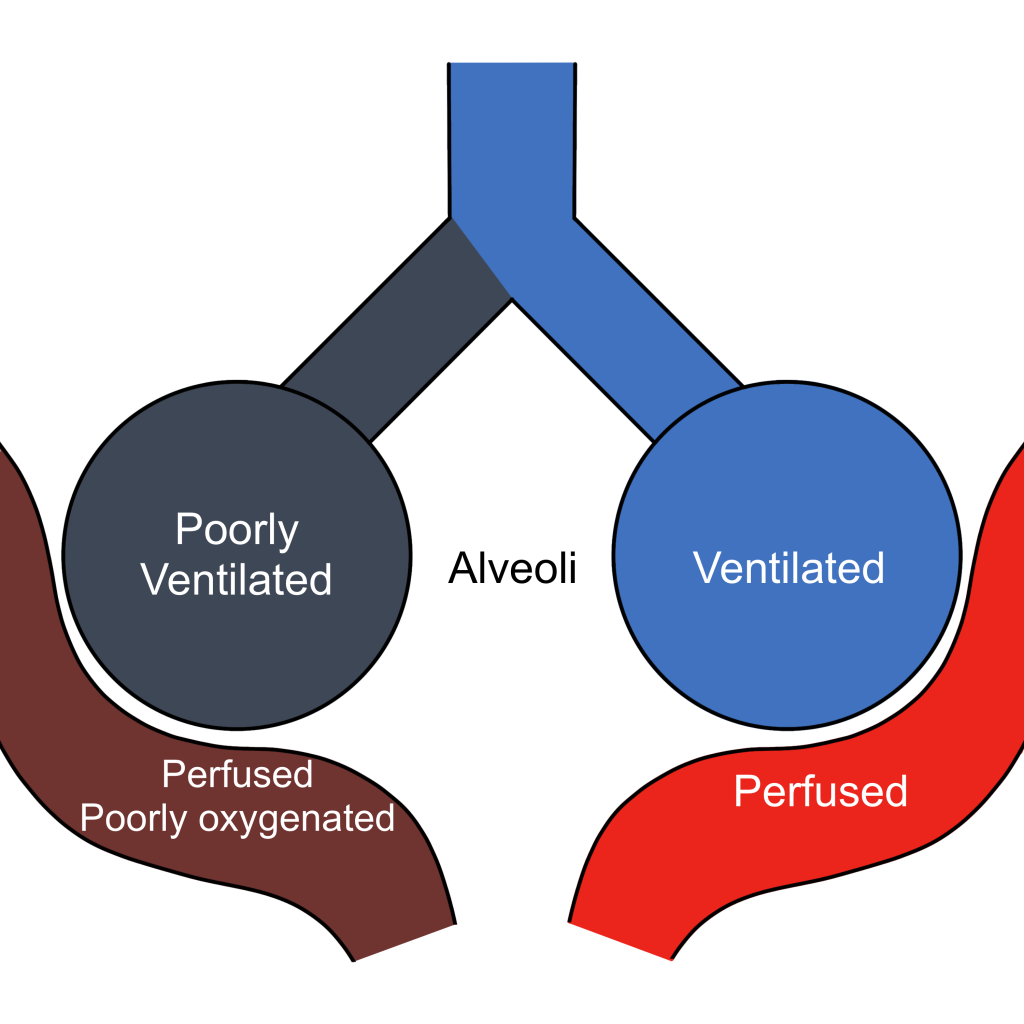
2. Lavt V/Q-forhold – “funksjonell shunt”
I den andre enden av skalaen har vi en situasjon hvor perfusjonen er normal, men ventilasjonen er redusert.
Her passerer blod gjennom kapillærene rundt alveoler som enten er dårlig ventilert eller ikke ventilert i det hele tatt.
Dette fører til utilstrekkelig oksygenering av blodet, og vi får en tilstand som kan sammenlignes med en shunt – der blodet går “forbi” lungen uten å bli tilført oksygen.
Lav V/Q forekommer ved:
- Astma
- KOLS
- Pneumoni
- Atelektase (sammenfalte lungeavsnitt)
Konsekvensen er ofte hypoksemi – lav oksygenmetning i blodet – som kan være vanskelig å korrigere selv med oksygentilførsel.
Ulike V/Q-enheter og deres konsekvenser
For å forstå hvordan ventilasjon og perfusjon påvirker gassinnholdet i alveolene, må vi se nærmere på hva som skjer i situasjoner hvor forholdet mellom de to ikke er ideelt.
Høye og lave V/Q-enheter har nemlig svært ulike konsekvenser for alveolær gassammensetning.
I en høy V/Q-enhet – som ved områder med god ventilasjon men lite perfusjon – vil det samle seg mer oksygen i alveolen enn det blodstrømmen kan hente med seg. Resultatet er at det alveolære partialtrykket av oksygen (P_AO₂) blir unormalt høyt, mens partialtrykket av karbondioksid (P_ACO₂) blir lavt.
Dette skjer fordi det tilføres lite CO₂ med blodet, samtidig som det som måtte være til stede, effektivt ventileres ut.
Et slikt område omtales gjerne som dødromsventilasjon, fordi luften som kommer inn i alveolen ikke deltar i effektiv gassutveksling.
I en lav V/Q-enhet, derimot, er blodstrømmen god, men ventilasjonen begrenset. I slike områder vil alveolene motta lite oksygen, samtidig som de mottar en normal mengde CO₂ fra blodet.
Resultatet blir lavt P_AO₂ og høyt P_ACO₂, siden ventilasjonen ikke klarer å fjerne det CO₂ som strømmer inn, og det tilføres utilstrekkelig oksygen. Disse områdene fungerer funksjonelt som shunter – blodet passerer alveolene uten å bli tilstrekkelig oksygenert.
Effekter på blodets sammensetning
Fordi ulike V/Q-enheter produserer alveolær luft med ulikt gassinnhold, vil også det kapillære blodet som forlater de enkelte enhetene ha forskjellig innhold av oksygen og karbondioksid.
Blod fra høye V/Q-enheter vil ha en oksygenmetning som ligger nær det normale. Problemet er at disse områdene som regel representerer en liten del av den totale perfusjonen, og kan dermed ikke kompensere for manglende oksygenering andre steder.
Blod fra lave V/Q-enheter vil derimot ha betydelig lavere oksygenmetning og høyere CO₂-innhold.
Dersom slike områder utgjør en stor andel av lungens kapillærnett, som ved mange lungesykdommer, vil dette redusere den totale oksygeneringen av blodet som returnerer til venstre hjertehalvdel.
V/Q-heterogenitet og lungesykdom
I en frisk lunge finnes det alltid en viss spredning i V/Q-forholdet mellom ulike områder.
Denne fysiologiske V/Q-heterogeniteten skyldes blant annet gravitasjonens innvirkning på ventilasjon og perfusjon, og den er vanligvis ikke problematisk.
Ved lungesykdom blir derimot forskjellene mellom ulike lungeavsnitt mye større. Noen områder får for mye luft i forhold til blod, mens andre får for mye blod i forhold til luft.
Dette kalles økt V/Q-heterogenitet, og er en viktig årsak til redusert gassutveksling.
Luftveissykdommer som astma, KOLS og atelektase påvirker først og fremst ventilasjonen.
Ved astma og KOLS er luftstrømmen ujevn på grunn av bronkokonstriksjon, slim og inflammasjon.
I atelektase kollapser alveoler helt, og får ingen ventilasjon – men perfusjonen kan fortsatt være bevart.
Sykdommer i lungeparenkym eller det pulmonale karsystemet fører til ujevn fordeling av blod.
Ved lungeemboli blokkeres blodstrømmen i enkelte områder, mens ventilasjonen fortsetter som normalt.
Ved pulmonal hypertensjon øker trykket i det lille kretsløpet, noe som fører til omdirigering av blodstrømmen.
Lungeødem kan også forstyrre både ventilasjon og perfusjon ved væskeansamling i vevet.
Konsekvenser av V/Q-heterogenitet
Når ulike områder av lungene har svært forskjellige V/Q-forhold, vil den samlede gassutvekslingen i lungene bli mindre effektiv. Dette gir en rekke konsekvenser:
- Den totale oksygentransporten reduseres, og blodet som returnerer til hjertet vil ha lavere oksygenmetning (PaO₂)
- CO₂-eliminasjonen blir mindre effektiv, og pasienten må ofte kompensere med økt ventilasjonsarbeid
- Respirasjonsarbeidet øker, noe som gir økt energibehov og kan føre til respirasjonssvikt ved alvorlig sykdom
- Hypoksemien som oppstår som følge av V/Q-mismatch kan være vanskelig å korrigere med oksygentilførsel alene, spesielt dersom det foreligger en betydelig andel lave V/Q-enheter
Klinisk betydning: V/Q-mismatch som årsak til hypoksemi
V/Q-ubalanse er den vanligste årsaken til hypoksemi ved lungesykdom.
Den utgjør én av fire klassiske mekanismer bak lavt arterielt oksygentrykk (PaO₂):
- V/Q-mismatch – ujevn fordeling av luft og blod i lungene
- Hypoventilasjon – redusert total ventilasjon gir opphopning av CO₂ og lavere oksygentrykk
- Shunt – blod passerer gjennom lungene uten å bli eksponert for ventilasjon (f.eks. ved pneumoni eller medfødte hjertefeil)
- Diffusjonsdefekt – nedsatt evne til å overføre O₂ fra alveole til kapillær, som ved interstitiell lungesykdom
Av disse er det altså V/Q-mismatch som er vanligst, og derfor en sentral mekanisme å forstå ved vurdering av pasienter med nedsatt oksygenmetning i blodet.
Effekten av V/Q-forholdet på alveolære gassverdier
Forholdet mellom ventilasjon og perfusjon påvirker direkte hvilket nivå av oksygen (O₂) og karbondioksid (CO₂) vi finner i alveolene.
Dette kan tydelig illustreres ved å se på ekstreme V/Q-forhold, fra fullstendig mismatch til perfekt balanse:
- Ved V/Q = 0, altså en shunt, finnes det ingen ventilasjon, men normal blodstrøm.
Blodet passerer da gjennom lungene uten kontakt med frisk luft, og gassverdiene i alveolen speiler det venøse blodet: ca. 40 mmHg O₂ og 45 mmHg CO₂. Slike forhold ses blant annet ved atelektase. - Ved V/Q = 1, som representerer optimal balanse mellom ventilasjon og perfusjon, finner vi normale alveolære gassverdier: ca. 100 mmHg O₂ og 40 mmHg CO₂. Dette er idealtilstanden for gassutveksling.
- Ved V/Q = ∞, altså i det vi kaller dødrom, er det ingen blodstrøm, men normal ventilasjon.
Luften i alveolen forblir da uendret fra den som pustes inn, og får verdier nær atmosfærisk luft: ca. 150 mmHg O₂ og 0 mmHg CO₂. Eksempler finnes ved lungeemboli.
Regionale forskjeller i V/Q-forhold
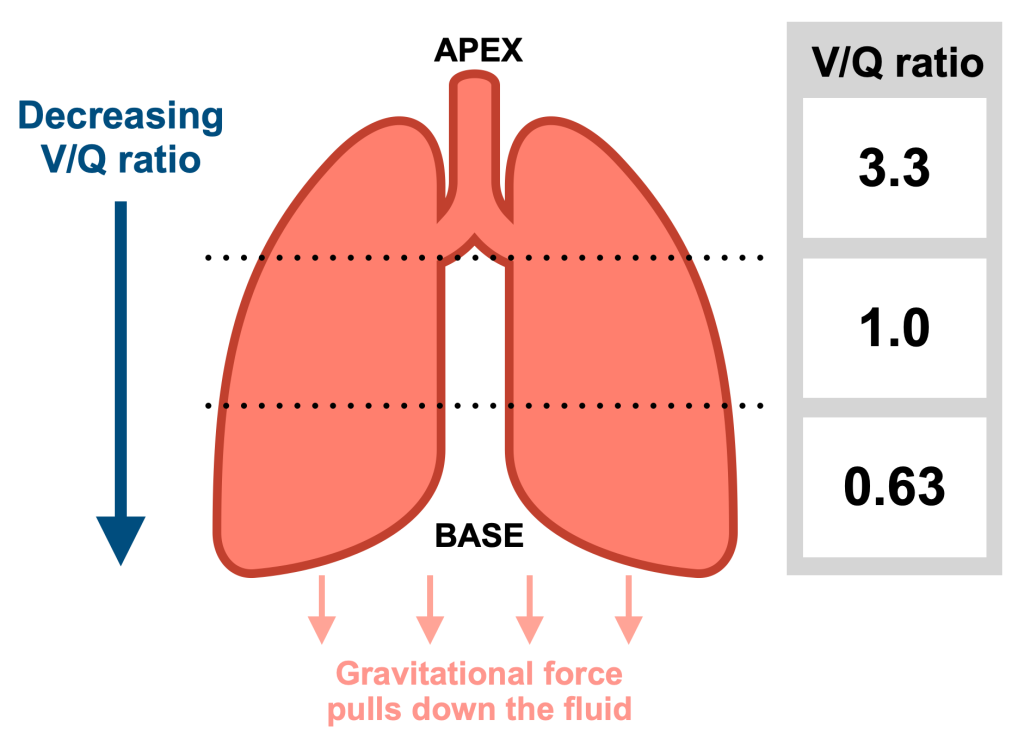
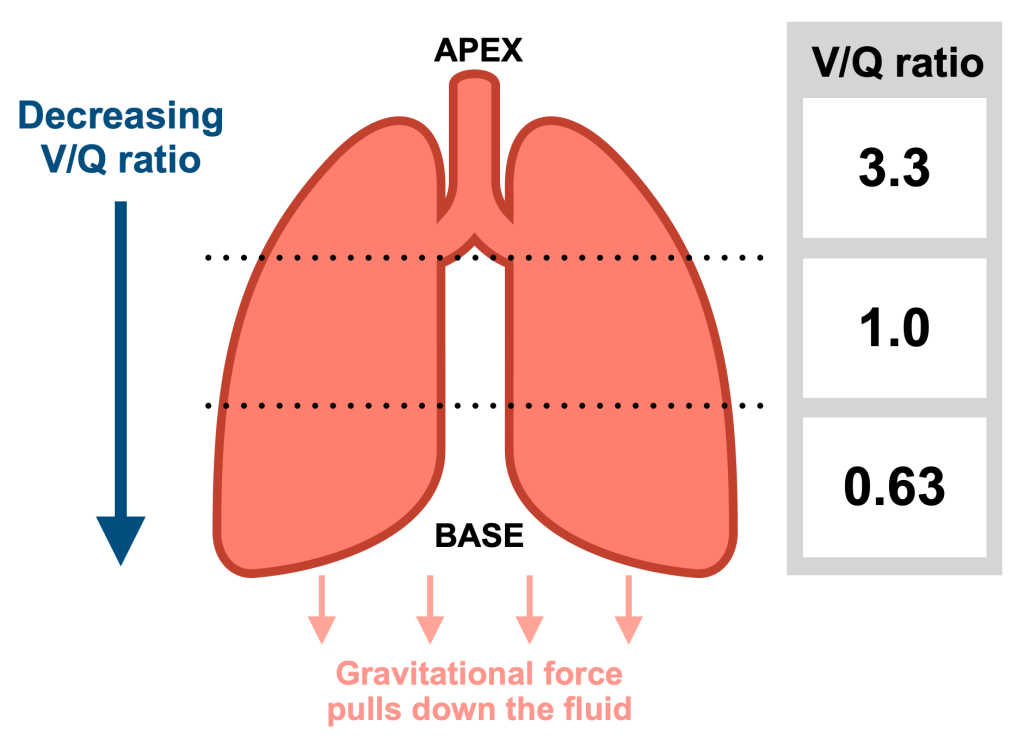
Lungene er ikke homogene. Gravitasjonen spiller en avgjørende rolle i hvordan både ventilasjon og perfusjon fordeles i det stående mennesket. Både luft og blod strømmer lettere til de nedre delene av lungene – altså mot basis – enn til de øvre delene (apex).
Likevel øker perfusjonen mer enn ventilasjonen mot lungens basis. Det betyr at V/Q-forholdet er lavere i basis og høyere i apex. Tallfestet kan dette illustreres slik:
- Apex: V/Q ≈ 3,3
- Høyt O₂-partialtrykk (≈ 130 mmHg)
- Lavt CO₂-partialtrykk (≈ 28 mmHg)
- Basis: V/Q ≈ 0,6
- Lavere O₂-partialtrykk (≈ 89 mmHg)
- Høyere CO₂-partialtrykk (≈ 42 mmHg)
De øvre lungesegmentene er altså bedre ventilert enn perfundert, mens de nedre får mer blod enn luft.
I sum skaper dette en naturlig V/Q-gradient som er viktig å forstå – spesielt ved sykdom.
Kliniske konsekvenser av regional V/Q-forskjell
Ved sykdom som rammer de nedre lungesegmentene – for eksempel pneumoni eller atelektase – vil områder med allerede lav V/Q-ratio få enda dårligere forhold, og gassutvekslingen forverres betraktelig.
Endringer i kroppsstilling påvirker også V/Q-forholdet gjennom gravitasjonens effekt:
- I stående stilling går V/Q-gradienten fra lungens topp til bunn (apex → basis)
- I liggende stilling (ryggleie) forskyves gradienten slik at bakre (dorsale) områder får mest perfusjon
- Ved sideliggende stilling får den nederste (avhengige) lungen mer blodtilførsel, men samtidig ofte redusert ventilasjon på grunn av kompresjon
- Hos pasienter med ensidig lungesykdom kan man utnytte dette ved å legge pasienten med frisk lunge ned, for å maksimere total gassutveksling
- I bukleie (prone position), som brukes ved alvorlig lungesvikt (ARDS), kan man forbedre ventilasjon og perfusjon i tidligere dårlige områder, og dermed øke oksygeneringen
Alder og sykdom øker V/Q-heterogenitet
Selv friske lunger har en viss normal V/Q-heterogenitet, men dette øker med alder og ved lungesykdommer. Årsaken er at både ventilasjon og perfusjon blir mindre jevnt fordelt, noe som skaper større forskjeller i alveolære gassverdier mellom ulike områder av lungen.
Hos eldre skjer dette naturlig som følge av aldringsrelaterte forandringer i lungevev og blodkar. Ved sykdom øker ujevnheten ytterligere – og konsekvensen blir ofte hypoksemi, som er vanskelig å korrigere med oksygen alene.
Man regner med at 95 % av normale V/Q-ratioer ligger innenfor området 0,3 til 2,1. Dersom mange enheter faller utenfor dette området, vil gassutvekslingen bli ineffektiv – og det vil kunne føre til kliniske symptomer.
Alveolær gassligning – beregning av PAO₂
For å kunne si noe presist om forholdene i alveolen, kan man bruke den såkalte alveolære gassligningen. Denne gir oss et estimat på det alveolære oksygentrykket (PAO₂) basert på forholdet mellom:
- Mengden oksygen som tilføres (inspiratorisk oksygentrykk, PIO₂)
- Mengden CO₂ som fjernes (målt som PaCO₂)
- Den respiratoriske kvotienten (R), som i hvile er ca. 0,8
Formelen for PAO₂ er:
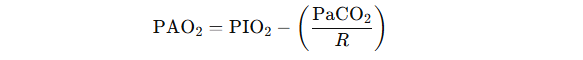
Her representerer PaCO₂ det CO₂ som transporteres tilbake til alveolene og diffunderer ut, og forholdet til R korrigerer for at ikke all CO₂-produksjon tilsvarer O₂-forbruk i et 1:1-forhold.
Klinisk bruk av alveolær gassligning
Ved å bruke gassligningen kan man beregne A-a-gradienten – forskjellen mellom det alveolære og arterielle oksygentrykket (PAO₂ – PaO₂). Dette gir et mål på hvor effektivt oksygen diffunderer fra alveole til blod.
- Normalt: Gradient på 1–2 kPa
- Høyere verdier: Tyder på problemer med diffusjon, shunt eller V/Q-mismatch
- Normale verdier tross lav PaO₂: Tyder på hypoventilasjon som årsak
- Fysisk aktivitet: Økt PAO₂ fordi ventilasjonen stiger
Dette gjør gassligningen til et viktig verktøy i vurdering av hypoksemi – både for å skille mellom ulike årsaker og for å vurdere hvorvidt oksygentilførsel vil ha effekt.
V/Q-heterogenitet og gassutveksling
Selv om enkelte områder av lungene ventileres godt, er det ikke alltid mulig for disse områdene å kompensere for andre deler med dårlig ventilasjon.
En lav V/Q-enhet, altså et område med god blodstrøm, men lite ventilasjon, har en uproporsjonalt stor negativ effekt på blodets oksygeninnhold.
Dette skyldes at redusert ventilasjon i én del av lungen fører til langt større reduksjon i oksygenering, enn det en tilsvarende økning i ventilasjon i en annen del klarer å kompensere for.
Dette fenomenet skyldes flere mekanismer:
For det første spiller oksyhemoglobinets dissosiasjonskurve(les mer om dette på linken) en viktig rolle. Hemoglobin i blodet blir nesten fullstendig mettet allerede ved et oksygentrykk (PAO₂) over 13 kPa.
Det betyr at selv om noen alveoler har svært god ventilasjon og høyt oksygentrykk, vil ikke disse områdene kunne ta opp særlig mer oksygen – hemoglobinet er allerede mettet.
Det finnes med andre ord en metningsgrense som setter et tak på hvor mye oksygen som kan transporteres, uansett hvor god ventilasjonen måtte være.
Videre er det slik at områder med lav V/Q ofte står for en uforholdsmessig stor andel av den totale blodstrømmen.
Dette skyldes at kroppen forsøker å kompensere for dårlig ventilasjon ved å omdirigere blodstrømmen, gjennom en mekanisme kjent som hypoksisk vasokonstriksjon.
Men denne mekanismen er ofte utilstrekkelig, særlig ved lungesykdom.
Resultatet er at en betydelig del av hjertets minuttvolum fortsetter å passere gjennom områder med dårlig ventilasjon og dermed dårlig gassutveksling.
Ved høy blodstrøm gjennom godt ventilerte alveoler kan det i tillegg oppstå en diffusjonsbegrensning.
Det betyr at oksygen ikke rekker å diffundere fullstendig over i blodet før det forlater kapillærene – særlig ved fysisk aktivitet, når kontakttiden mellom alveole og blod blir kortere.
Til slutt oppstår en såkalt shunteffekt i områder med svært lav V/Q.
Her passerer blodet lungekretsløpet uten å ta opp oksygen, omtrent som ved en reell høyre-til-venstre shunt.
Dette blodet blander seg med oksygenrikt blod fra bedre ventilerte områder og «fortynner» det totale oksygeninnholdet i det arterielle blodet.
Konsekvenser av hypoksemi
Når oksygeninnholdet i blodet (PaO₂) reduseres, reduseres også tilførselen av oksygen til kroppens vev og organer. Dersom hypoksemien blir alvorlig og vedvarende, kan det oppstå organsvikt som følge av utilstrekkelig oksygenering, noe vi kjenner som respirasjonssvikt.
Noen pasientgrupper er særlig utsatt. Ved for eksempel aterosklerotisk sykdom, der blodforsyningen til vev allerede er redusert, vil hypoksemi kunne føre til kritisk iskemi, særlig i muskulatur (claudicatio intermittens) eller i hjertet (type 2 hjerteinfarkt). Dette gjør forståelsen av hypoksemiens underliggende mekanismer ekstra viktig i klinisk praksis.
Mekanismer bak hypoksemi
Under normale forhold står de alveolære gassverdiene (PAO₂ og PACO₂) i likevekt med blodets endekapillære verdier. Det vil si at trykkene i alveolene gjenspeiles i blodet som forlater dem – med mindre gassutvekslingen forstyrres. Vi har snakker om dette, men her er en oversikt på de fire hovedmekanismene som kan føre til hypoksemi:
1. Diffusjonsbegrensning
Ved diffusjonsbegrensning reduseres evnen til å overføre oksygen fra alveolene til blodet. Dette kan skyldes fortykket alveolokapillær membran, som ved interstitiell lungesykdom (f.eks. lungefibrose). Her erstattes normal lungevev med bindevev, som gir dårligere gassutveksling.
Problemet blir spesielt tydelig under fysisk aktivitet, når blodet strømmer raskere gjennom kapillærene og oppholdstiden reduseres – noe som gir enda mindre tid for diffusjon.
2. Shunt
En shunt oppstår når blodet passerer gjennom lungene uten kontakt med ventilert alveolært luftrom. Ved en anatomisk shunt, som ved en åpen foramen ovale eller pulmonale AV-malformasjoner, strømmer blodet direkte fra høyre til venstre hjertehalvdel uten å passere gjennom alveolene.
En fysiologisk shunt oppstår når blodet passerer gjennom lungeområder som ikke ventileres, slik som ved atelektase eller pneumoni. I begge tilfeller vil ikke oksygentilskudd ha ønsket effekt, siden det shuntede blodet aldri eksponeres for luft og dermed ikke kan oksygeneres.
3. Hypoventilasjon
Ved hypoventilasjon er det en generell reduksjon i alveolær ventilasjon. Dette fører til opphopning av CO₂ i blodet (hyperkapni), som gjennom alveolær gassligning gir redusert PAO₂. Resultatet er lavere arterielt oksygentrykk (PaO₂).
Hypoventilasjon kan være generell, som ved nevromuskulære sykdommer (f.eks. ALS), opioidoverdoser eller svikt i respirasjonssenteret. Den kan også være regional, der enkelte deler av lungene ventileres dårlig, f.eks. ved thoraxdeformiteter eller alvorlig fedme (obesitas-hypoventilasjonssyndrom).
Kjennetegnet ved hypoventilasjon er at både PaO₂ og PaCO₂ er endret samtidig – typisk lavt oksygentrykk og høyt karbondioksidtrykk.
4. V/Q-mismatch
Den klart vanligste årsaken til hypoksemi ved lungesykdom er V/Q-mismatch – altså en ubalanse mellom ventilasjon og perfusjon. Denne tilstanden gir ujevn gassutveksling i ulike deler av lungene, og oppstår i mange forskjellige sykdommer.
Eksempler inkluderer:
- KOLS, der luftstrømmen er obstruert og visse områder ventileres dårlig
- Lungeemboli, som gir redusert perfusjon til visse områder
- Interstitiell lungesykdom (ILD), som gir både diffusjonsproblemer og lav V/Q
Hypoksisk vasokonstriksjon forsøker å redusere blodstrømmen til de dårlig ventilerte områdene, men denne mekanismen er ofte utilstrekkelig ved sykdom. Resultatet blir at en betydelig del av blodet strømmer gjennom områder med lav V/Q, og oksygeneringen reduseres.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3
❓ Test deg selv
Obs, tomt! Kommer etterhvert <3