Glukose er en essensiell energikilde for mange av kroppens celler, spesielt for hjernen, røde blodceller og nervesystemet. For å opprettholde stabile blodsukkernivåer benytter kroppen seg av to hovedprosesser:
- Glukoneogenese: Syntese av glukose fra ikke-karbohydratkilder som laktat, glyserol og visse aminosyrer. Denne prosessen er spesielt viktig under faste eller lavt karbohydratinntak, når glykogenlagrene er uttømt.
- Glykogenmetabolisme: Lagring og mobilisering av glukose i form av glykogen. Glykogensyntese (glykogenese) refererer til oppbyggingen av glykogen fra glukose, mens glykogennedbrytning (glykogenolyse) er prosessen der glykogen brytes ned tilbake til glukose ved behov.
Disse prosessene samarbeider for å sikre at kroppens celler alltid har tilgang til nødvendig glukose, selv under perioder med faste eller økt energibehov.
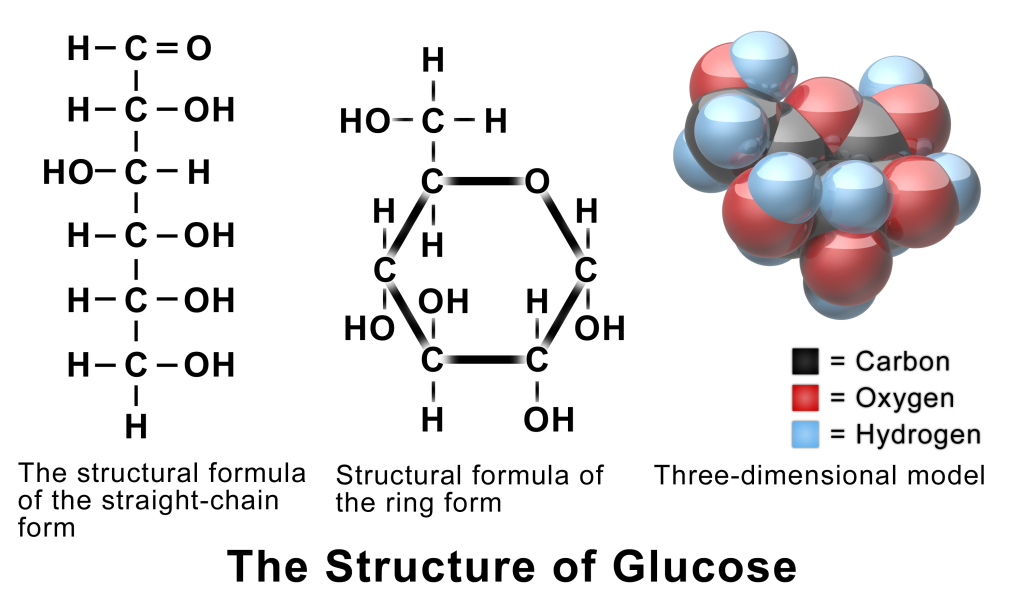
Glukoneogenese
Når kroppen opplever perioder med faste, langvarig fysisk aktivitet eller lavt karbohydratinntak, er det avgjørende at blodsukkeret opprettholdes på et tilstrekkelig nivå. Hjernen, røde blodceller og nervesystemet er spesielt avhengige av glukose som energikilde. Men hva skjer når glukoseinntaket stopper opp, eller glykogenlagrene i leveren begynner å tømmes?
Da aktiveres en fascinerende biokjemisk prosess kalt glukoneogenese, som ordrett betyr «nydanning av glukose». Denne prosessen gjør kroppen i stand til å produsere glukose fra andre molekyler enn karbohydrater, og er livsviktig for å forhindre hypoglykemi under fasteperioder eller lavkarbo-tilstander.
Substrater for glukoneogenese
Glukoneogenesen starter med molekyler som ikke i utgangspunktet er glukose, men som kan omdannes til det. Disse kildene inkluderer:
- Laktat, som dannes i muskler og røde blodceller under anaerobe forhold (uten oksygen).
- Glyserol, som frigjøres når fettvev bryter ned fettmolekyler (triglyserider).
- Glukogene aminosyrer, hovedsakelig alanin, som frigjøres ved nedbrytning av muskelprotein under langvarig faste eller stress.
Gjennom glukoneogenesen blir disse substratene gradvis omdannet tilbake til glukose i leveren (og i mindre grad i nyrene), og deretter frigjort til blodbanen, hvor de gjenoppretter glukosenivået og forsyner kroppens organer med nødvendig energi.
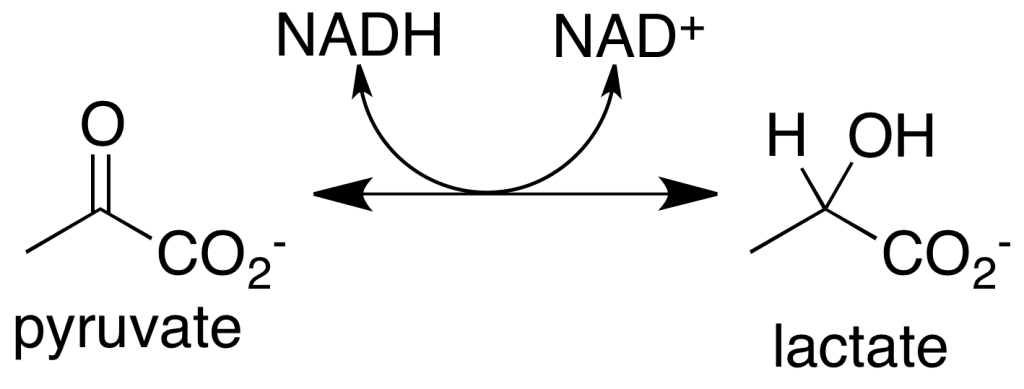
Biokjemiske trinn i glukoneogenese
Glukoneogenese foregår hovedsakelig i leveren, og i noe mindre grad i nyrene. Selv om denne prosessen ofte kalles «det motsatte av glykolyse», er det viktig å huske at glukoneogenese ikke bare er glykolysen baklengs. Enkelte av reaksjonene i glykolysen er irreversible (går kun én vei), og derfor benytter glukoneogenesen egne spesifikke enzymer for å omgå disse irreversiblene trinnene.
De mest sentrale enzymatiske trinnene i glukoneogenesen er:
1. Fra pyruvat til fosfoenolpyruvat (PEP)
Dette steget krever to unike enzymatiske reaksjoner fordi den tilsvarende glykolysereaksjonen er irreversibel. Først omdannes pyruvat til oksaloacetat ved hjelp av enzymet pyruvatkarboksylase i mitokondriene. Deretter omdannes oksaloacetat videre til fosfoenolpyruvat av enzymet PEP-karboksykinase (PEPCK).
2. Fra fruktose-1,6-bisfosfat til fruktose-6-fosfat
Enzymet som omgår det irreversible glykolyseenzymet fosfofruktokinase-1, heter fruktose-1,6-bisfosfatase. Dette er et reguleringspunkt som avgjør om glukoneogenesen skal fortsette videre eller hemmes, avhengig av kroppens energistatus og behov.
3. Fra glukose-6-fosfat til glukose
Til slutt må glukose-6-fosfat omdannes til fri glukose som kan forlate levercellen og entre blodbanen. Dette skjer ved hjelp av enzymet glukose-6-fosfatase, som kun finnes i lever og nyrer. Muskelceller mangler dette enzymet, og kan derfor ikke frigjøre fri glukose til blodet.
Disse spesialiserte enzymatiske trinnene sikrer at glukoneogenese effektivt produserer glukose uten å kollidere med glykolysen, noe som ville ført til energitap og ineffektiv metabolisme.
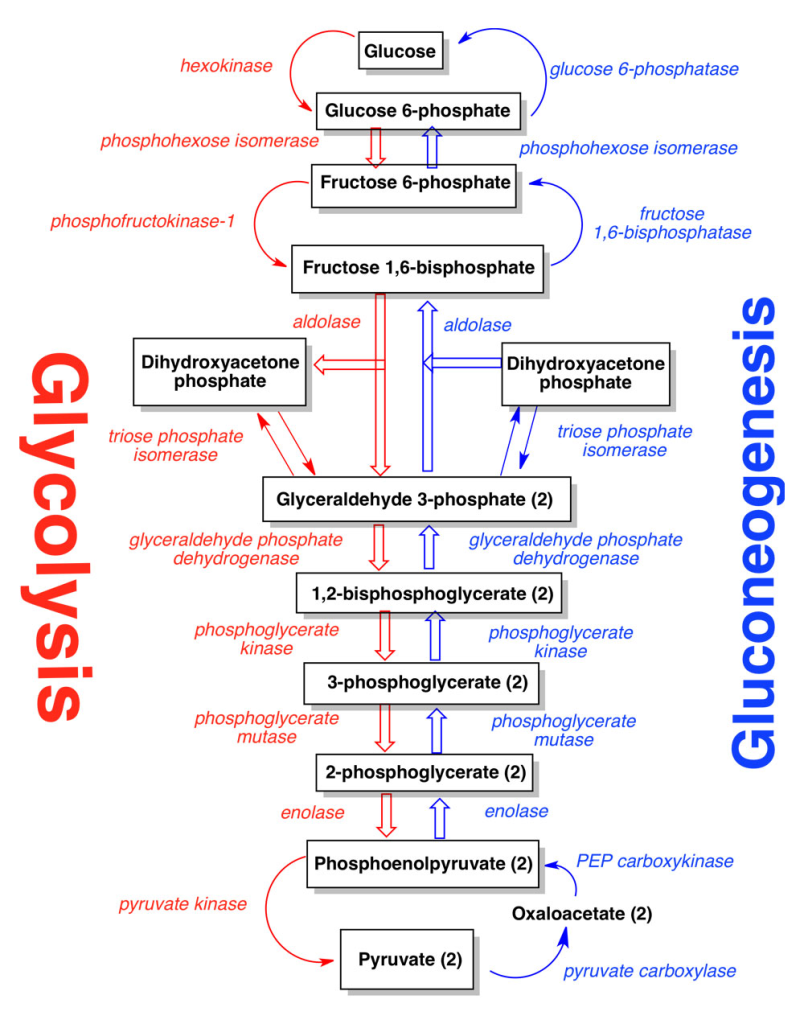
De irreversible enzymene i glykolysen – og hvordan glukoneogenesen omgår dem
For å forstå glukoneogenesen fullt ut, må vi kjenne til noen avgjørende steg i glykolysen som er irreversibel. Disse enzymatiske reaksjonene er ensrettede på grunn av at de involverer store energiforandringer som gjør at de ikke enkelt kan reverseres direkte.
Nettopp derfor må glukoneogenesen ta spesifikke, energikrevende omveier for å omgå disse punktene. De tre viktigste irreversible enzymene i glykolysen er:
1. Heksokinase (glukokinase i lever)
Det aller første steget i glykolysen katalyseres av enzymet heksokinase (eller glukokinase i leveren).
Dette enzymet omdanner glukose til glukose-6-fosfat ved å bruke ATP. Ved denne reaksjonen overføres en fosfatgruppe fra ATP til glukose, og det dannes ADP. Reaksjonen er irreversibel, fordi den innebærer et stort energitap – energien i ATP går direkte over til glukosemolekylet.
Dette irreversible steget er svært viktig for cellen fordi det «fanger» glukose inne i cellen, da glukose-6-fosfat ikke lenger kan diffundere ut igjen over cellemembranen. Men dette skaper samtidig en utfordring for glukoneogenesen: hvis kroppen skal lage ny glukose, må glukose-6-fosfat omdannes tilbake til fri glukose.
For å løse dette problemet har leveren og nyrene et spesielt enzym kalt glukose-6-fosfatase.
Dette enzymet finnes i membranen til det endoplasmatiske retikkelet i lever- og nyreceller, og katalyserer omdannelsen av glukose-6-fosfat tilbake til fri glukose. Fri glukose kan deretter transporteres ut i blodet og bidra til å opprettholde blodsukkernivået under faste. Muskler og hjernen mangler dette enzymet, og kan derfor ikke frigjøre glukose til blodbanen.
2. Fosfofruktokinase-1 (PFK-1)
Det andre avgjørende irreversible steget i glykolysen involverer enzymet fosfofruktokinase-1 (PFK-1).
Dette enzymet omdanner fruktose-6-fosfat til fruktose-1,6-bisfosfat, ved hjelp av nok et ATP-molekyl.
Denne reaksjonen representerer det viktigste reguleringspunktet i glykolysen – «point of no return«.
Når denne reaksjonen først har skjedd, er cellen irreversibelt på vei mot energiproduksjon fra glukose.
For glukoneogenese må også dette steget reverseres, noe som ikke kan skje direkte via PFK-1 fordi reaksjonen er sterkt energimessig ugunstig i motsatt retning.
Derfor finnes det et eget enzym som heter fruktose-1,6-bisfosfatase.
Dette enzymet gjør at reaksjonen kan gå motsatt vei ved å hydrolysere (spalte) fosfatgruppen bort fra fruktose-1,6-bisfosfat, slik at det dannes fruktose-6-fosfat uten at ATP dannes tilbake.
Reguleringen av disse to enzymene – PFK-1 og fruktose-1,6-bisfosfatase – er svært nøye styrt av cellens energinivå (AMP, ATP) og fruktose-2,6-bisfosfat, et viktig reguleringsmolekyl som produseres i respons til hormoner som insulin og glukagon. På denne måten sikres det at glykolyse og glukoneogenese aldri er aktive samtidig, noe som ville sløst bort verdifulle energiressurser.
3. Pyruvatkinase
Det siste irreversible steget i glykolysen katalyseres av enzymet pyruvatkinase. Dette enzymet omdanner fosfoenolpyruvat (PEP) til pyruvat, samtidig som det produserer ATP.
Fordi reaksjonen gir en stor frigjøring av energi, kan heller ikke dette trinnet enkelt reverseres. Glukoneogenesen må derfor bruke en kompleks og energikrevende omvei for å gå motsatt vei fra pyruvat tilbake til PEP:
Først må pyruvat transporteres inn i mitokondriet, hvor enzymet pyruvatkarboksylase omdanner pyruvat til oksaloacetat.
Denne reaksjonen krever energi (ATP), karbondioksid (CO₂ fra bikarbonat), og kofaktoren biotin.
Oksaloacetat kan ikke transporteres direkte ut av mitokondriet, og blir derfor omdannet til malat (via malat-dehydrogenase).
Malat frakter dermed nødvendig NADH (reduksjonskraft) fra mitokondriet ut i cytosol.
I cytosol omdannes malat tilbake til oksaloacetat samtidig som NADH gjendannes, noe som er helt nødvendig for senere trinn i glukoneogenesen.
Til slutt katalyserer enzymet fosfoenolpyruvat karboksykinase (PEPCK) den energikrevende reaksjonen hvor oksaloacetat omdannes til PEP.
Dette steget krever energi i form av GTP, og CO₂ frigjøres.
Dermed har glukoneogenesen klart å omgå det irreversible siste trinnet i glykolysen – men til prisen av et betydelig energiforbruk.
Regulering av glukoneogenese
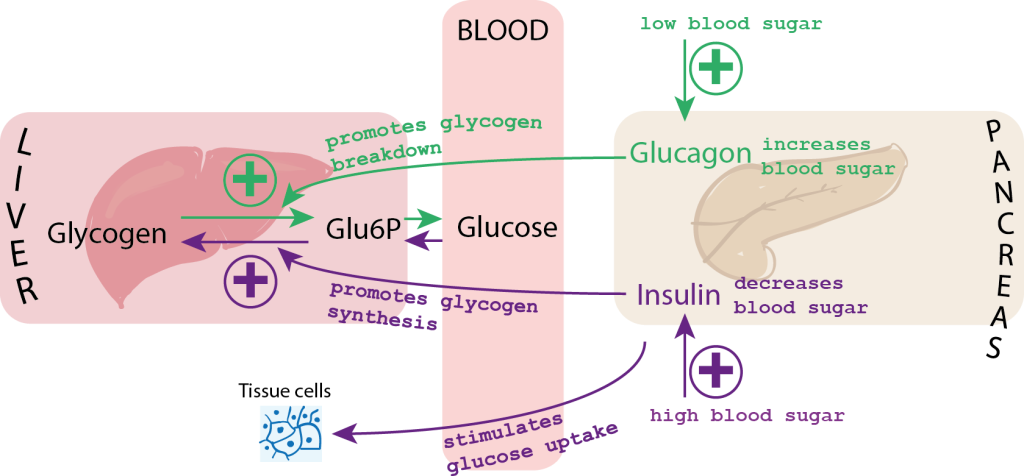
Glukoneogenesen reguleres strengt, hovedsakelig gjennom hormonelle signaler som gjenspeiler kroppens energistatus.
Når blodsukkeret synker, slik det gjør under faste, skilles hormonet glukagon ut fra bukspyttkjertelen. Glukagon stimulerer flere trinn i glukoneogenesen, spesielt ved å øke nivået av enzymet PEPCK, og ved å aktivere fruktose-1,6-bisfosfatase.
På den andre siden, etter et karbohydratrikt måltid, stiger blodsukkeret, og kroppen skiller ut hormonet insulin.
Insulin hemmer glukoneogenesen, både ved å redusere mengden av nøkkelenzymer som PEPCK og ved å aktivere glykolysens enzymer. Denne balanserte reguleringen mellom glukagon og insulin sørger for at kroppen kun produserer glukose når det er nødvendig, og hindrer unødvendig energibruk når blodsukkeret er høyt.
Kort sagt sikrer reguleringen at glukoneogenesen fungerer effektivt som kroppens beredskapssystem, klar til å forsyne viktige organer med glukose når behovet oppstår.
Regulering via PFK2 og fruktose-2,6-bisfosfat (F-2,6-BP)
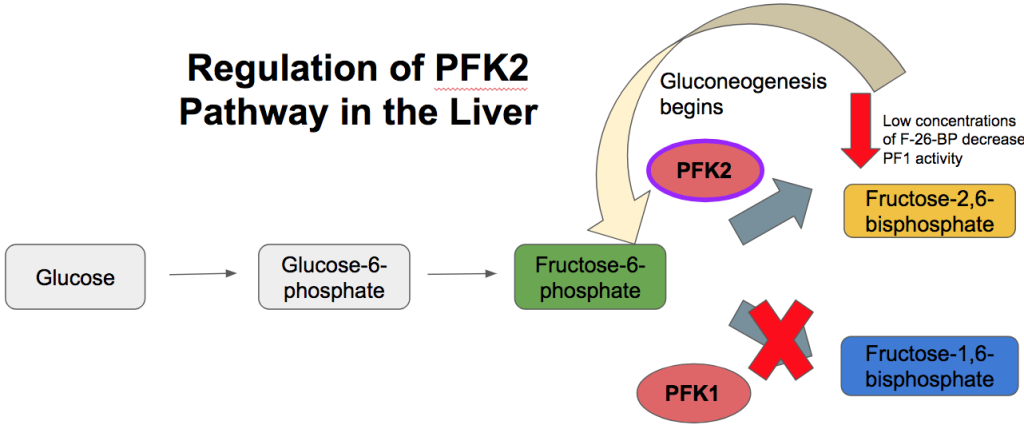
En sentral mekanisme kroppen bruker for å regulere balansen mellom glykolyse (glukosenedbrytning) og glukoneogenese (glukoseproduksjon), involverer enzymet fosfofruktokinase-2 (PFK2). Dette enzymet har en unik dobbeltfunksjon: det kan både produsere og bryte ned molekylet fruktose-2,6-bisfosfat (F-2,6-BP).
Fruktose-2,6-bisfosfat er en svært potent regulator som kontrollerer aktivitetene til nøkkelenzymene i glykolyse og glukoneogenese, nemlig:
- Fosfofruktokinase-1 (PFK1), det viktigste regulerende enzymet i glykolysen.
- Fruktose-1,6-bisfosfatase, et nøkkelenzym i glukoneogenesen.
Når blodsukkernivået er høyt (f.eks. etter et karbohydratrikt måltid), øker konsentrasjonen av F-2,6-BP. Dette aktiverer PFK1 og stimulerer glykolysen, samtidig som det hemmer fruktose-1,6-bisfosfatase og dermed hindrer glukoneogenese.
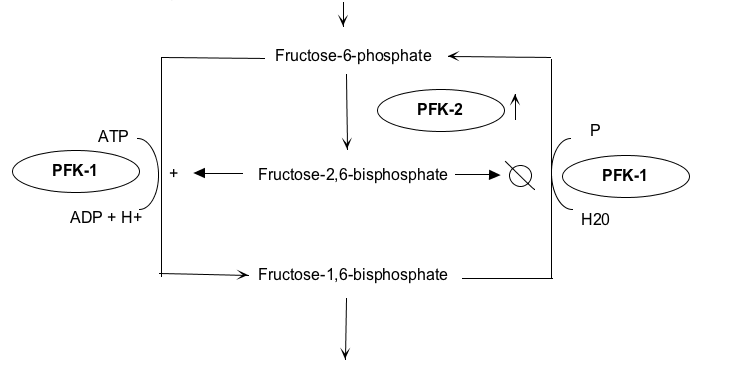
Når blodsukkeret derimot synker (under faste), vil hormonet glukagon føre til fosforylering og aktivering av enzymet PFK2 sin nedbrytningsfunksjon. Dette resulterer i en reduksjon av F-2,6-BP. Når nivået av F-2,6-BP reduseres, avtar aktiviteten til PFK1, og glykolysen bremses kraftig ned. Samtidig fjernes hemmingen av fruktose-1,6-bisfosfatase, noe som åpner døren for glukoneogenese.
Dette er en måte kroppen sørger for at glykolyse og glukoneogenese ikke skjer samtidig og hindrer unødvendig energiforbruk.
Regulering av glukoneogenese – kortsiktig vs. langsiktig
Glukoneogenesen styres av både hormonelle signaler og celleinterne energinivåer, og noen ganger trekker disse i ulike retninger – alt etter tidsperspektiv og metabolsk behov.
Tidlig i sult eller lavt energinivå, stiger AMP-nivået i cellene.
Dette signaliserer at cellen mangler energi, og aktiverer blant annet AMPK (AMP-activated protein kinase).
→ AMP hemmer glukoneogenese, fordi prosessen bruker mye ATP – noe cellen da ikke har råd til å bruke.
Ved vedvarende faste, dominerer hormonelle signaler fra glukagon og kortisol. Disse hormonene reduserer nivået av fruktose-2,6-bisfosfat, som fører til aktivering av fruktose-1,6-bisfosfatase og dermed stimulerer glukoneogenese.
→ Kroppen prioriterer da å opprettholde blodsukkeret, selv om det koster energi.
🧠 Kort oppsummert:
- AMP hemmer glukoneogenese (kort sikt, lavt energinivå)
- Glukagon og lav F2,6-BP stimulerer glukoneogenese (lang sikt, blodsukkerprioritet)
Dette samspillet sikrer at kroppen balanserer energibehovet med behovet for blodsukkerstabilitet, avhengig av situasjon og varighet.
Glykogenmetabolisme
I kroppen vår eksisterer glukose ikke bare som en umiddelbar energikilde, men også som et energilager som kan brukes når det oppstår behov. Dette lagret kalles glykogen, et forgrenet polysakkarid sammensatt av mange glukosemolekyler. Glykogenet lagres hovedsakelig i lever og muskler. Disse lagrene fungerer som et effektivt reservoar, klart til å levere energi raskt når kroppen trenger det – enten mellom måltider, under fysisk aktivitet eller i perioder med faste.
Glykogenmetabolismen består av to motsatte prosesser:
- Glykogensyntese (glykogenese), oppbyggingen av glykogen.
- Glykogennedbrytning (glykogenolyse), nedbrytningen av glykogen til glukose.
La oss se nærmere på disse prosessene og hvordan kroppen regulerer dem.
Glykogensyntese (glykogenese)
Når du spiser mat rik på karbohydrater og blodsukkeret stiger, frigjør kroppen hormonet insulin. Insulin gir signal om at det er overskudd av energi i blodbanen, og dermed at noe av glukosen bør lagres. Kroppen responderer ved å aktivere prosessen glykogensyntese.
I glykogensyntesen omdannes glukose til glukose-6-fosfat, deretter videre til glukose-1-fosfat, før det til slutt kobles til en nukleotid-bærer (UDP-glukose). Denne UDP-glukosen brukes av enzymet glykogensyntase til å bygge opp de lange og forgrenede kjedene som kjennetegner glykogen. Jo mer glukose som er tilgjengelig, jo større blir glykogenlagrene i lever og muskelceller.
Glykogensyntase er nøkkelenzymet i glykogensyntesen, og insulin stimulerer dette enzymet ved å fjerne fosfatgrupper (defosforylere det), noe som øker enzymets aktivitet. Resultatet er effektiv lagring av glukose i form av glykogen.
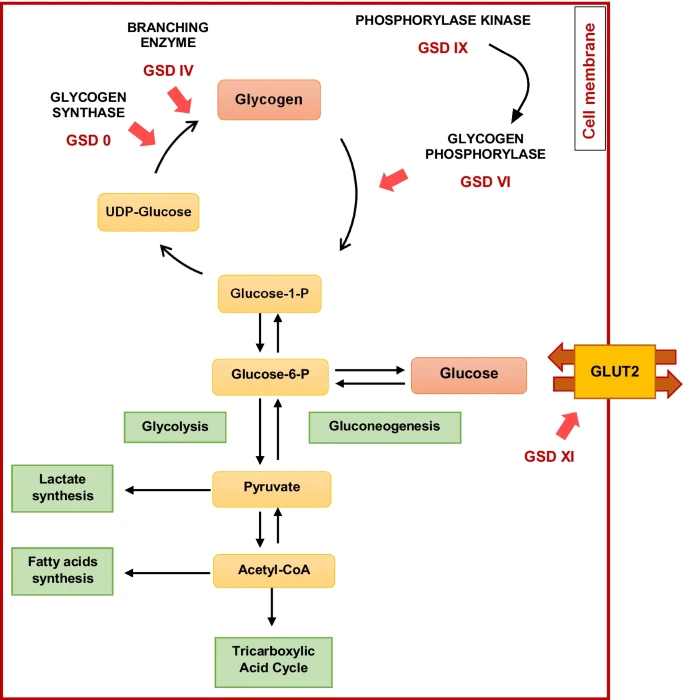
Glykogennedbrytning (glykogenolyse)
Hva skjer så når kroppen trenger energi igjen, for eksempel under trening eller etter flere timer uten mat? Da må glykogenlagrene mobiliseres raskt, og kroppen aktiverer prosessen kjent som glykogenolyse.
Glykogenolyse innebærer at glykogen brytes ned til glukose-1-fosfat av enzymet glykogenfosforylase.
Dette enzymet klipper av glukosemolekyler fra enden av de lange, forgrenede glykogenkjedene.
Glukose-1-fosfat blir raskt omdannet videre til glukose-6-fosfat.
I leveren finnes enzymet glukose-6-fosfatase, som frigjør fri glukose til blodbanen, slik at hjernen og andre organer kan forsynes med nødvendig energi.
Muskelceller mangler dette enzymet, og glukosen de frigjør fra glykogenlagrene brukes derfor lokalt som energikilde.
Glykogenfosforylase aktiveres av hormonet glukagon (i lever) og av stresshormonet adrenalin (i både lever og muskler).
Når disse hormonene frigjøres, fosforyleres glykogenfosforylase og aktiveres raskt, slik at kroppen øyeblikkelig kan bryte ned glykogen og øke blodsukkeret og energitilførselen til muskler.
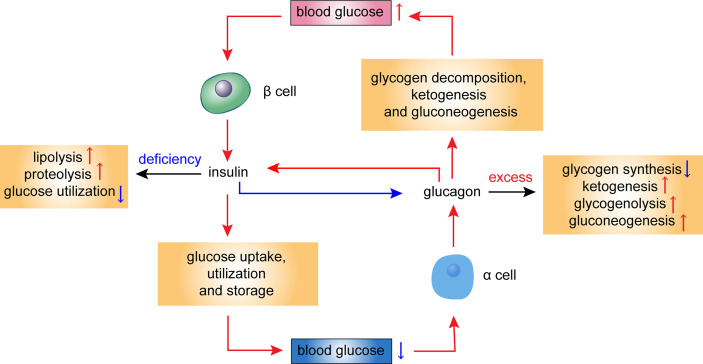
Regulering av glykogenmetabolisme
Den fine balansen mellom lagring og nedbrytning av glykogen styres nøye gjennom hormonelle signaler. Det er spesielt hormonene insulin, glukagon og adrenalin som sørger for at kroppen responderer effektivt på endringer i energibehov:
- Insulin frigjøres ved høyt blodsukker og stimulerer glykogensyntese ved å aktivere enzymet glykogensyntase, samtidig som det hemmer enzymet glykogenfosforylase.
- Glukagon og adrenalin skilles ut når kroppen opplever lavt blodsukker eller stress. Disse hormonene aktiverer enzymet glykogenfosforylase, som resulterer i rask frigjøring av glukose fra glykogenlagrene.
Denne hormonelle reguleringen sikrer at kroppen raskt kan veksle mellom lagring og frigjøring av glukose etter behov, noe som er helt nødvendig for å opprettholde et stabilt energinivå i alle kroppens organer.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3