Dette er en kort video som hjelper deg å huske glykolysen:
Glykolysen er den første og kanskje mest grunnleggende delen av cellens energiomsetning.
Det er her glukose, et sekskarbon-sukker, brytes ned til to molekyler pyruvat – og i prosessen dannes energi som cellen kan bruke.
Glykolysen foregår i cytosol, altså væsken inni cellen, og den fungerer uten oksygen. Det betyr at prosessen er anaerob og dermed også viktig for celler og organismer som har begrenset tilgang på oksygen.
Selv om glykolysen bare gir en liten del av den totale energien som kan hentes ut fra glukose, er den helt nødvendig.
For det første er det glykolysen som setter i gang hele prosessen med cellulær respirasjon.
For det andre kan mange celler – inkludert røde blodceller – kun hente energi fra glykolysen, fordi de ikke har mitokondrier til å drive videre nedbrytning. Tenk over hvorfor røde blodceller ikke driver glykolyse.
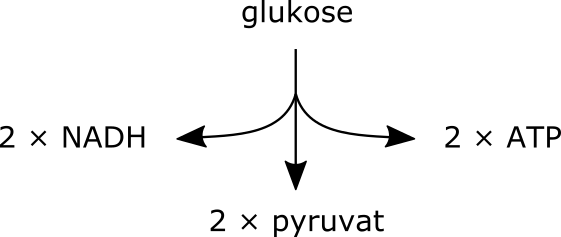
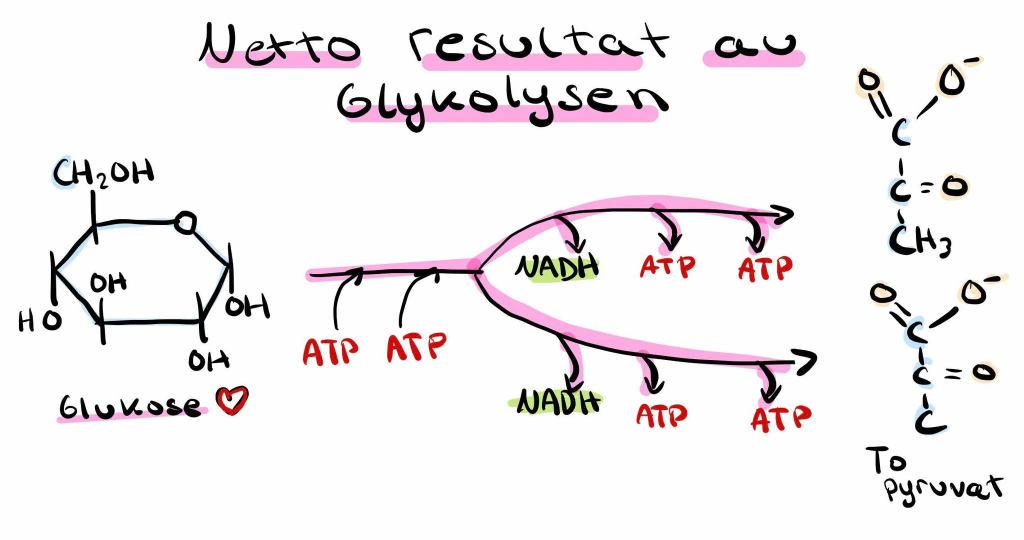
Hva får vi ut av glykolysen?
Netto energigevinst etter én glukose er:
- 2 ATP – produsert direkte via substratnivåfosforylering.
- 2 NADH – som bærer høyenergielektroner og senere kan gi mer ATP i elektrontransportkjeden (dersom oksygen er til stede).
Glykolysen ender med dannelsen av to pyruvatmolekyler. Hva som skjer med pyruvat avhenger av om det er oksygen tilgjengelig. I aerobe celler føres pyruvat videre til mitokondriene, hvor det omdannes til acetyl-CoA og går inn i Krebs-syklusen. Deretter kobles prosessen til elektrontransportkjeden i oksidativ fosforylering – og her produseres hovedmengden ATP.
Glykolysen – veien til energi
Glykolysen er en av de mest fundamentale prosessene i cellens energimetabolisme. Den er ikke bare viktig – den er uunnværlig. Når kroppen bryter ned glukose for å hente energi, skjer dette ikke i ett stort smell. I stedet foregår prosessen trinnvis, slik at energien kan utnyttes kontrollert og effektivt.
Den store reaksjonen
Den fullstendige nedbrytningen av ett glukosemolekyl (C₆H₁₂O₆) til karbondioksid (CO₂) og vann (H₂O) er en prosess som involverer både glykolysen, Krebs-syklusen og oksidativ fosforylering. Sammen sørger de for at energien i glukose omdannes til ATP – cellens viktigste energibærer.
Hovedreaksjon:
C₆H₁₂O₆ + 6O₂ → 6CO₂ + 6H₂O + energi (ATP)
Denne kjemiske likningen viser hvordan kroppen med hjelp av oksygen henter ut energi fra glukose – en prosess som danner grunnlaget for aerob cellulær respirasjon.
ATP – cellens energivaluta
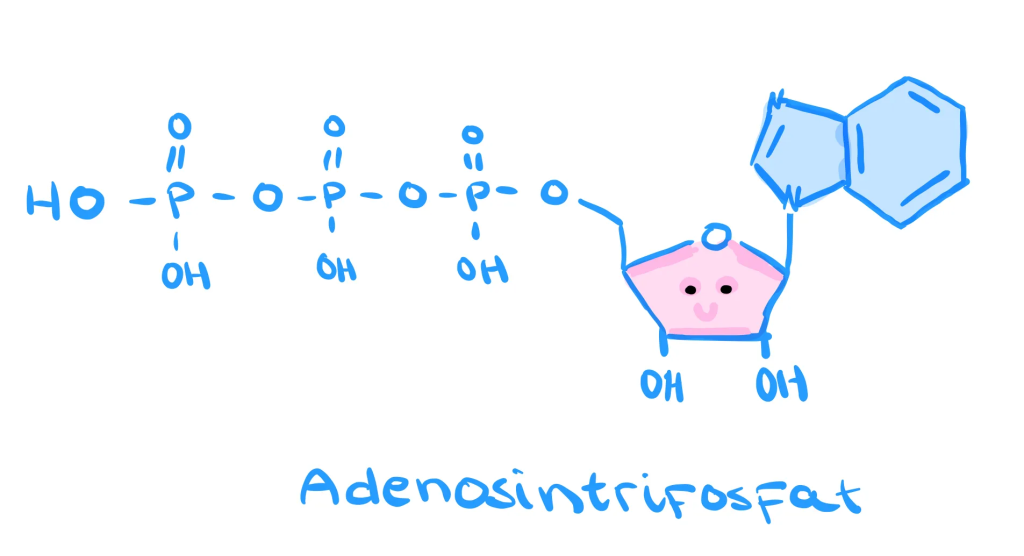
ATP står for adenosintrifosfat, og er molekylet cellene bruker når de trenger energi – enten det er for å bevege seg, bygge proteiner eller sende nervesignaler. ATP består av tre deler: en nitrogenholdig base (adenin), et sukker (ribose), og tre fosfatgrupper på rekke. Det er bindingene mellom disse fosfatgruppene som er nøkkelen til ATPs energipotensial.
Den ytre fosfatbindingen er særlig ustabil, og når den brytes i en prosess som kalles hydrolyse, frigjøres det en betydelig mengde energi:
ATP + H₂O → ADP + Pi + energi
ΔG = -30,5 kJ/mol
Energien som frigjøres her er faktisk nok til å varme opp omtrent 10 gram vann fra frysepunktet til kokepunktet – per mol ATP.
Celler forbruker ATP så raskt at en gjennomsnittlig person faktisk resirkulerer omtrent sin egen kroppsvekt i ATP hver eneste dag.
Oksidasjon og reduksjon
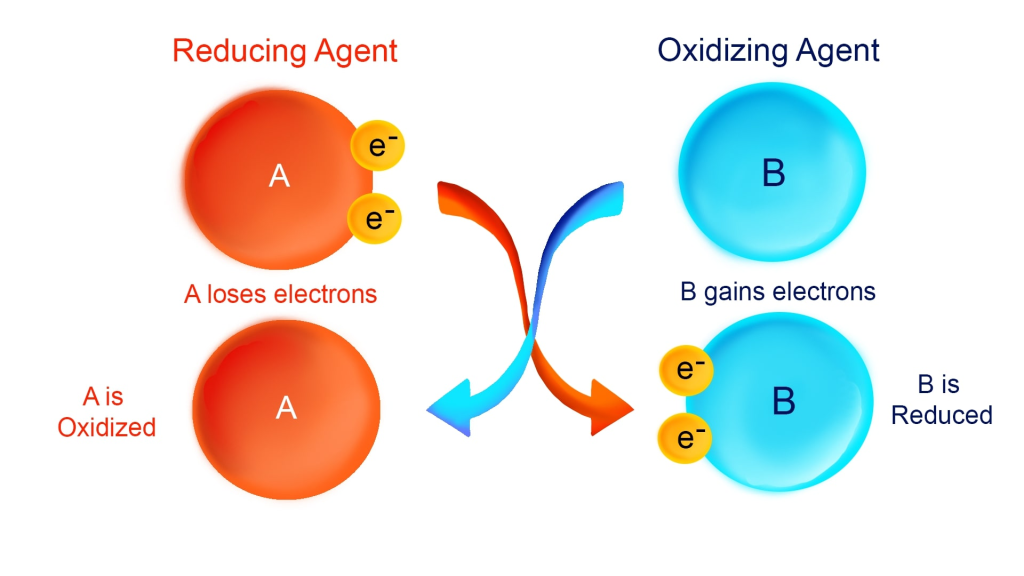
I biokjemien handler mye om overføring av elektroner. Når et stoff oksideres, mister det elektroner eller hydrogenatomer – og dette frigjør energi. Når et annet stoff reduseres, tar det opp disse elektronene. Oksidasjon og reduksjon skjer alltid sammen, og i cellen er dette sentralt for hvordan energi overføres og utnyttes.
- Oksidasjon = Elektroner fjernes → energi frigjøres (katabolsk)
- Reduksjon = Elektroner tas opp → energi lagres (anabolsk)
Denne elektronflyten skjer via spesialiserte bærermolekyler.
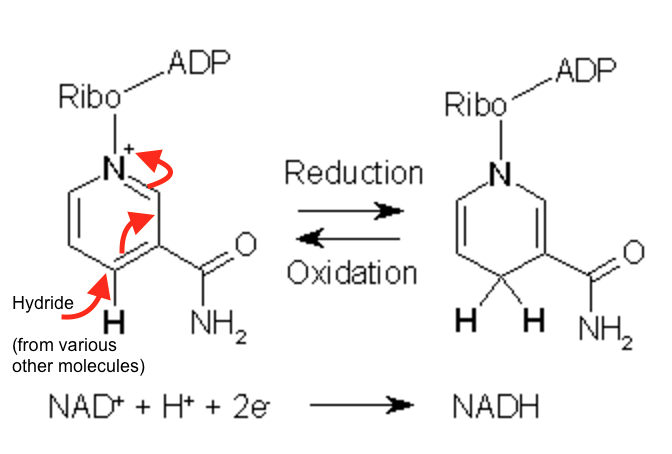
NADH og NADPH – cellens elektronbærere
To av de viktigste elektronbærerne i cellen er NAD⁺/NADH og NADP⁺/NADPH.
Disse fungerer som små, mobile «batterier» som tar opp og gir fra seg elektroner – akkurat når det trengs.
Når NAD⁺ tar opp elektroner og ett hydrogenatom (H⁺), dannes NADH – den reduserte formen.
NADH er energirik og kan levere elektroner videre til elektrontransportkjeden, hvor den bidrar til ATP-produksjon.
- NAD⁺ = oksidert form
- NADH = redusert form
NADPH fungerer på lignende måte, men brukes hovedsakelig i anabole prosesser, som syntese av fettsyrer og kolesterol, hvor det bidrar med elektroner.
Et viktig poeng er at NADH og NADPH er minst stabile i sin reduserte form. Det betyr at de lett gir fra seg elektroner – og nettopp det gjør dem så nyttige for cellen.
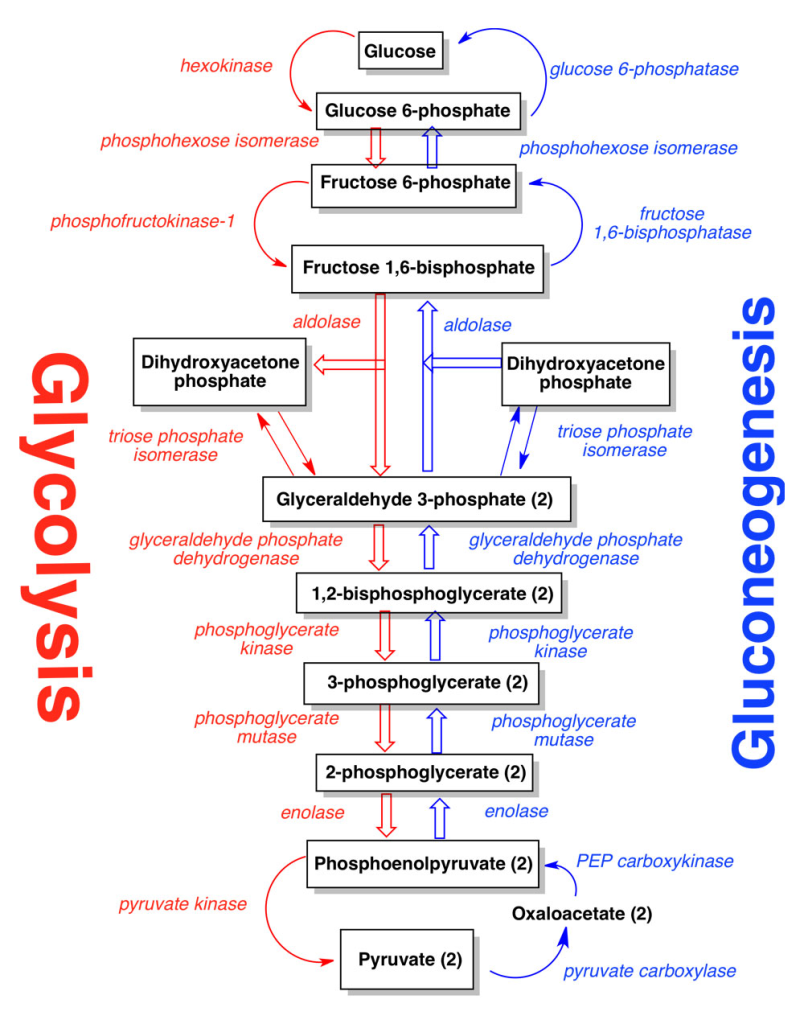
Alle steg i glykolysen
Glykolysen skjer gjennom flere trinn, hver katalysert av spesifikke enzymer. Man trenger ATP for å sette i gang reaksjonen, men det vil netto gi tilbake mer ATP og NADH. Glykolysen finner sted i cellens cytosol, den er uavhengig av oksygen.
Pyruvat kan kanaliseres inn i TCA-syklusen (Krebs-syklusen) og brytes fullstendig ned til CO₂ og vann. Denne fullstendige nedbrytningen genererer en betydelig mengde ATP.
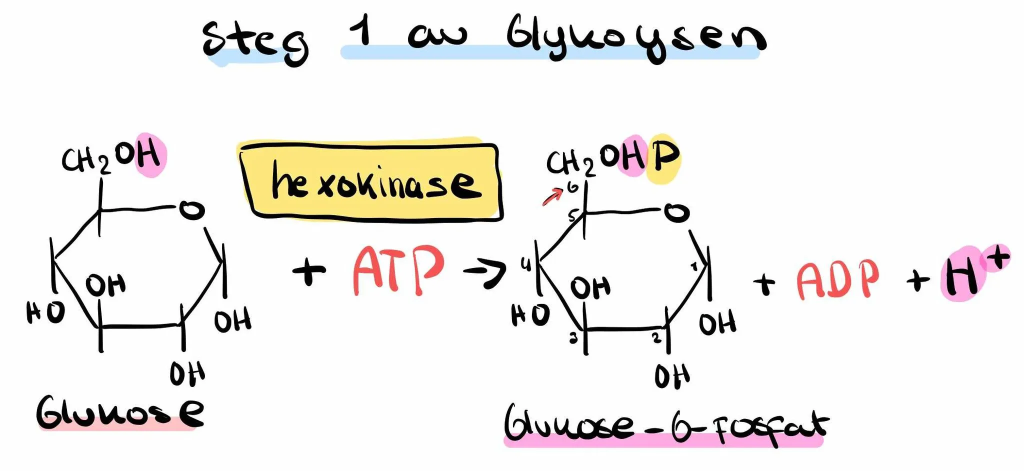
Steg 1: Fosforylering av glukose
Aller først må glukose aktiveres. Det skjer ved at det festes en fosfatgruppe til glukosemolekylet – en prosess som bruker én ATP.
Dermed dannes glukose-6-fosfat.
Denne reaksjonen katalyseres av enzymet heksokinase, og den er viktig av flere grunner:
- Glukose fanges inne i cellen: Når fosfatgruppen bindes til glukose, endres strukturen og glukose kan ikke lenger passere cellemembranen. Den er «låst inne».
- Reaksjonen er irreversibel: Reaksjonen går bare én vei under normale fysiologiske forhold – noe som gjør dette til et reguleringspunkt i glykolysen.
- Fosforylering øker reaktiviteten: Fosfatgrupper har en negativ ladning, som gjør at molekylet blir mer reaktivt og klar for videre kjemiske transformasjoner.
Hvorfor fosforylere?
Fosforylerte forbindelser har flere viktige egenskaper:
- De blir i cellen, fordi negativt ladede grupper hindrer diffusjon gjennom cellemembraner.
- De fungerer som energilagre, der fosfatgruppen kan overføres til andre molekyler.
- De gjør substratene mer spesifikke for enzymene i neste trinn i glykolysen.
- De kan bidra til å senke aktiveringsenergien i reaksjoner.
💡 Heksokinase – et viktig nøkkelenzym
Heksokinase er faktisk ikke ett enzym, men en familie av nært beslektede enzymer som alle gjør samme jobb: De fosforylerer glukose til glukose-6-fosfat.
Hos pattedyr finnes det fire hovedtyper:
| Enzymtype | Affinitet for glukose | Hvor finnes det? | Kalles også |
|---|---|---|---|
| Heksokinase I | Høy (lav Km) | Hjerne, muskler | – |
| Heksokinase II | Høy (lav Km) | Muskler, fett | – |
| Heksokinase III | Høy (lav Km) | Varierte vev | – |
| Heksokinase IV | Lav (høy Km) | Lever og betaceller i pankreas | Glukokinase |
Det spesielle med glukokinase er at den bare er aktiv når glukosenivåene i blodet er høye – slik som etter et måltid. Dette er viktig i leveren, som da tar opp overskuddsglukose og lagrer det som glykogen. I betacellene i bukspyttkjertelen fungerer glukokinase nærmest som en «sensor» for blodsukker, og påvirker utskillelsen av insulin.
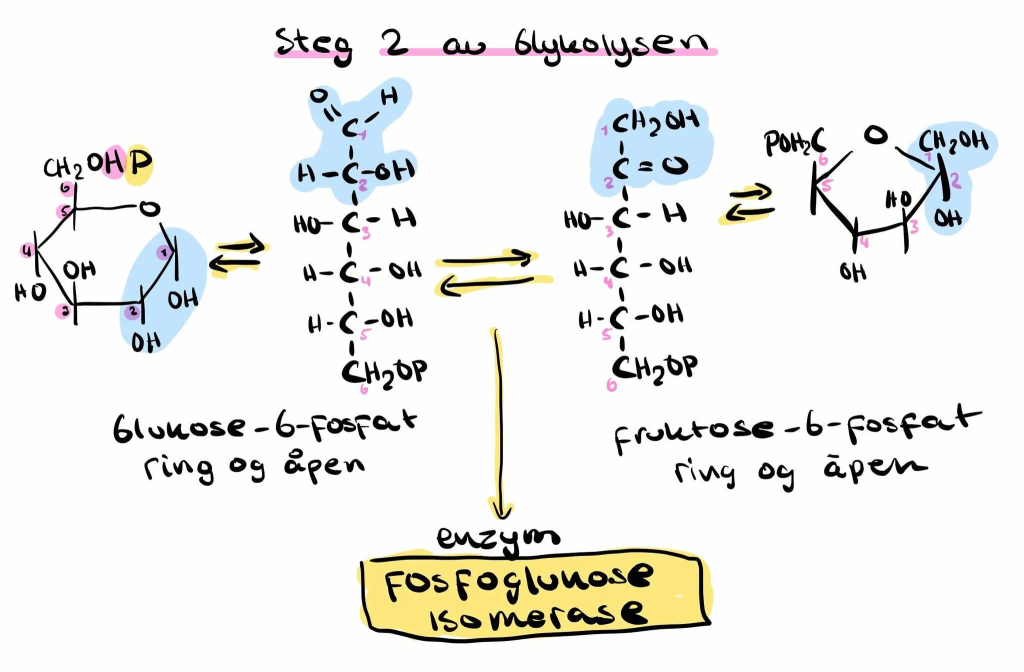
Steg 2: Omforming av glukose-6-fosfat til fruktose-6-fosfat
I dette steget katalyserer enzymet fosfoglukoisomerase en isomerisering – altså en omorganisering av atomer uten å endre molekylformelen.
Det sekskantede glukose-6-fosfat-molekylet åpnes, og karbonylgruppen flyttes fra karbon 1 til karbon 2.
Dette omdanner glukose (en aldose) til fruktose (en ketose).
Resultatet er fruktose-6-fosfat, som er bedre egnet for videre fosforylering og symmetrisk spalting.
Denne reaksjonen er reversibel, men går effektivt fremover fordi produktet raskt forbrukes i neste trinn.
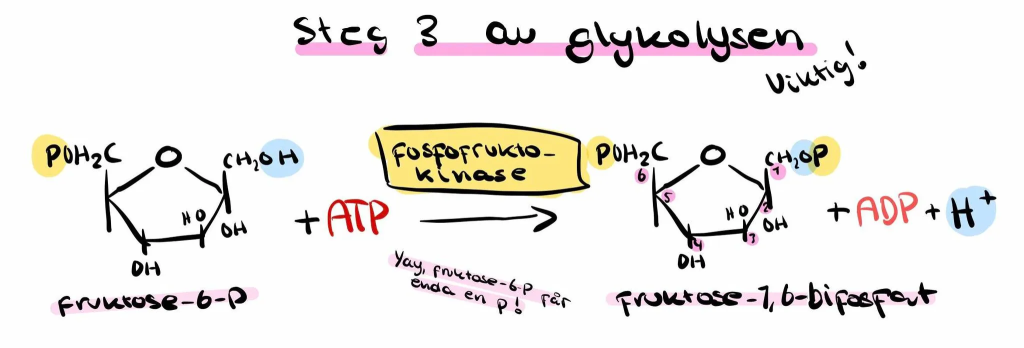
Steg 3: Fosforylering av fruktose-6-fosfat til fruktose-1,6-bisfosfat
Her kommer en av de viktigste reaksjonene i hele glykolysen – det vi kan kalle et reguleringspunkt.
Enzymet fosfofruktokinase-1 (PFK-1) overfører en ny fosfatgruppe fra ATP til karbon 1 i fruktose-6-fosfat, og danner fruktose-1,6-bisfosfat.
Reaksjonen er irreversibel, og fungerer nærmest som en “port” som bestemmer om glukose virkelig skal brukes til energiproduksjon.
PFK-1 er et sentralt regulert enzym, og responderer blant annet på cellens energistatus (mengden ATP og AMP).
💡 Tenk på dette som det punktet hvor cellen sier: «OK, vi skal virkelig bruke dette glukosemolekylet til å lage energi.»
Steg 4: Spalting av fruktose-1,6-bisfosfat
Det som nå skjer er at det sekskarbon-sukkeret splittes i to trekarbonforbindelser. Enzymet aldolase katalyserer denne reaksjonen og danner:
- Dihydroksyacetonfosfat (DHAP)
- Glyseraldehyd-3-fosfat (G3P)
Selv om reaksjonen er reversibel, drives den effektivt fremover fordi glyseraldehyd-3-fosfat raskt forbrukes i neste trinn av glykolysen.
Men hva skjer med DHAP? Jo, dette molekylet er en speilvendt isomer av G3P og kan derfor enkelt konverteres til glyseraldehyd-3-fosfat av enzymet triosefosfatisomerase.
👉 Dermed ender vi opp med to molekyler G3P fra hvert glukosemolekyl, klare til å gå inn i neste fase av glykolysen: energiutbytte-fasen.
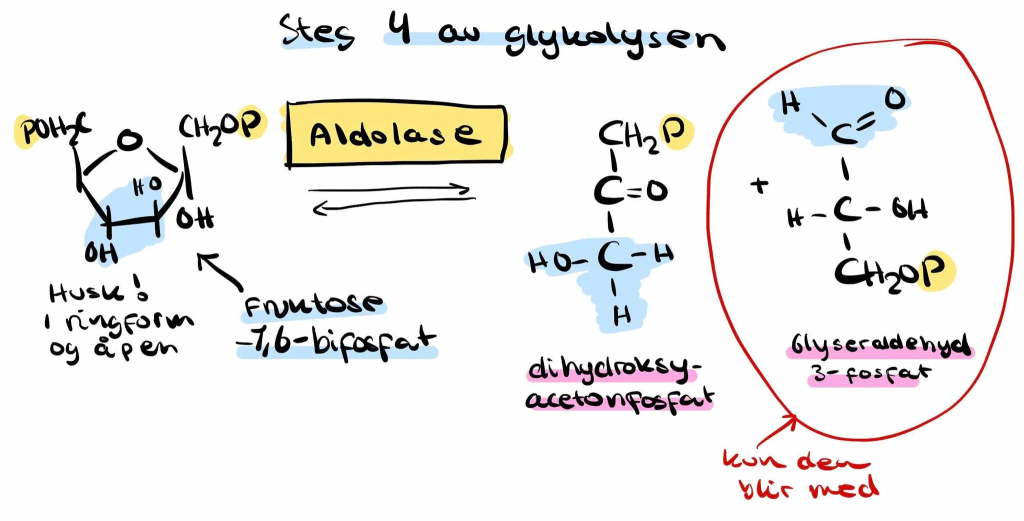
Steg 5: Isomerisering av DHAP til glyseraldehyd-3-fosfat (G3P)
Enzymet triosefosfatisomerase konverterer dihydroksyacetonfosfat (DHAP) til glyseraldehyd-3-fosfat (G3P).
Dermed har vi to molekyler G3P fra hvert glukosemolekyl.
Dette steget er viktig fordi bare G3P kan gå videre i glykolysen.
Reaksjonen er reversibel, men drives fremover ved at G3P brukes umiddelbart i neste reaksjon.
🔁 Dette steget markerer slutten på energiinvesteringsfasen: To ATP er brukt, og glukose er delt i to like energibærende molekyler.
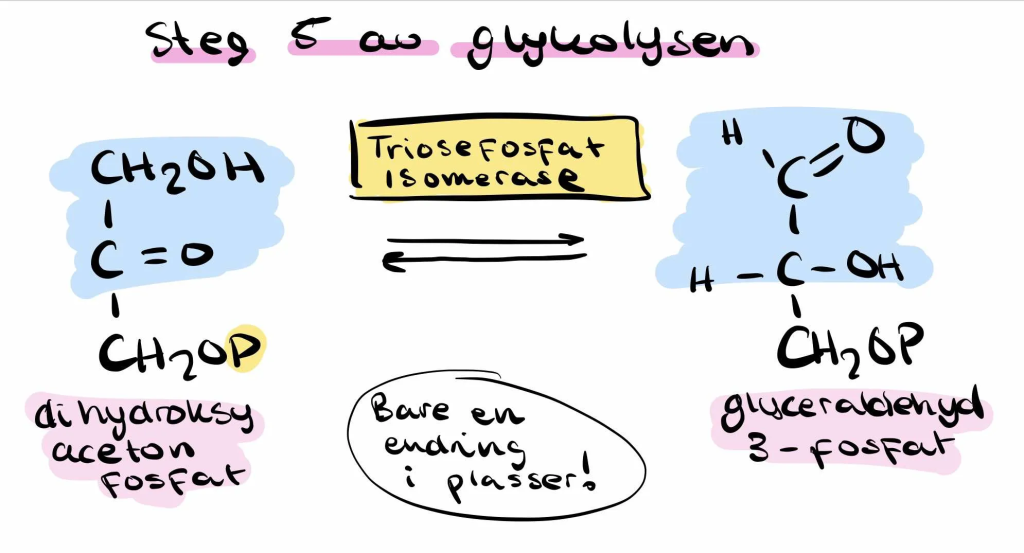
Steg 6: Oksidasjon av G3P til 1,3-bisfosfoglyserat (1,3-BPG)
Her skjer den første oksidasjonsreaksjonen i glykolysen.
Enzymet glyseraldehyd-3-fosfat dehydrogenase fjerner elektroner fra G3P og overfører dem til NAD⁺, som dermed reduseres til NADH.
Samtidig utnyttes energien fra oksidasjonen til å feste en uorganisk fosfatgruppe (Pi) til molekylet. Resultatet er 1,3-bisfosfoglyserat (1,3-BPG) – et molekyl med en svært energirik fosfatbinding.
⚡ Dette er første gang i glykolysen at NADH dannes, som senere kan brukes i elektrontransportkjeden for å lage mer ATP.
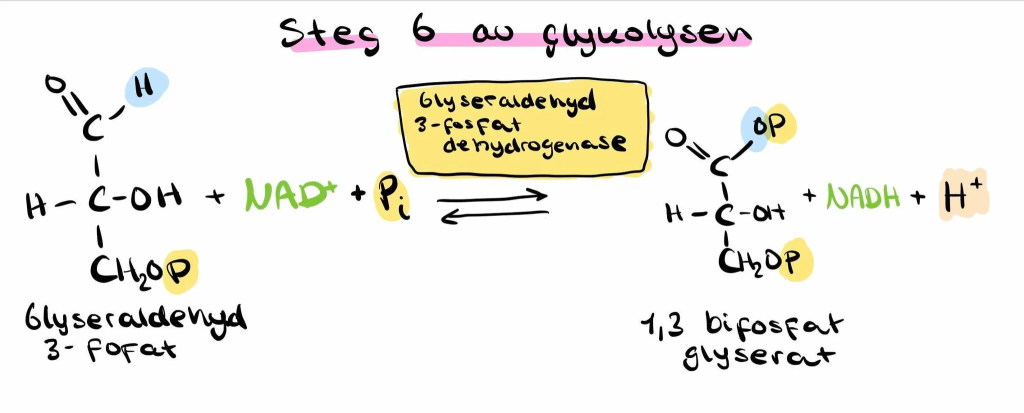
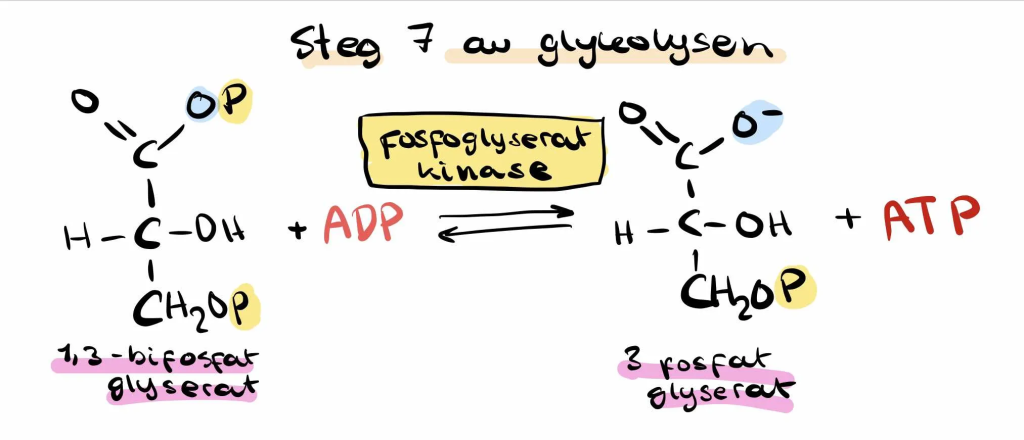
Steg 7: Produksjon av ATP fra 1,3-BPG
Den høye energien i 1,3-BPG brukes nå til å fosforylere ADP til ATP. Dette skjer via enzymet fosfoglyseratkinase, som overfører en fosfatgruppe fra 1,3-BPG til ADP.
Dette kalles substratnivåfosforylering, fordi ATP dannes direkte fra substratet – uten hjelp av oksygen eller mitokondrier.
Dette er første gang i glykolysen at cellen får tilbake ATP – og siden hvert glukose gir to G3P, får vi to ATP i dette steget.
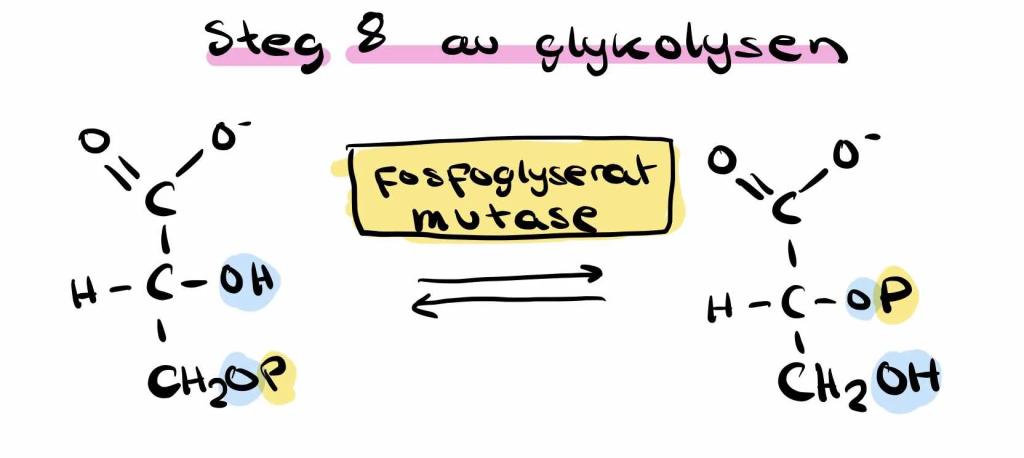
Steg 8: Omorganisering av 3-fosfoglyserat til 2-fosfoglyserat
Etter at ATP er produsert, sitter vi igjen med 3-fosfoglyserat.
Enzymet fosfoglyseratmutase flytter fosfatgruppen fra karbon 3 til karbon 2 og danner 2-fosfoglyserat.
Dette er en forberedelse for å danne et nytt høyenergimolekyl.
3-fosfoglyserat har ikke nok energi til å fosforylere ADP direkte, men det vil 2-fosfoglyserat snart kunne.
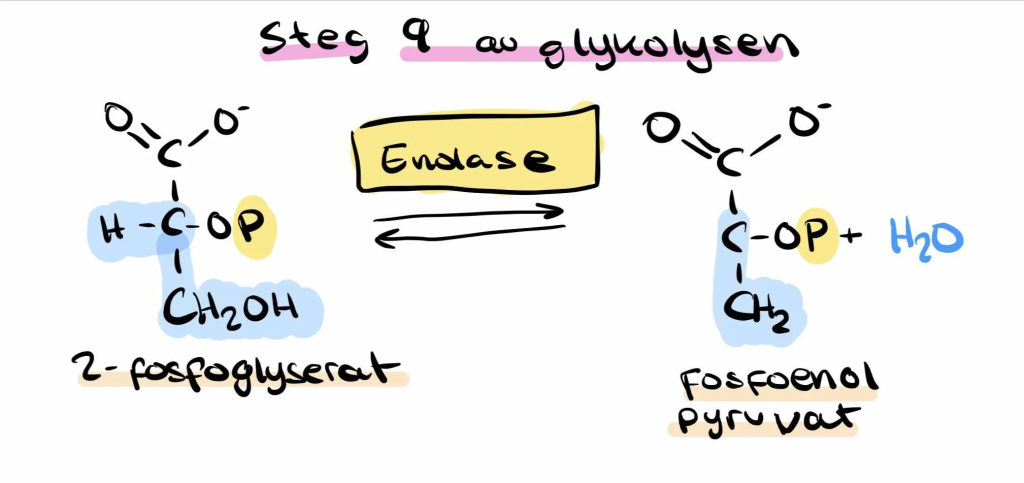
Steg 9: Dehydrering til fosfoenolpyruvat (PEP)
Nå fjerner enzymet enolase et vannmolekyl fra 2-fosfoglyserat.
Dette skaper en dobbeltbinding og danner fosfoenolpyruvat (PEP) – et molekyl med ekstremt høy fosfatgruppeoverføringspotensial.
PEP inneholder en av de mest energirike fosfatbindingene i kroppen.
Den lagrede energien i bindingen skal brukes til å danne enda mer ATP i neste steg.
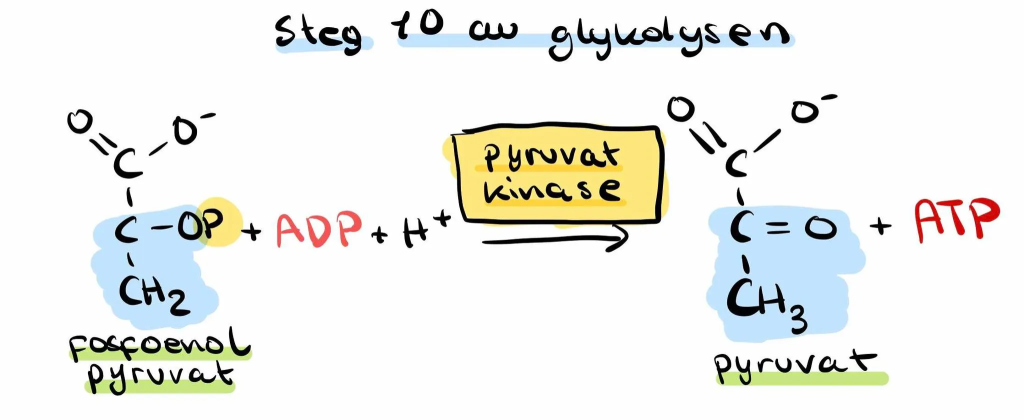
Steg 10: Dannelse av ATP og pyruvat
I det siste steget i glykolysen overfører enzymet pyruvatkinase fosfatgruppen fra PEP til ADP, og danner ATP og pyruvat.
Dette er den andre substratnivåfosforyleringen i glykolysen – og også her dannes to ATP for hvert glukosemolekyl (én per PEP).
Samtidig produseres pyruvat, som er sluttproduktet i glykolysen. Avhengig av oksygentilgang og celletypens behov, kan pyruvat gå videre til ulike veier:
- Omdannes til acetyl-CoA og gå inn i sitronsyresyklusen.
- Omdannes til laktat i fravær av oksygen (anaerob glykolyse).
Oppsummert energiutbytte (per glukosemolekyl):
- Bruk: 2 ATP (i trinn 1 og 3)
- Gevinst: 4 ATP (trinn 7 og 10) og 2 NADH (trinn 6)
- Netto energigevinst: 2 ATP + 2 NADH + 2 pyruvat
Glykolysens Energiøkonomi og Pyruvats Videre Skjebne
Glykolysen er ikke bare en serie kjemiske reaksjoner – det er en nøye koordinert balanse mellom investering og gevinst. For å kunne utnytte glukose som energikilde må cellen først bruke litt energi, før den får betalt med renter i form av ATP og NADH.
Energiinvestering og høsting
Tidlig i glykolysen investerer cellen to ATP-molekyler. Disse brukes til å:
- Fosforylere glukose, slik at det fanges inne i cellen
- Aktivere glukose og forvandle det til energirike mellomprodukter
De fosforylerte mellomproduktene som dannes har faktisk høyere energiinnhold enn glukose selv. Dette gjør dem ideelle som utgangspunkt for videre nedbrytning, der energien kan hentes ut.
I de senere trinnene av glykolysen hentes denne investerte energien tilbake – og mer til.
Totalt produseres fire ATP, men fordi to ATP ble brukt i starten, sitter cellen igjen med en netto gevinst på to ATP per glukosemolekyl.
I tillegg produseres to NADH-molekyler, som senere kan brukes til ATP-syntese i mitokondriene hvis oksygen er tilgjengelig.
Hvor blir det av energien?
Selv etter at glykolysen er ferdig, er det meste av energien i glukosemolekylet fortsatt lagret i de to pyruvatmolekylene som dannes. Faktisk overføres 90–95 % av energien fra glukose til pyruvat.
For å hente ut resten av denne energien, må pyruvat gå videre til nye reaksjonsveier – og hva som skjer videre, avhenger av hvorvidt cellen har tilgang på oksygen eller ikke.
Pyruvats videre skjebne
Aerobe forhold: Pyruvat → Acetyl-CoA
Hvis oksygen er tilgjengelig, transporteres pyruvat inn i mitokondriene og omdannes til acetyl-CoA.
Dette molekylet går så inn i sitronsyresyklusen (Krebs-syklusen), og videre inn i den oksidative fosforyleringen, hvor mesteparten av cellens ATP dannes.
- Energiutbytte i aerobe forhold: opptil ~38 ATP per glukose
Anaerobe forhold: Pyruvat → Laktat
I fravær av oksygen – for eksempel i muskelceller under hard fysisk belastning – er ikke mitokondriene tilgjengelige for oksidativ nedbrytning. I stedet omdannes pyruvat til laktat i en prosess som også regenererer NAD⁺ fra NADH.
Denne reaksjonen, katalysert av laktatdehydrogenase, er avgjørende for at glykolysen skal kunne fortsette. NAD⁺ er nemlig nødvendig for oksidasjonstrinnet i glykolysen (steg 6).
- Energiutbytte i anaerobe forhold: kun 2 ATP per glukose
Eksempel: Under intens trening, når oksygentilførselen til musklene ikke er tilstrekkelig, går glykolysen videre i anaerob retning – og laktat bygges opp.
Oppsummert: Valget mellom to veier
| Forhold | Pyruvat omdannes til | Hensikt | Energiutbytte |
|---|---|---|---|
| Aerobt | Acetyl-CoA | Fullstendig nedbrytning i mitokondriene | ~38 ATP |
| Anaerobt | Laktat | Regenerere NAD⁺ for glykolyse | 2 ATP |
NAD⁺
For at glykolysen skal kunne fortsette uavbrutt, spesielt gjennom det energihøstende trinnet hvor glyseraldehyd-3-fosfat oksideres (steg 6), er cellen avhengig av at elektronbæreren NAD⁺ er tilgjengelig i sin oksiderte form.
Hvorfor er NAD⁺ så viktig?
I trinn 6 donerer glyseraldehyd-3-fosfat elektroner til NAD⁺ og danner NADH. Uten NAD⁺ stopper denne reaksjonen opp, og dermed stopper hele glykolysen. Cellen må derfor kontinuerlig regenerere NAD⁺ for å holde glykolysen i gang.
Regenerering av NAD⁺:
- Under aerobe forhold: NAD⁺ regenereres i mitokondriene, der NADH leverer elektroner til elektrontransportkjeden. Pyruvat går samtidig inn i sitronsyresyklusen og fullføres i oksidativ fosforylering.
- Under anaerobe forhold (f.eks. under intensiv trening): Elektrontransportkjeden kan ikke brukes, fordi oksygen mangler som endelig elektronakseptor. I stedet reduseres pyruvat til laktat i cytosol ved hjelp av enzymet laktatdehydrogenase, som samtidig oksiderer NADH tilbake til NAD⁺.
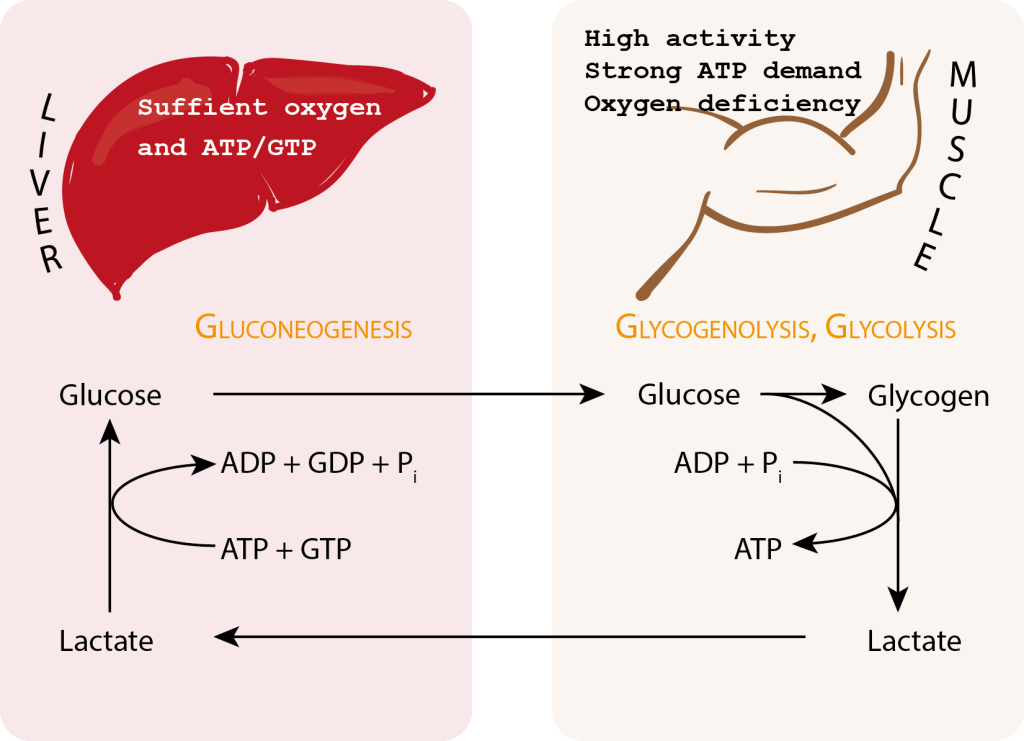
Cori-syklus – Kroppens Energiresirkuleringssystem
Når laktat bygges opp i muskelcellene under anaerobe forhold, kan det ikke akkumuleres for lenge uten konsekvenser.
I stedet transporteres det med blodet til leveren, hvor det igjen omdannes til glukose via glukoneogenese.
Denne glukosen kan så sendes tilbake til musklene og brukes på nytt i glykolysen – en energikrevende, men viktig resirkuleringsmekanisme kjent som Cori-syklus.
Cori-syklusen illustrerer et elegant samspill mellom muskler og lever i reguleringen av blodsukker og energiforsyning.
Energi og Ubalanse: Delta G i Glykolysen
Glykolysen inneholder ti enzymkatalyserte reaksjoner, men det er særlig tre av disse som skiller seg ut ved å ha svært negative Gibbs fri energi-endringer (ΔG). Dette gjør dem irreversible, og dermed nøkkeltrinn for regulering.
De tre irreversible reaksjonene:
- Hexokinase (trinn 1): Fosforylerer glukose til glukose-6-fosfat
- Fosfofruktokinase-1 (PFK-1) (trinn 3): Fosforylerer fruktose-6-fosfat til fruktose-1,6-bisfosfat
- Pyruvatkinase (trinn 10): Overfører fosfat fra PEP til ADP, og danner pyruvat og ATP
Disse reaksjonene har så stor negativ ΔG at de i praksis ikke kan reverseres under normale forhold i cellen. Nettopp derfor brukes de også som regulatoriske knutepunkt.
Regulering av Glykolysen
Celler har en fantastisk evne til å tilpasse sin energiproduksjon etter behov. Når ATP-nivåene synker og cellen trenger mer energi, økes aktiviteten i glykolysen – særlig i de tre irreversible trinnene.
Disse enzymene stimuleres av:
- Lav ATP
- Høyt AMP/ADP
- Økt tilgjengelighet av substrater som glukose
Og hemmes av:
- Høye nivåer av ATP (spesielt PFK-1)
- Sitronsyre og andre metabolitter fra mitokondriene som signaliserer at cellen har nok energi
Resultatet er en elegant og kontinuerlig regulering hvor glykolysen skrus på når det trengs – og bremses når energibehovet er lavt.
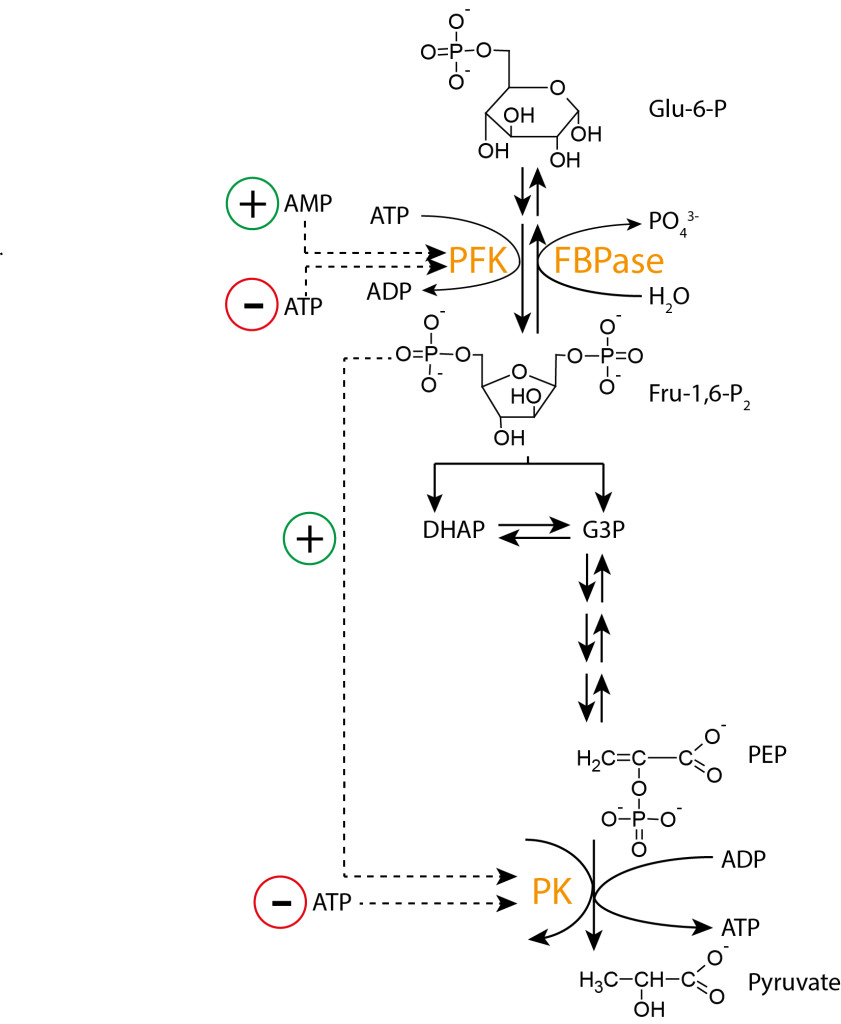
Regulering av Glykolysen
Glykolysen er ikke bare en energiproduserende vei – den er også strengt regulert. Det er spesielt tre trinn i glykolysen som er irreversible og fungerer som strategiske kontrollpunkter for å justere strømmen av metabolitter etter cellens behov: steg 1, 3 og 10. Ved å regulere disse enzymene, kan cellen øke eller bremse glykolysen avhengig av energibehov og hormonelle signaler.
Steg 1: Hexokinase – Portvokteren som stenger glukose inne i cellen
Hexokinase katalyserer det første trinnet i glykolysen – fosforyleringen av glukose til glukose-6-fosfat (G-6-P). Dette trinnet er viktig fordi det forhindrer glukose fra å forlate cellen igjen.
Men denne reaksjonen er ikke ukritisk – enzymet reguleres gjennom allosterisk hemming av sitt eget produkt, G-6-P.
Når konsentrasjonen av G-6-P blir høy, reduseres enzymets aktivitet.
Dette hindrer overforbruk av ATP og unødvendig glukoseopptak når cellen ikke trenger mer energi.
Ulike vev, ulike behov:
- I muskelceller er hexokinase alltid aktiv – musklene trenger ofte energi raskt og bruker glukose effektivt, uavhengig av blodsukkeret.
- I leveren finnes et isoenzym kalt glukokinase (hexokinase IV), som kun aktiveres ved høye glukosenivåer. Det er ikke hemmet av G-6-P, noe som gjør det ideelt for å hjelpe leveren å regulere blodsukkeret etter måltider.
Steg 3: Fosfofruktokinase-1 (PFK-1) – Glykolysens sjefsbryter
Dette er glykolysens viktigste kontrollpunkt.
PFK-1 regulerer overgangen fra fruktose-6-fosfat til fruktose-1,6-bisfosfat – og fungerer som cellens metabolske «gasspedal».
Hemmere:
- ATP fungerer som en allosterisk hemmer: Når det er mye ATP i cellen, reduseres PFK-1s affinitet for substratet – et signal om at cellen har nok energi.
- Citratsyklusens mellomprodukt citrat hemmer også enzymet – og fungerer som en kobling til mitokondriell metabolisme. Når citrat hoper seg opp, bremser glykolysen.
Aktiverere:
- AMP og ADP aktiverer PFK-1 – signaler om lavt energinivå får glykolysen til å gå raskere.
- Fruktose-2,6-bisfosfat (F-2,6-BP) er en kraftig allosterisk aktivator som overstyrer ATPs hemmende effekt og stimulerer glykolysen selv når energinivået er høyt.
PFK-2/FBPase-2 – Det hormonstyrte skiftet mellom glykolyse og glukoneogenese
F-2,6-BP dannes og brytes ned av et bifunksjonelt enzym med to domener:
- PFK-2: Katalyserer dannelse av F-2,6-BP → stimulerer glykolyse via PFK-1.
- FBPase-2: Bryter ned F-2,6-BP → hemmer glykolyse og fremmer glukoneogenese.
Hormonkontroll:
- Insulin aktiverer PFK-2 og fremmer dannelsen av F-2,6-BP → glykolyse stimuleres.
- Glukagon aktiverer FBPase-2 og bryter ned F-2,6-BP → glykolyse hemmes, og glukoneogenese favoriseres.
Dette systemet gir cellene en måte å finstyre glykolyse etter kroppens hormonelle status – for eksempel i fasting eller etter måltider.
Steg 10: Pyruvatkinase – Sluttporten til energiproduksjon
Pyruvatkinase katalyserer det siste steget i glykolysen, der PEP omdannes til pyruvat, samtidig som det dannes ATP.
Regulering:
- ATP hemmer enzymet – et signal om at energilageret er fullt.
- Acetyl-CoA, som kommer fra fettsyreoksidasjon og sitronsyresyklus, hemmer også pyruvatkinase og sparer på glukose når andre energikilder er tilgjengelige.
- Fruktose-1,6-bisfosfat, som dannes tidligere i glykolysen, aktiverer pyruvatkinase – et godt eksempel på feed-forward-aktivering, hvor metabolitten «forbereder» senere trinn.
Hormonregulering i leveren:
- Insulin stimulerer pyruvatkinase ved defosforylering → aktiverer glykolyse.
- Glukagon hemmer enzymet via fosforylering → bremser glykolyse og sparer glukose i leveren.
Kooperativitet:
Pyruvatkinase har fire subenheter, og binding av ett substrat (PEP) øker affiniteten for de andre – en egenskap kjent som kooperativ binding, også sett hos hemoglobin.
Hva er egentlig allosterisk regulering?
Allosterisk regulering betyr at enzymaktivitet justeres ved binding av regulatoriske molekyler til et annet sted enn det aktive setet – det såkalte allosteriske setet. Disse regulatorene kan enten aktivere eller hemme enzymet, ofte ved å endre enzymets tredimensjonale form.
Dette gjør at cellen kan raskt og presist tilpasse enzymaktiviteten etter indre og ytre signaler – et nøkkelprinsipp i all metabolsk regulering.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3
❓ Test deg selv
Obs, tomt! Kommer etterhvert <3
Legg igjen en kommentar