Enzymer fungerer som biokatalysatorer og er hovedsakelig sammensatt av proteiner, med noen få unntak som ribosomer. Disse molekylene har en evne til å akselerere kjemiske reaksjoner uten selv å bli forbrukt i prosessen.
Nøkkelfakta om enzymer:
- Enzymer gjør det mulig for kjemiske reaksjoner å foregå raskere ved kroppstemperatur.
- I menneskekroppen finnes det rundt 20 000 protein-kodende gener, hvor omtrent 25-35% av disse koder for enzymer.
- De fleste enzymer er globulære proteiner og varierer i størrelse fra 50 til 2500 aminosyrer.
Enzymenes effektivitet ligger i deres evne til å senke aktiveringsenergien for kjemiske reaksjoner. Dette oppnås gjennom det aktive setet, en spesifikk region på enzymet hvor substratet binder seg og den katalytiske aktiviteten finner sted. Det aktive setet er ofte rikt på polare og ladede aminosyrer som kan indusere kjemiske endringer i substratet.
Klassifisering av enzymer
Enzymer er naturens egne katalysatorer – biologiske verktøy som setter fart på kjemiske reaksjoner uten selv å forbrukes. For å kunne holde oversikt over alle de tusenvis av enzymene som finnes i kroppen, har den internasjonale biokjemiunionen (IUB) sammen med Enzymkommisjonen (EC) laget en systematisk klassifisering. Den deler enzymene inn i seks hovedklasser, basert på hvilken type kjemisk reaksjon de katalyserer. Dette gjør det lettere å forstå både hva enzymet gjør, og hvilken rolle det spiller i cellens indre kjemi.
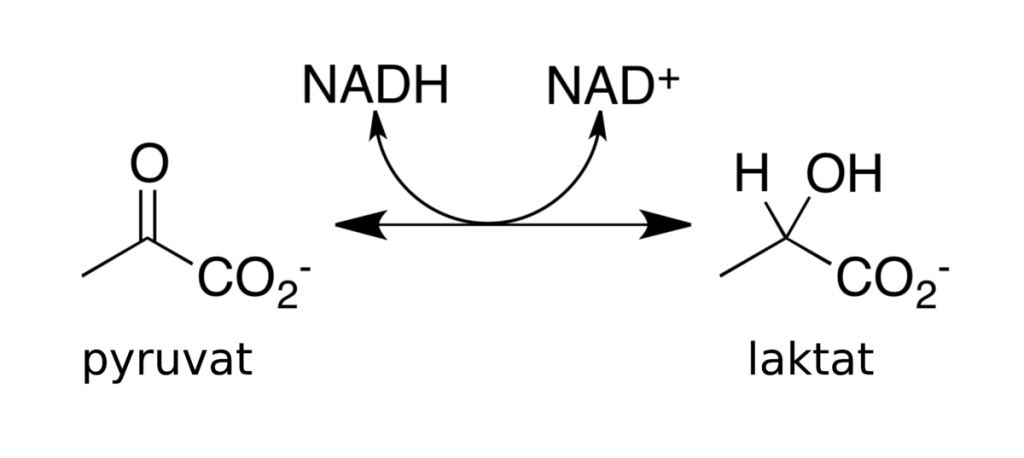
Den første og kanskje mest fundamentale klassen er oksidoreduktaser. Disse enzymene katalyserer redoksreaksjoner – det vil si overføring av elektroner fra ett molekyl til et annet. Dette er helt sentralt i cellens energiomsetning, spesielt i mitokondriene. Et klassisk eksempel er laktatdehydrogenase, som katalyserer omdanningen av laktat til pyruvat, samtidig som NAD⁺ reduseres til NADH. Her overføres elektronene fra laktat til NAD⁺, noe som gjør dette enzymet til en viktig aktør i glukosemetabolismen.
Den neste klassen, transferaser, fungerer som molekylære «fraktemenn.» De overfører en funksjonell gruppe – som en fosfat-, metyl- eller aminogruppe – fra ett molekyl til et annet. Dette er helt avgjørende i biosyntetiske veier. Et godt eksempel er serin hydroksymetyltransferase, som overfører en hydroksymetylgruppe til glycin og danner serin – en nøkkelreaksjon i metabolismen av aminosyrer.
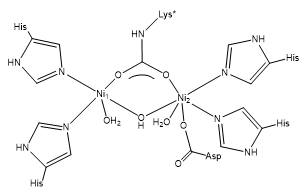
Hydrolaser er enzymer som bryter bindinger ved hjelp av vann. Dette er den mest tallrike enzymklassen, og dominerer i fordøyelsessystemet, hvor store molekyler som proteiner og nukleinsyrer må brytes ned til mindre bestanddeler. Urease, som spalter urea til ammoniakk og karbondioksid ved hydrolyse, er et godt eksempel på hvordan kroppen håndterer nitrogenavfall.
Der hydrolaser bruker vann, gjør lyaser jobben uten verken vann eller redoks. Disse enzymene bryter kjemiske bindinger – særlig karbon-karbon, karbon-oksygen eller karbon-nitrogen-bindinger – men gjennom helt andre mekanismer. Ofte dannes det dobbeltbindinger i prosessen. Et klassisk eksempel er pyruvat dekarboksylase, som fjerner en karboksylgruppe fra pyruvat og danner acetaldehyd og CO₂ – en viktig reaksjon i alkoholgjæring.
Isomeraser er spesialister på å omorganisere molekylstrukturer. De endrer konfigurasjonen til et molekyl uten å legge til eller fjerne atomer – de skaper altså isomerer. Dette kan være essensielt i metabolske veier som krever bestemte stereoisomerer. Et eksempel er metylenmalonyl-CoA-isomerase, som omdanner metylenmalonyl-CoA til succinyl-CoA i forberedelse til TCA-syklusen.
Den siste klassen er ligaser, enzymene som binder sammen to molekyler ved hjelp av energi – vanligvis fra ATP. De brukes ofte i anabole prosesser der nye bindinger må dannes, for eksempel i DNA-syntese eller karbonfiksering. Pyruvatkarboksylase er et kjent eksempel: det binder sammen pyruvat og CO₂ for å danne oksaloacetat, et sentralt molekyl i glukoneogenesen.
Selv om alle enzymene har ulike roller, deler de dette felles: de senker aktiveringsenergien i en reaksjon og gjør det mulig for cellen å kontrollere kjemi med ekstrem presisjon og hastighet. Klassifiseringen i seks hovedgrupper hjelper oss å se mønstre og forstå enzymenes rolle i de store biologiske prosessene.
Stabilisering av overgangstilstanden
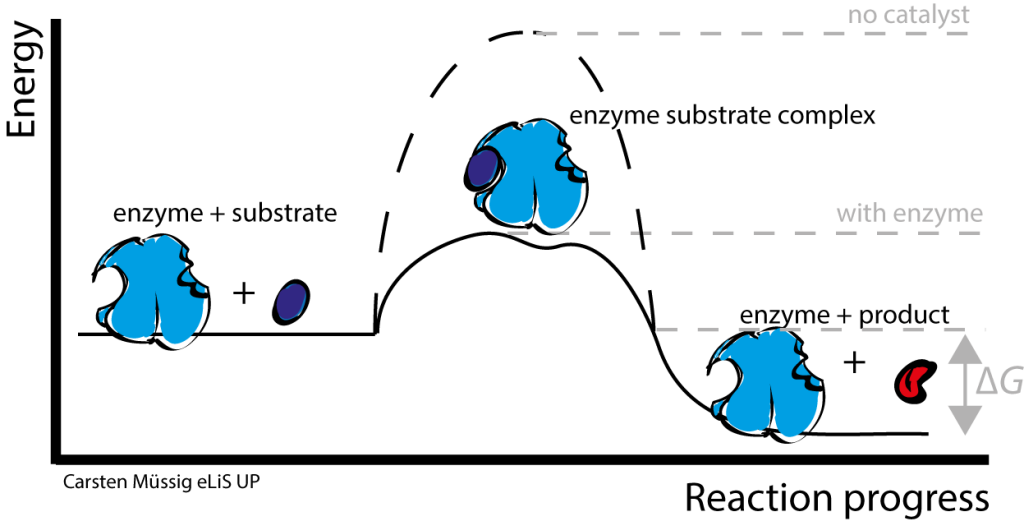
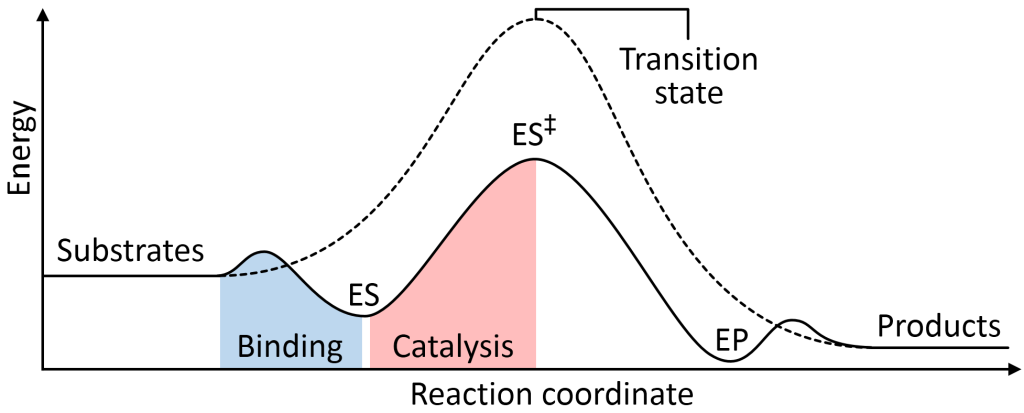
Enzymer har en unik evne til å øke hastigheten på kjemiske reaksjoner – noen ganger med en faktor på millioner. Men de gjør det ikke ved å tilføre energi, som varme ville gjort i et reagensrør. I stedet jobber enzymer på en mye mer elegant måte: de senker aktiveringsenergien, altså energibarrieren som reaksjonen må overvinne. Det viktigste trikset de bruker for å få til dette, er å stabilisere overgangstilstanden.
Hva er overgangstilstanden?
Når to molekyler reagerer, går de gjennom en høyenergetisk og ustabil mellomfase, kalt overgangstilstanden. Her er gamle bindinger i ferd med å brytes, og nye i ferd med å dannes. Dette er det mest krevende punktet i reaksjonen – en slags «topp» som reaksjonen må klatre over før den kan gå videre. Jo lavere toppen er, desto raskere går reaksjonen. Enzymer hjelper til med å flate ut denne toppen.
Et enzym stabiliserer overgangstilstanden ved å samhandle med substratet på en måte som senker energien som kreves for å nå denne mellomtilstanden. Dette kan sammenlignes med å bruke et stativ for å holde en ustabil gjenstand på plass – mindre energi trengs for å holde det hele sammen. Enzymet gjør dette gjennom flere presise mekanismer:
1. Optimal orientering av reaktantene
Enzymer binder substratene og plasserer dem nøyaktig i forhold til hverandre, slik at de kjemiske gruppene som skal reagere kommer i perfekt posisjon. Uten enzymet måtte molekylene «snuble» inn i hverandre med riktig vinkel og energi ved en tilfeldighet. Med enzymet ligger alt klart til reaksjon.
2. Dannelse av partielle ladninger
Mange enzymreaksjoner involverer overføring av elektroner, protoner eller ladninger. Enzymer kan endre ladningsfordelingen i substratet ved å samhandle med det på atomnivå – for eksempel ved å danne midlertidige hydrogenbindinger eller elektrostatiske interaksjoner. Dette kan gjøre substratet mer reaktivt, og lette overgangen til reaksjonsproduktet.
3. Induksjon av spenning i substratet
Noen enzymer virker ved å deformere substratet litt – binde det på en måte som «drar» i en binding som skal brytes, eller presser substratet inn i en form som ligner overgangstilstanden. Dette skaper indre spenning i molekylet, som gjør det mer tilbøyelig til å gjennomgå den ønskede kjemiske forandringen. Det er nesten som enzymet «jukser» substratet litt nærmere målstreken før løpet har begynt.
Hvordan enzymer fungerer
For å forstå hvordan enzymer gjør jobben sin, må vi først se nærmere på hva som skjer når et enzym møter sitt substrat – altså molekylet det skal reagere med. Enzymer er svært spesifikke; de kjenner igjen bestemte substrater og binder dem på en nøye tilpasset måte. Men hvordan skjer denne gjenkjenningen og bindingen?
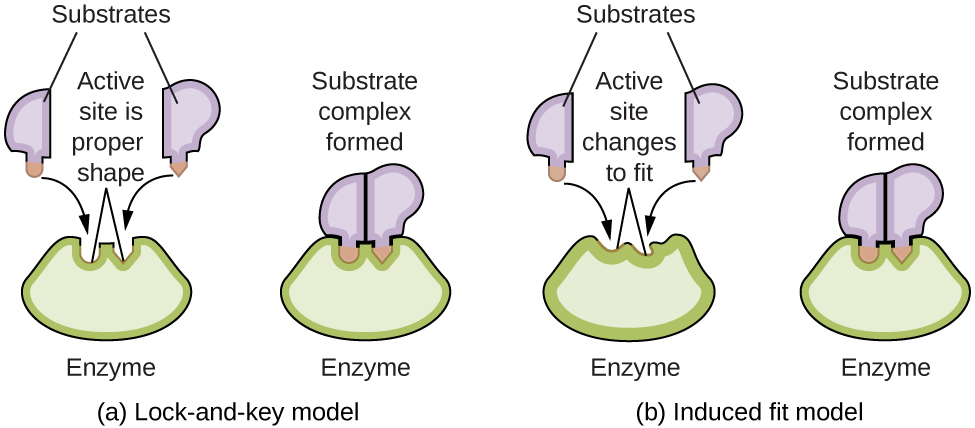
Forskere har utviklet ulike modeller for å forklare dette, og de to mest kjente er Lock-and-Key-modellen og Induced Fit-modellen.
Lock-and-Key – perfekt passform fra start
Den klassiske Lock-and-Key-modellen ble foreslått tidlig i enzymforskningens historie. Den ser for seg enzymet som en lås, og substratet som en nøkkel som passer perfekt inn i det aktive setet – enzymets «arbeidsrom». I denne modellen er både enzym og substrat stive strukturer som passer sammen uten at noen av dem trenger å endre form.
Et godt eksempel på denne mekanismen er enzymet lysozym, som finnes i spytt og tårer. Lysozym bryter ned bakteriers cellevegg ved å passe perfekt rundt et bestemt sukkermolekyl i celleveggen. Her er enzymets aktive sete som en skreddersydd fordypning, og substratet passer som hånd i hanske.
Induced Fit – fleksibel tilpasning
Senere forskning har vist at enzymet ofte ikke er helt «låst» i form. I stedet er mange enzymer fleksible, og tilpasser seg substratet når det nærmer seg. Dette kalles Induced Fit-modellen – en mer dynamisk og moderne forståelse av enzymers funksjon. Her er enzymet som en hanske som former seg etter hånden som settes inn i den.
Et tydelig eksempel er enzymet heksokinase, som spiller en viktig rolle i glukosemetabolismen. Når glukose nærmer seg det aktive setet, endrer heksokinase form – nesten som om det «omfavner» substratet. Denne formendringen fører substratet enda tettere på de kjemiske gruppene som skal gjøre jobben, og øker dermed reaksjonens hastighet og presisjon.
Hvorfor er dette viktig?
Uansett hvilken modell som gjelder for et spesifikt enzym, er poenget det samme: enzymer binder substrater og bringer dem i riktig posisjon for å senke aktiveringsenergien og fremskynde reaksjonen. Om det skjer gjennom perfekt passform eller dynamisk tilpasning, handler det alltid om å gjøre kjemien lettere for cellen.
Kofaktorer og spesifisitet
Mange enzymer trenger hjelp fra små molekyler for å kunne utføre sin katalytiske oppgave – disse hjelperne kalles kofaktorer.
En kofaktor er et ikke-proteinmolekyl som binder seg til enzymet og hjelper til i reaksjonen. Noen kofaktorer er permanente deler av enzymet og er sterkt bundet – disse kalles prostetiske grupper. Andre binder seg mer løst og midlertidig – de kalles ofte koenzymer.
Kofaktorer kan være både organiske molekyler og metallioner. Mange er avledet fra vitaminer, og derfor er tilstrekkelig vitamininntak avgjørende for enzymfunksjon i kroppen.
Eksempler på viktige kofaktorer:
- Tiaminpyrofosfat (fra vitamin B1): Brukes av enzymer som håndterer aldehyder.
- Flavin-adenin-dinukleotid (FAD, fra vitamin B2): Viktig for elektronoverføring, spesielt i celleånding.
- Koenzym A: Nøkkelspiller i overføring av acylgrupper, som i fettsyreomsetning og TCA-syklusen.
- Pyridoksalfosfat (fra vitamin B6): Brukes i reaksjoner der aminogrupper overføres, altså i aminosyremetabolismen.
Disse små molekylene fungerer som midlertidige «bærere» av elektroner, atomer eller grupper som må flyttes mellom molekyler i løpet av en kjemisk reaksjon.
Nøkkelen passer bare én lås – eller flere?
En annen viktig egenskap ved enzymer er hvor spesifikke de er for sine substrater. Denne spesifisiteten varierer – noen enzymer er kresne og jobber bare med én type substrat, mens andre er mer fleksible.
Absolutt spesifisitet
Noen enzymer fungerer som en spesialnøkkel som bare passer én lås. Et klassisk eksempel er glukoseoksidase, som bare reagerer med glukose og ignorerer alle andre sukkermolekyler. Dette gir høy nøyaktighet, og brukes blant annet i blodsukkermålere.
Gruppespesifisitet
Andre enzymer er mer som en hovednøkkel som kan åpne flere lignende låser. For eksempel kan alkoholdehydrogenase katalysere reaksjoner for flere ulike alkoholer – som etanol, metanol og propanol. Enzymet kjenner igjen en bestemt kjemisk gruppe (–OH-gruppen) og kan jobbe med substrater som har denne.
Enzymkinetikk
Enzymer er biologiske katalysatorer som muliggjør livsnødvendige reaksjoner i kroppen. Men hvor raskt virker de egentlig? Og hva påvirker hastigheten? For å svare på dette har biokjemikere utviklet faget enzymkinetikk – et verktøy som gir oss muligheten til å måle og forstå enzymers aktivitet under ulike betingelser. Et av de viktigste konseptene i enzymkinetikken er forholdet mellom substratkonsentrasjon og reaksjonshastighet, og dette er nettopp det Michaelis-Menten-modellen forsøker å beskrive.
Denne modellen, som bygger på enkle forutsetninger, gir et matematisk bilde av hvordan enzymets hastighet (V) øker med økende mengde substrat ([S]), men flater ut når enzymet blir mettet – altså når nesten alle de aktive setene på enzymet til enhver tid er bundet til substrater. Michaelis-Menten-ligningen beskrives slik:
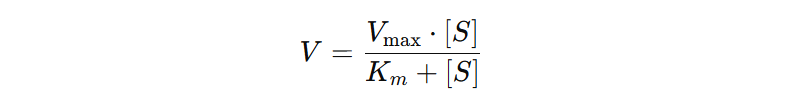
Her står V for den faktiske reaksjonshastigheten, [S] for substratkonsentrasjonen, Vₘₐₓ for den maksimale reaksjonshastigheten når enzymet er mettet med substrat, og Kₘ for Michaelis-konstanten.
Michaelis-konstanten, Kₘ, er spesielt viktig fordi den forteller oss noe om enzymets affinitet for sitt substrat. Rent praktisk defineres Kₘ som den substratkonsentrasjonen der reaksjonshastigheten er halvparten av Vₘₐₓ.
Enzymet jobber da på «halv maskin».
Jo lavere Kₘ-verdien er, desto høyere er enzymets affinitet for substratet, fordi det trengs mindre substrat for å oppnå høy aktivitet.
Et enzym med høy Kₘ derimot, krever en mye større konsentrasjon av substrat for å nå samme nivå av aktivitet – og har dermed lavere affinitet.
Reaksjonshastigheten øker altså med økende substratkonsentrasjon, men bare opp til et visst punkt.
Etter hvert som alle de aktive setene på enzymet blir opptatt, vil økt substratkonsentrasjon ha stadig mindre effekt.
Kurven for dette forholdet er karakteristisk buet: rask økning i starten, før den gradvis flater ut mot en asymptotisk Vₘₐₓ.
Denne kurven er selve signaturen på Michaelis-Menten-kinetikk.
For å kunne analysere enzymkinetiske data mer nøyaktig, benytter man ofte en lineær versjon av modellen – det såkalte Lineweaver-Burk-plottet. Her tar man den dobbelte resiproke verdien av både reaksjonshastighet og substratkonsentrasjon, og setter dette inn i en lineær ligning:
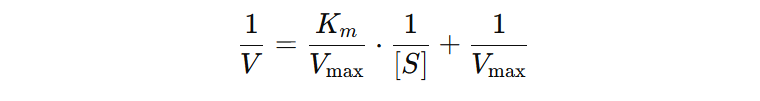
Dette gir en rett linje der skjæringspunktet med y-aksen tilsvarer 1/Vₘₐₓ, og med x-aksen −1/Kₘ.
Stigningen på linjen er gitt av forholdet Kₘ/Vₘₐₓ. Selv om denne fremstillingen er nyttig for å hente ut eksakte verdier, har den sine svakheter – blant annet at målefeil får stor betydning ved lave substratkonsentrasjoner – men den har likevel historisk vært viktig i enzymforskningen.
Å kjenne til et enzyms Kₘ og Vₘₐₓ er ikke bare akademisk – det har klinisk og praktisk verdi.
Farmasøyter bruker det til å designe legemidler som hemmer spesifikke enzymer. Fysiologer og biokjemikere bruker det til å forstå hvordan kroppen justerer enzymaktiviteten i ulike organer og tilstander.
Enzym + substrat → produkt
Reisen begynner med at et enzym møter sitt substrat – det molekylet det skal omdanne. Enzymet har et aktivt sete, en liten «lomme» i sin struktur, hvor substratet passer inn. Når enzym og substrat møtes, dannes et enzym-substrat-kompleks (ES). Dette komplekset kan enten gå videre og danne produkt, eller brytes opp igjen til enzym og substrat uten at noen kjemisk reaksjon har skjedd.
Denne dynamikken kan beskrives slik:
E + S ⇌ ES → E + P
Med andre ord: enzymet og substratet binder hverandre reversibelt, før substratet eventuelt omdannes til produkt.
Hva avgjør hvor raskt reaksjonen skjer?
Reaksjonshastigheten – altså hvor mye produkt som dannes per tidsenhet – avhenger i stor grad av hvor mye substrat som finnes tilgjengelig. Når substratkonsentrasjonen er lav, vil mange enzymmolekyler være ledige, og reaksjonen går sakte fordi det er få «kollisjoner» mellom enzym og substrat. Men når substratkonsentrasjonen øker, vil flere og flere enzymmolekyler være opptatt med substrat, og reaksjonshastigheten øker.
Men denne økningen skjer ikke i det uendelige. Etter hvert vil alle enzymene være opptatt, og reaksjonen når et metningspunkt. Nå hjelper det ikke lenger å tilsette mer substrat – enzymene jobber allerede så raskt de kan. Denne makshastigheten kalles Vmax.
Michaelis-konstanten (Km)
Et nøkkelbegrep i Michaelis-Menten-kinetikken er Km – Michaelis-konstanten. Dette er substratkonsentrasjonen som gir halvparten av maksimal reaksjonshastighet. Km sier noe viktig om affiniteten mellom enzym og substrat: en lav Km betyr at enzymet binder substratet godt, mens en høy Km antyder svakere binding og behov for høyere substratkonsentrasjon for å oppnå effekt.
Hva forteller Michaelis-Menten-ligningen oss?
Michaelis-Menten-ligningen gir oss ikke bare en matematisk beskrivelse av enzymkinetikk – den forteller oss noe viktig om hvordan enzymet oppfører seg under ulike forhold. Spesielt sier den noe om hva som skjer ved lave og høye substratkonsentrasjoner.
Ved lave substratkonsentrasjoner ([S] ≪ Km)
Når det er lite substrat til stede, er de fleste enzymene ledige – de venter på å binde noe. Under slike forhold vil hastigheten på reaksjonen være direkte proporsjonal med substratkonsentrasjonen. Vi sier at reaksjonen følger førsteordens kinetikk med hensyn til substratet.
Matematisk kan vi forenkle Michaelis-Menten-ligningen slik:
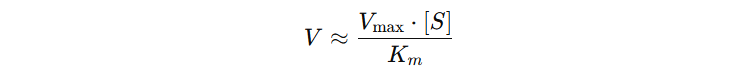
Her ser vi at V øker lineært med [S] – en dobling av substrat gir omtrent en dobling i hastighet. Dette gir mening: når det er lite «mat», klarer enzymet å jobbe raskere for hver lille økning i tilgangen på substrat.
Ved høye substratkonsentrasjoner ([S] ≫ Km)
Når substratkonsentrasjonen er høy, blir de fleste enzymene mettet – det vil si at nesten alle aktive seter allerede er bundet til et substratmolekyl. Enzymet har ikke tid til å ta imot mer, uansett hvor mye substrat som finnes. Under disse forholdene flater kurven ut, og reaksjonen går med maksimal hastighet (Vmax).
Matematisk kan ligningen forenkles slik:
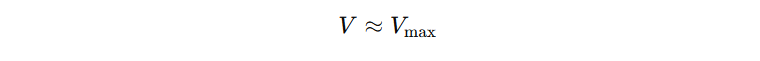
Her ser vi at reaksjonshastigheten er nesten uavhengig av substratkonsentrasjonen – vi sier at reaksjonen følger nullteordens kinetikk med hensyn til substratet. Det hjelper altså ikke å tilsette mer substrat – enzymet jobber så raskt det kan.
Lav [S] → Reaksjonshastighet øker lineært med substratmengde (førsteordens)
Høy [S] → Reaksjonshastighet når taket (Vmax), og videre økning i [S] har liten effekt (nullteordens)
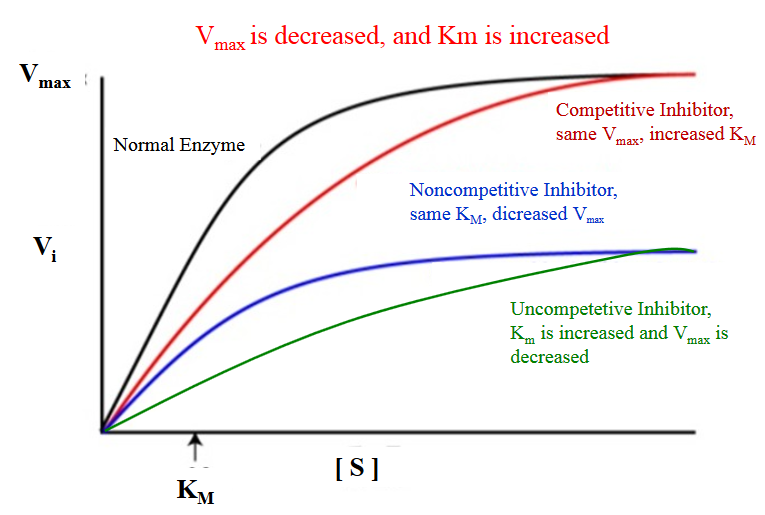
Grafen
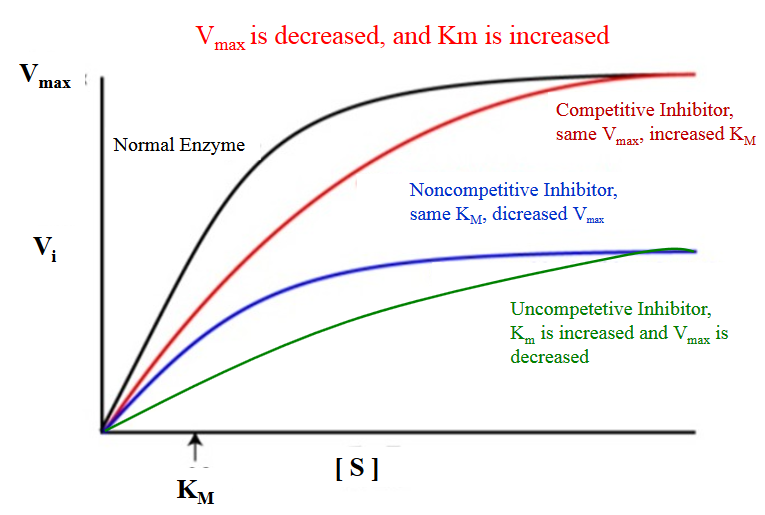
Ikke alle enzymer får arbeide uforstyrret. I mange biologiske og medisinske sammenhenger finnes det molekyler som hemmer enzymaktiviteten, enten naturlig i kroppen eller som legemidler. Disse hemmerne påvirker enzymets kinetikk, og for å forstå hvordan de virker, bruker vi gjerne Michaelis-Menten-modellen som referanseramme. Ved å sammenligne kurver for enzymaktivitet med og uten hemmer, får vi innsikt i hvordan reaksjonshastighet, substrataffinitet og maksimal enzymaktivitet påvirkes.
La oss se nærmere på de tre vanligste formene for enzymhemming: kompetitiv, non-kompetitiv og ukompetitiv hemming.
1. Normal enzymreaksjon (referansekurve)
Uten noen hemmer til stede vil et enzym følge en klassisk Michaelis-Menten-kurve. Reaksjonshastigheten (V) øker med substratkonsentrasjonen ([S]) frem til enzymet er mettet, og reaksjonen når sitt tak: Vmax.
Ved den substratkonsentrasjonen der enzymet når halvparten av Vmax, finner vi Michaelis-konstanten (Km) – et mål på enzymets affinitet for substratet. Denne kurven fungerer som en referanse for alle former for hemming.
2. Kompetitiv hemming 🔴
En kompetitiv hemmer etterligner substratet og konkurrerer om å binde seg til enzymets aktive sete. Så lenge hemmeren er til stede, er det færre enzymmolekyler tilgjengelige for substratet, og det kreves mer substrat for å oppnå samme reaksjonshastighet som normalt.
Resultatet er at:
- Km øker (substrataffiniteten ser ut til å bli lavere)
- Vmax forblir uendret (fordi nok substrat kan konkurrere ut hemmeren)
Med andre ord: enzymet kan fortsatt nå full hastighet hvis det er tilstrekkelig substrat, men det krever mer.
3. Non-kompetitiv hemming 🔵
En non-kompetitiv hemmer binder seg til et annet sted på enzymet – ikke det aktive setet – og påvirker enzymets form eller funksjon. Denne bindingen skjer uavhengig av om substratet er bundet eller ikke. Hemmeren hindrer enzymets evne til å omdanne substratet til produkt, selv om substratet fortsatt kan binde seg.
Dette gir følgende effekt:
- Km er uendret (substratet binder seg like godt som før)
- Vmax reduseres (fordi færre enzymmolekyler er fullt funksjonelle)
Her hjelper det ikke å tilsette mer substrat – enzymets kapasitet er rett og slett redusert.
4. Ukompetitiv hemming 🟢
En ukompetitiv hemmer binder seg kun til enzym-substrat-komplekset (ES) – ikke til det frie enzymet. Når substratet allerede er bundet, kommer hemmeren og låser komplekset slik at det ikke kan omdannes til produkt. Dette reduserer både tilgjengeligheten av aktive enzymkomplekser og produktdannelsen.
Konsekvensene er:
- Km reduseres (fordi substratet bindes mer stabilt – hemmeren «låser» det på plass)
- Vmax reduseres (fordi mindre produkt dannes)
Dette er en mer sjelden form for hemming, men viktig å kjenne til, spesielt i medisinsk biokjemi.
🔁 Oppsummering
| Type hemming | Km | Vmax |
|---|---|---|
| Kompetitiv | Øker | Uendret |
| Non-kompetitiv | Uendret | Redusert |
| Ukompetitiv | Redusert | Redusert |
Eksamensoppgave
Irreversible hemmere og regulering av enzymaktivitet
I motsetning til reversible enzymhemmere, som midlertidig binder seg til enzymet og kan løsne igjen, finnes det også en mer drastisk kategori: irreversible hemmere. Disse hemmerne binder seg permanent til enzymet – ofte ved å danne kovalente bindinger til aminosyrer i eller nær det aktive setet. Resultatet er at enzymet deaktiveres for godt og ikke kan gjenoppta sin funksjon.
Et klassisk eksempel er Hg²⁺-ioner, som binder seg til cysteinrester i enzymets struktur. Cystein inneholder en reaktiv tiolgruppe (-SH), som lett reagerer med metaller som kvikksølv. Når denne bindingen først har skjedd, er enzymet ødelagt og må brytes ned og erstattes med nye proteiner.
Slike irreversible hemmere er ikke bare et biokjemisk fenomen – de har viktige anvendelser. Mange legemidler, spesielt antibiotika og kreftmedisiner, virker ved å irreversibelt hemme enzymer som er avgjørende for vekst og overlevelse av bakterier eller kreftceller. Penicillin er et kjent eksempel: det hemmer et enzym som bakterier trenger for å bygge opp celleveggen, og binder seg irreversibelt slik at bakterien til slutt dør.
Faktorer som påvirker enzymaktivitet
Selv uten hemmere kan enzymers aktivitet påvirkes av ulike fysiske og kjemiske forhold. Disse faktorene er avgjørende for hvordan enzymer fungerer i kroppen – og hvordan de reguleres.
Som for de fleste kjemiske reaksjoner, øker reaksjonshastigheten med økende temperatur – opp til et punkt. Enzymer har en optimal temperatur der de fungerer best (ofte rundt 37 °C hos mennesker), men ved for høye temperaturer denaturerer enzymet: det mister sin tredimensjonale struktur, og dermed også sin funksjon.
Enzymets struktur og ladningsforhold i det aktive setet er følsomt for pH. Hver enzymtype har et optimalt pH-område, og avvik fra dette kan føre til redusert aktivitet eller fullstendig inaktivering. For eksempel fungerer pepsin best i den sure pH-en i magesekken (~pH 2), mens trypsin i tynntarmen trives bedre i nøytralt miljø.
Som vi har sett med Michaelis-Menten-kinetikk, vil økt substratkonsentrasjon føre til økt reaksjonshastighet – opp til metningspunktet, hvor alle aktive seter er opptatt.
Regulering av enzymaktivitet i cellen
Celler har også flere sofistikerte mekanismer for å regulere enzymers aktivitet, både raskt og langsiktig. Dette gjør det mulig for kroppen å tilpasse stoffskiftet til ulike behov og miljøbetingelser.
Enzymkomplekser og organisering
Enzymer kan organiseres i store multi-enzymsystemer eller fysiske strukturer i cellen for å gjøre reaksjonskjeder mer effektive. Produktet fra ett enzym går rett videre som substrat for det neste – som på et samlebånd.
Genregulering
Cellen kan justere mengden enzym som produseres, enten ved å øke eller dempe transkripsjonen av genet som koder for enzymet. På lengre sikt kan enzymene også brytes ned og resirkuleres ved hjelp av proteasomer.
Substrat- og produktkonsentrasjon
Reaksjonsbalansen kan flyttes ved å øke mengden substrat eller fjerne produktet – et prinsipp basert på massevirkningsloven. Dette påvirker reaksjonens retning og hastighet.
Kovalente modifikasjoner
Enzymer kan aktiveres eller inaktiveres gjennom post-translasjonelle modifikasjoner, som fosforylering, metylering eller glykosylering. Dette skjer ofte via signalveier som styres av hormoner og andre signalmolekyler.
Post-translasjonelle modifikasjoner (PTMs)
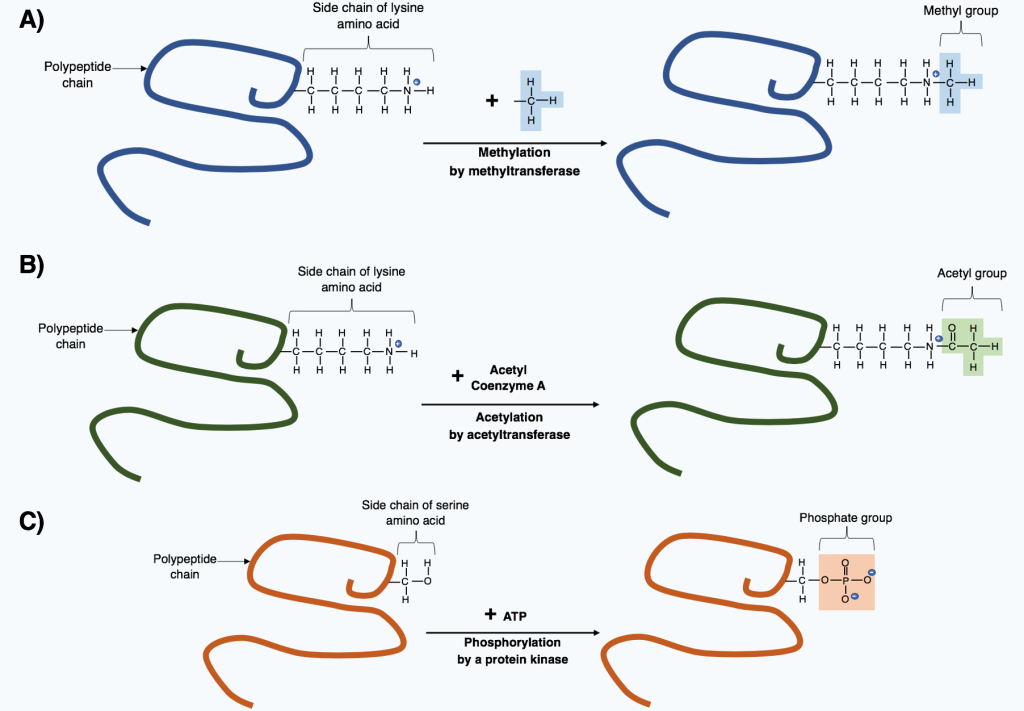
Et protein er ikke nødvendigvis «ferdig» i det øyeblikket det er syntetisert på ribosomet. I virkeligheten starter et nytt kapittel i proteinets liv etter translasjonen – nemlig den post-translasjonelle modifikasjonen. Post-translasjonelle modifikasjoner (PTMs) er kovalente endringer som skjer etter at et protein er oversatt fra mRNA. Disse modifikasjonene kan forandre proteinets skjebne dramatisk: fra hvor det skal lokaliseres i cellen, til hvor lenge det skal leve, og hvilke funksjoner det skal ha.
Man kan sammenligne PTMs med tilpasningene man gjør på et ferdigbygd hus: man legger til dører, maler veggene, og installerer elektrisitet – det er fortsatt det samme huset, men nå klart til å fungere i sitt miljø. På samme måte får proteinet nye kjemiske egenskaper som bestemmer dets biologiske rolle. Det finnes over 400 kjente typer PTMs, og mange proteiner gjennomgår flere av dem samtidig.
Eksempler på vanlige PTMs:
- Fosforylering er blant de mest studerte modifikasjonene. Her festes en fosfatgruppe til spesifikke aminosyrer, ofte serin, treonin eller tyrosin. Dette brukes til å skru enzymer «av» eller «på», og er sentralt i signaloverføring.
- Glykosylering innebærer at sukkergrupper festes til proteinet, ofte på nitrogen (N-glykosylering) eller oksygen (O-glykosylering). Dette påvirker både folding og transport av proteinet, og er helt avgjørende for celleoverflateproteiner og sekretoriske proteiner.
- Ubiquitinering innebærer at et lite protein kalt ubiquitin kobles til lysinrester på et protein, og fungerer som et molekylært «dødsstempel» som merker proteinet for nedbrytning i proteasomet.
- SUMOylation, som ligner på ubiquitinering, bruker et annet lite protein kalt SUMO. Dette påvirker i hovedsak proteinkomplekser, DNA-interaksjoner og lokalisering i cellekjernen.
- Lipidering knytter en fettsyre til proteinet, ofte for å feste det til cellemembranen. Dette er viktig for proteiner i signalveier.
- Metylering og acetylering skjer ofte på lysin- eller argininrester og brukes særlig i regulering av genuttrykk – for eksempel ved å modifisere histoner i DNA-pakking.
- Hydroksylering og disulfidbindinger påvirker proteinets struktur og stabilitet. Kollagen får sin mekaniske styrke gjennom hydroksylering, og disulfidbindinger (mellom cysteinrester) sørger for korrekt foldede, stabile proteiner.
Hva gjør PTMs så viktige?
PTMs er ikke tilfeldige pynt – de er nødvendige for at et protein skal virke riktig. De:
- Aktiverer eller deaktiverer enzymer
- Endrer proteinets struktur eller interaksjoner
- Styrer hvor i cellen proteinet skal gå
- Markerer det for nedbrytning eller resirkulering
I tillegg gir de cellen mulighet til å finregulere proteinaktivitet i sanntid, uten å måtte syntetisere nye proteiner fra bunnen av. Dette er særlig viktig i raskt skiftende miljøer og signalveier.
Enzymkomplekser – effektiv biokjemisk samarbeid
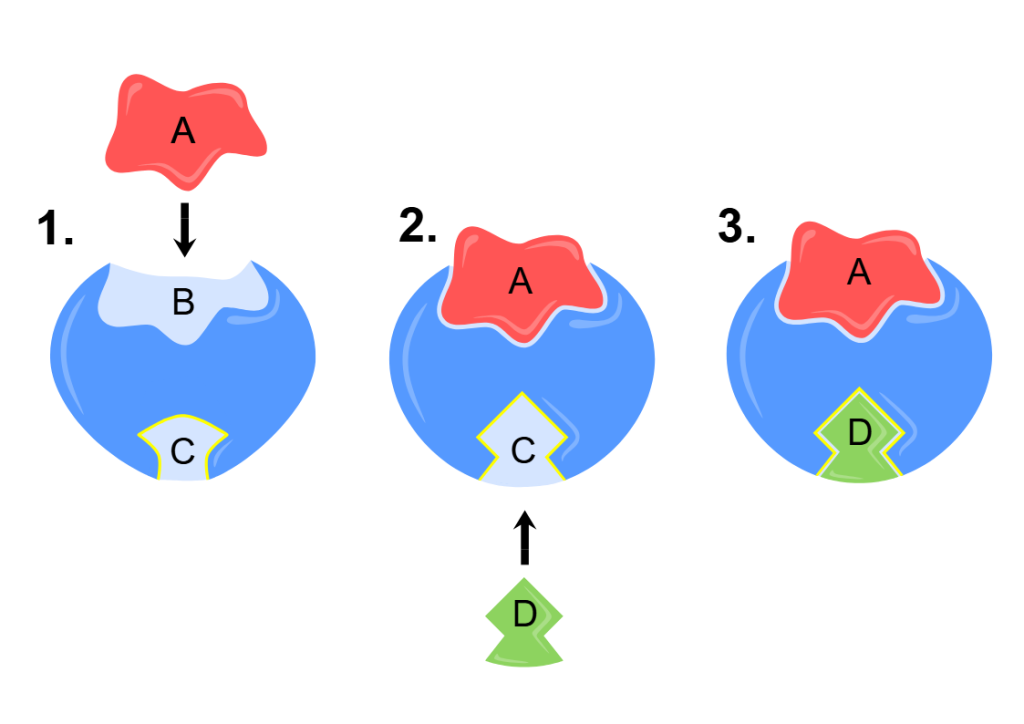
Enzymer arbeider sjelden alene. Ofte organiseres de i enzymkomplekser – funksjonelle enheter der flere enzymer samarbeider om å utføre påfølgende trinn i en reaksjonsvei. Dette gir cellen en rekke fordeler: høy effektivitet, beskyttelse av ustabile mellomprodukter, og tettere regulering.
Et enzymkompleks kan være bygget opp av:
- Identiske underenheter (homooligomer)
- Ulike underenheter med forskjellige funksjoner (heterooligomer)
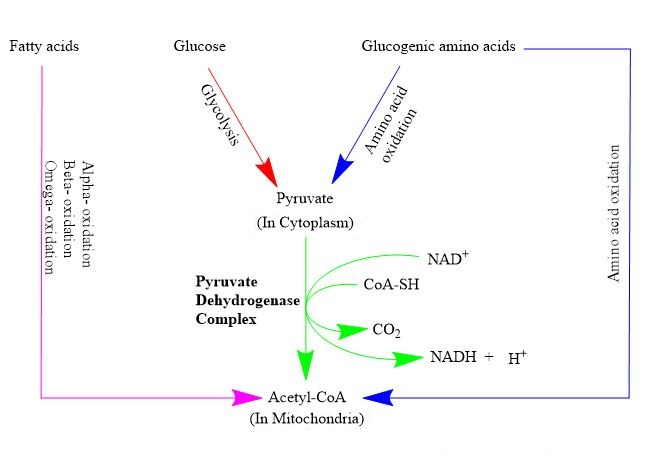
Et klassisk eksempel er pyruvatdehydrogenase-komplekset, som konverterer pyruvat til acetyl-CoA i mitokondriene. Her er tre ulike enzymer organisert sammen, og produktet fra ett trinn overføres direkte til det neste enzymet – uten å slippes fri i cytosol. Dette kalles ofte substratkanalisering, og bidrar til at reaksjonen blir både raskere og mer kontrollert.
Fordeler med enzymkomplekser:
- Effektivitet: Reaksjonstrinn skjer i rekkefølge, uten at molekylene må diffundere fritt mellom enzymene.
- Regulering: Hele komplekset kan aktiveres eller deaktiveres som en enhet.
- Energiutnyttelse: Strukturelle endringer i komplekset – ofte drevet av ATP-hydrolyse – kan påvirke aktiviteten til bestemte deler av systemet.
- Romlig organisering: Enzymkomplekser kan lokaliseres til spesifikke steder i cellen, som mitokondrier eller cytoskjelettet.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3
❓ Test deg selv
Obs, tomt! Kommer etterhvert <3