Cellen er ikke en tilfeldig samling av molekyler, men en organisert og dynamisk helhet, der hvert protein må være på rett sted til rett tid for at alt skal fungere. Etter at et protein er produsert, er det sjelden ferdig med reisen sin. I stedet må det transporteres videre til et bestemt sted i cellen – enten det skal jobbe i cellekjernen, i mitokondriene, i plasmamembranen eller kanskje til og med skilles ut av cellen.
Denne interne transporten er helt avgjørende.
Et enzym som er ment å delta i DNA-reparasjon i cellekjernen, vil være verdiløst – eller til og med farlig – hvis det havner i cytoplasma. Et membranprotein som skal sitte i overflaten og sende signaler fra omverdenen, må fraktes via et nøye regulert nettverk av vesikler og mellomstasjoner. Og proteiner som skal brytes ned, må sendes til lysosomer – cellens nedbrytningsstasjoner – ikke bli liggende og hope seg opp.
For å klare dette har cellen utviklet et komplekst system for å dirigere proteiner dit de skal. Den intracellulære proteintransporten fungerer som et logistikknettverk – nesten som et postsystem, der hvert protein har en innebygd «adresse» i form av en aminosyresekvens. Basert på denne adressen velger cellen riktig transportmekanisme: noen proteiner fraktes gjennom porer, andre trenger å pakkes inn i små membranbobler, og noen må trekkes gjennom membraner ved hjelp av spesielle porter.
Det finnes ikke én felles vei – det finnes flere. Avhengig av hvor proteinet skal, benytter cellen ulike strategier. Det som gjør dette ekstra imponerende, er at alt dette skjer kontinuerlig og parallelt i tusenvis av proteiner, samtidig, i hver eneste levende celle.
Å forstå hvordan denne transporten fungerer er ikke bare viktig for å forstå hvordan cellen er bygget opp. Det gir også innsikt i sykdommer, medisiner og hvordan virus kaprer cellens egne transportsystemer for å spre seg. Men først og fremst viser det hvor ufattelig koordinert og intelligent en levende celle faktisk er.
Hvordan vet cellen hvor et protein skal?
Når et protein blir syntetisert, er det bare en kjede av aminosyrer som ennå ikke vet hvor den hører hjemme. Likevel klarer cellen på en effektiv måte å sende hvert protein til riktig destinasjon. Hvordan er det mulig?
Svaret ligger i små, men presise adresser som ligger gjemt i selve aminosyresekvensen. Disse kalles sorteringssignaler, og de fungerer som postkoder – korte sekvenser av aminosyrer som forteller cellen hvor proteinet skal leveres.
De kan for eksempel angi at et protein skal til mitokondriene, til kjernen, til lysosomer eller til plasmamembranen. Noen signaler sitter i begynnelsen av proteinet, andre i midten, og noen i enden. Noen ganger består signalet av bare noen få aminosyrer, mens andre ganger handler det mer om strukturen proteinet folder seg i.
Disse sorteringssignalene gjenkjennes av egne transportproteiner og reseptorer i cellen, som igjen setter i gang den riktige transportmekanismen. Hvis et protein mangler et slikt signal, blir det som oftest værende i cytoplasma. Det er standarddestinasjonen – som å ikke skrive på adressen og la brevet ligge igjen på postkontoret.
I noen tilfeller er signalet permanent og uforanderlig – proteinet går alltid til samme sted. Men i andre tilfeller kan sorteringssignalet aktiveres eller maskeres, avhengig av cellens behov. På den måten kan cellen regulere hvor og når et protein skal utføre sin funksjon.
I tillegg til selve sorteringssignalet, spiller også det cellulære miljøet en rolle. For eksempel krever mange transportprosesser energi, og enkelte transportveier er avhengige av spesielle hjelpemolekyler, såkalte chaperoner, som holder proteinet i en ufoldet tilstand underveis.
Det finnes altså ikke én universell vei som alle proteiner følger. I stedet finnes det flere parallelle og spesialiserte ruter i cellens indre transportsystem. De tre viktigste prinsippene for intracellulær transport er:
- Gated transport – gjennom spesialiserte porer, for eksempel til og fra cellekjernen
- Transmembran transport – gjennom membraner inn i organeller som mitokondrier eller ER
- Vesikulær transport – der proteiner pakkes inn i små blærer og fraktes fra et sted til et annet
I de neste delene går vi gjennom hver av disse hovedtypene og ser hvordan cellen bruker dem for å flytte proteiner effektivt og målrettet.
Gated transport – inn og ut av cellekjernen
Cellekjernen er cellens kontrollsenter, der DNA ligger lagret og transkriberes til mRNA. For at kjernen skal fungere, må det være en nøye regulert utveksling av stoffer mellom kjernen og cytoplasma. RNA må ut, og mange proteiner må inn. Dette skjer gjennom en spesialisert transportmekanisme kalt gated transport – en slags selektiv portvakt mellom kjernen og resten av cellen.
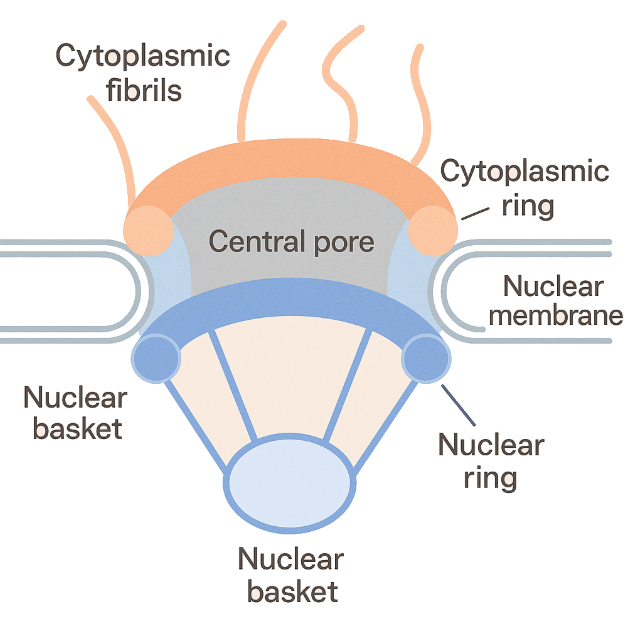
Kjernen er omgitt av en dobbel membran, og i denne membranen finner vi tusenvis av små åpninger kalt kjerneporer. Men dette er ikke bare hull – kjerneporene er komplekse og dynamiske strukturer bygget opp av mange ulike proteiner, og de fungerer som aktive porter som regulerer hva som får passere.
Små molekyler, som ioner og enkelte metabolitter, kan passere fritt gjennom kjerneporene. Men større molekyler – som proteiner og RNA – krever aktiv transport. For at et protein skal få komme inn i kjernen, må det bære med seg et spesifikt signal – en nukleær lokaliseringssekvens (NLS).
Dette er en kort aminosyresekvens som fungerer som adgangstegn.
Transporten skjer via egne reseptorer, kalt importiner, som gjenkjenner NLS og frakter proteinet inn gjennom poren. På samme måte finnes det exportiner som frakter RNA og visse proteiner ut av kjernen igjen.
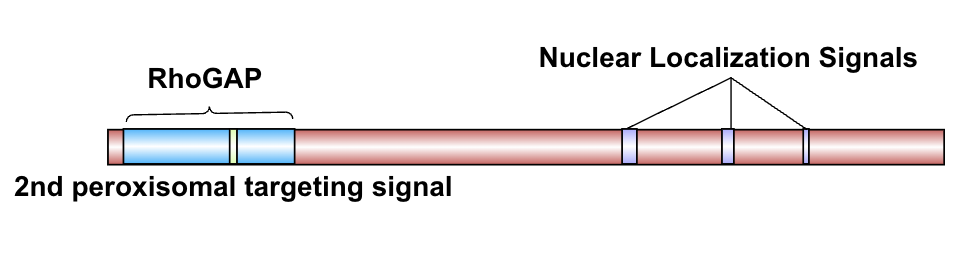
Denne transporten er ikke bare selektiv – den er også energikrevende.
Den drives av små GTP-bindende proteiner, særlig Ran, som finnes i ulike former på hver side av kjerneporen. Ran fungerer som en molekylær bryter som gir retning og retursikkerhet: import skjer én vei, eksport den andre. Dette skaper et asymmetrisk miljø som gjør at transporten går målrettet, og ikke i begge retninger samtidig.
Gated transport gjør det mulig for cellen å skille tydelig mellom det som foregår i kjernen og det som skjer i cytoplasma. Det gir cellen kontroll over hvilke transkripsjonsfaktorer som får tilgang til DNA, og når RNA får forlate kjernen og delta i proteinsyntesen. Ved å regulere åpningen og lukningen av portene, og ved å bestemme hvilke signaler som gir adgang, kan cellen justere genuttrykket sitt i sanntid – og dermed svare raskt på både indre behov og ytre påvirkninger.
Eksempel: NF-AT – signalstyrt import til kjernen i T-celler
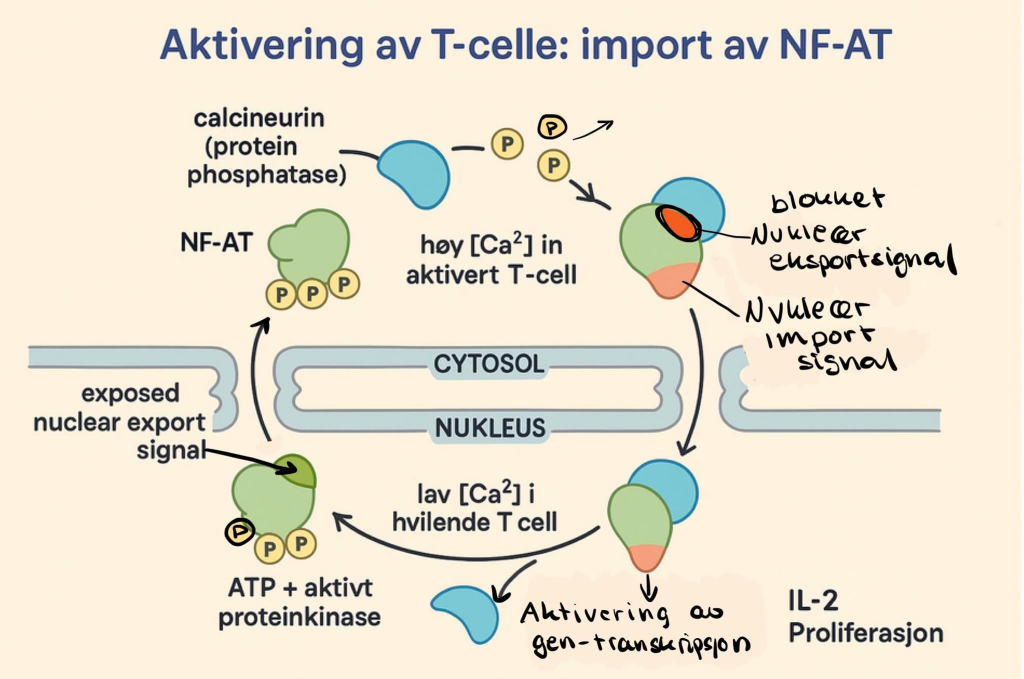
Et godt eksempel på gated transport i praksis finner vi i immuncellene våre, nærmere bestemt T-cellene. Når en T-celle er i hvile, befinner et viktig reguleringsprotein kalt NF-AT (nuclear factor of activated T-cells) seg inaktivt i cytoplasma. Det er fosforylert, noe som betyr at det har flere fosfatgrupper bundet til seg. Disse fosfatene skjuler det nukleære importsignalet og holder NF-AT ute i cytosol.
Men når T-cellen aktiveres, for eksempel ved kontakt med en fremmed mikroorganisme, øker nivået av Ca²⁺ inne i cellen.
Dette kalsiumsignalet aktiverer et enzym kalt calcineurin, som fungerer som en fosfatase. Den fjerner fosfatgruppene fra NF-AT – en prosess som kalles defosforylering. Når dette skjer, endres hele signalbalansen i proteinet: importsignalet blir synlig, eksportsignalet blokkeres, og NF-AT kan nå fraktes inn i cellekjernen gjennom kjerneporene.
Vel inne i kjernen binder NF-AT seg til DNA og skrur på gener som er viktige for immunresponsen, som for eksempel IL-2, som stimulerer T-celleproliferasjon.
Denne mekanismen er også klinisk relevant. Legemidler som cyclosporin A og FK506 (tacrolimus) hemmer calcineurin og forhindrer dermed at NF-AT går inn i kjernen. Dette brukes blant annet ved organtransplantasjoner for å dempe immunreaksjoner og forhindre avstøtning.
Transmembran transport – gjennom membraner til indre organeller
Ikke alle proteiner som lages i cellen skal bli værende i cytoplasma eller sendes til cellekjernen. Mange proteiner har oppgaver inne i organeller som endoplasmatisk retikulum (ER), mitokondrier eller peroksisomer.
For å komme dit må de krysse membranen som omslutter disse organellene – og det gjør de gjennom en transportform som kalles transmembran transport.
Dette er en direkte transport gjennom en membran, men i motsetning til gated transport, der poren holder seg åpen nok til at hele proteinet kan passere, krever transmembran transport som regel at proteinet tres gjennom en spesialisert kanal eller port – ofte mens det fortsatt er ufoldet. Det betyr at proteinet holdes i en lang, trådaktig form av egne hjelpeproteiner kalt chaperoner, som forhindrer at det folder seg sammen for tidlig.
Proteiner som skal inn i mitokondrier, kloroplaster (i planteceller) eller peroksisomer, har egne sorteringssignaler som gjenkjennes av reseptorer på overflaten av organellen. Disse reseptorene leder proteinet til et translokasjonskompleks – et slags proteinhull i membranen – som kan åpnes for å slippe proteinet gjennom.
Et godt eksempel er mitokondriet, som har både en ytre og en indre membran. Proteiner som skal inn i mitokondriematrixen må derfor krysse to membraner. Dette skjer gjennom en koordinert overlevering mellom transportkomplekser i den ytre og den indre membranen. Prosessen krever energi, ofte i form av både ATP og membranpotensial, og involverer flere ulike chaperoner som holder proteinet i riktig tilstand underveis.
Noen organeller, som det ru endoplasmatiske retikulumet (rER), tar imot proteiner mens de fortsatt blir syntetisert. I slike tilfeller skjer transmembran transport ko-translasjonelt, altså samtidig med at proteinet lages av ribosomet. Ribosomet fester seg direkte til ER-membranen, og det voksende proteinet føres rett inn i ER gjennom en kanal kalt translokon. Når hele proteinet er inne, kan det foldes, få disulfidbindinger og modifiseres videre – ofte ved å få påsatt sukkerkjeder (glykosylering).
Transmembran transport er dermed ikke bare en enkel gjennomfart. Det er en kompleks og presis prosess som sikrer at proteiner ikke bare kommer til riktig organelle, men også i riktig tilstand, med korrekt folding og modifikasjoner som gjør dem funksjonelle.
Uten denne typen transport ville cellens organeller være tomme skall – uten spesialiserte enzymer og strukturer som gir dem funksjon. Transmembran transport er derfor avgjørende for at cellen skal være mer enn bare en væskefylt pose – den gjør det mulig å ha indre rom med egne oppgaver og miljøer.
Vesikulær transport
Mange proteiner har en reiserute som ikke bare går til én spesifikk organelle, men som krever at de fraktes mellom flere stasjoner i cellens indre.
Dette gjelder særlig proteiner som skal til plasmamembranen, til lysosomer, eller som skal skilles ut av cellen. For slike reiser benytter cellen et avansert transportsystem basert på små membranblærer, kalt vesikler. Denne typen transport kalles vesikulær transport.
Vesikulær transport fungerer omtrent som et postsystem med pakker og leveranser. Først pakkes proteiner inn i små membranblærer som avsnøres fra en donororganelle, for eksempel det endoplasmatiske retikulum eller Golgiapparatet.
Disse blærene – vesiklene – fraktes deretter gjennom cytoplasma og smelter sammen med membranen til målorganellen, slik at innholdet kan leveres dit det skal.
Prosessen starter med at spesifikke proteiner i membranen markerer stedet hvor vesikkelen skal dannes.
Disse rekrutterer coat-proteiner, som clathrin, COPI eller COPII, som legger seg som et ytre lag rundt membranen og former en kulelignende struktur. Når vesikkelen er formet, snøres den av fra membranen, ofte med hjelp av motorproteiner og energikrevende prosesser.
Etter at vesikkelen har løsnet fra sin opprinnelse, må den finne frem til riktig mål. Dette styres av små GTPaser (som Rab-proteiner) og spesialiserte SNARE-proteiner, som fungerer som molekylære adresser og låser.
V-SNARE-proteiner på vesikkelens overflate gjenkjennes av t-SNARE-proteiner på målmembranen. Når riktig match oppstår, smelter vesikkelen sammen med målet, og innholdet tømmes ut – enten inni organellet eller ut av cellen.
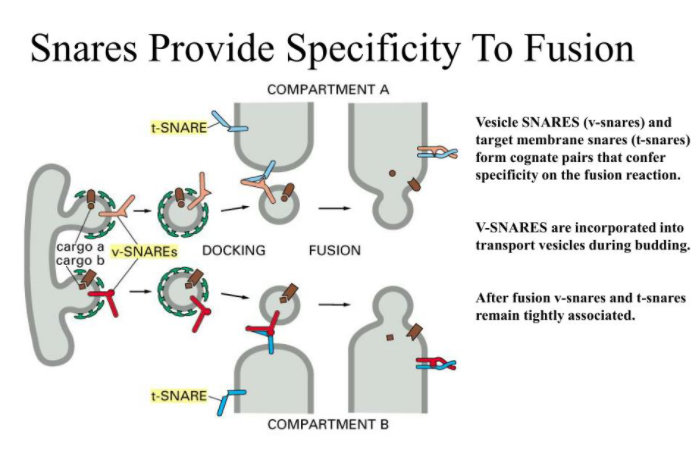
Et klassisk eksempel på vesikulær transport er det som skjer med proteiner som først syntetiseres i det ru endoplasmatiske retikulum, så pakkes i vesikler og sendes til Golgiapparatet for videre modifisering, og deretter videre til plasmamembranen eller lysosomer.
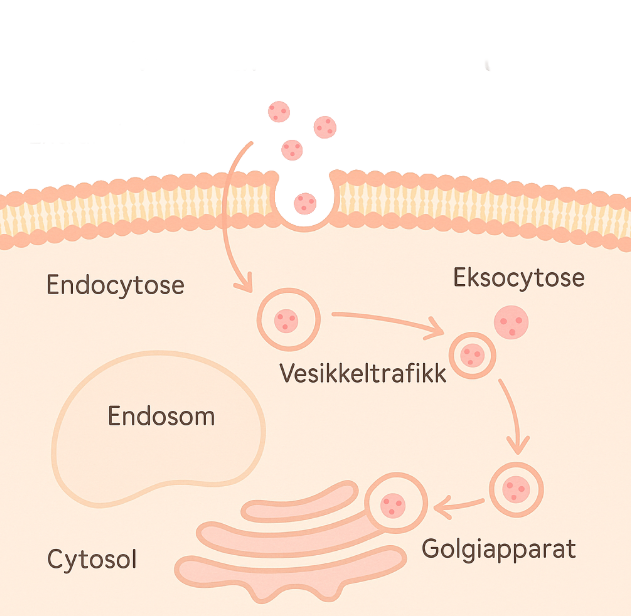
Denne typen transport er også helt avgjørende for eksocytose – der proteiner eller signalstoffer slippes ut av cellen – og for endocytose, der cellen tar opp stoffer fra omgivelsene ved å omslutte dem i membranblærer.
Vesikulær transport gjør det altså mulig å flytte både løselige proteiner og membranproteiner over større avstander i cellen, uten at de trenger å krysse lipidmembraner direkte. I stedet tas hele pakken med, inkludert membransegmentet det sitter i, og leveres hel til neste stoppested. Dette gir cellen en imponerende kontroll over hvor, når og hvordan proteiner lokaliseres og aktiveres.
Endocytose og eksocytose – når cellen tar inn og sender ut
Celler er ikke isolerte enheter. De må hele tiden utveksle stoffer med omgivelsene – ta opp næringsstoffer, svare på signaler, kvitte seg med avfall og sende beskjeder til andre celler. Til dette bruker cellen ikke bare ionekanaler og transportproteiner i membranen, men også vesikulær transport på membrannivå. Når hele vesikler dannes fra eller smelter sammen med plasmamembranen, snakker vi om endocytose og eksocytose.
Endocytose – når cellen tar opp
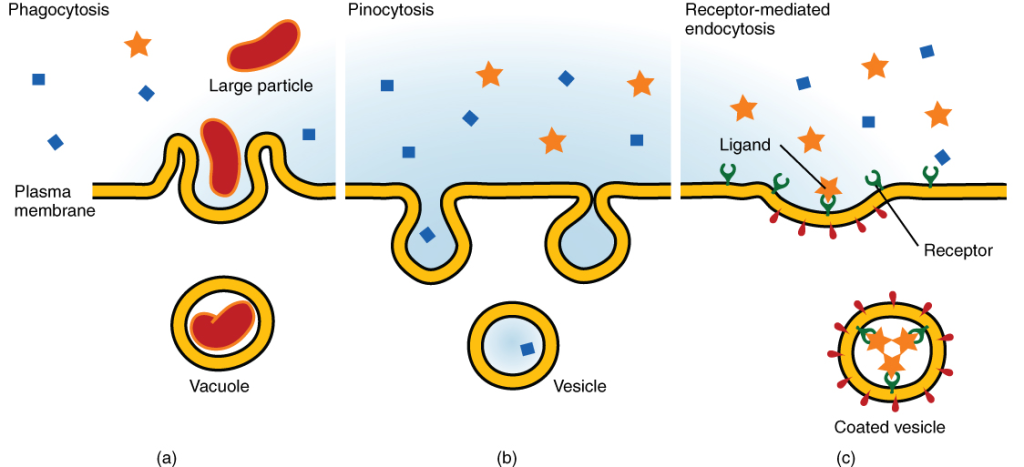
Endocytose er prosessen der cellen tar inn stoffer fra utsiden ved å omslutte dem med cellemembranen og danne en vesikkel som trekkes inn i cytoplasma. Dette gjør at større molekyler – som proteiner, lipider eller hele bakterier – kan tas opp, noe som ellers ikke ville vært mulig via kanaler eller transportproteiner.
Det finnes flere varianter av endocytose. I fagocytose – «celle-spising» – omslutter cellen store partikler som bakterier eller cellefragmenter, og danner store vesikler kalt fagosomer. Dette er vanlig hos immunceller som makrofager. I pinocytose – «celle-drikking» – tas væske og oppløste stoffer opp i små vesikler, ofte uten spesifisitet. Og i reseptormediert endocytose binder spesifikke molekyler seg til reseptorer på celleoverflaten, noe som trigger dannelsen av en vesikkel. Et godt eksempel på dette er opptaket av LDL-kolesterol fra blodet, som skjer via LDL-reseptorer og clathrindekkede vesikler.
Etter at vesikkelen er dannet, smelter den ofte sammen med endosomer, og innholdet kan sorteres videre – til resirkulering, nedbrytning i lysosomer, eller transport videre innover i cellen.
Eksocytose – når cellen sender ut
Eksocytose er det motsatte av endocytose: cellen skiller ut stoffer ved å fusjonere intracellulære vesikler med plasmamembranen. Dette er en vanlig måte å frakte proteiner ut av cellen på, spesielt de som er produsert i det endoplasmatiske retikulum og bearbeidet i Golgiapparatet.
Eksocytose kan være konstitutiv, altså kontinuerlig og uten spesifikke signaler – som ved utskillelse av visse enzymer eller komponenter i ekstracellulær matriks.
Men den kan også være regulert, slik som i nerveceller og hormonproduserende celler, der signaler som økt kalsiumkonsentrasjon utløser en rask fusjon av vesikler med membranen og frigjøring av innholdet – som nevrotransmittere eller insulin.
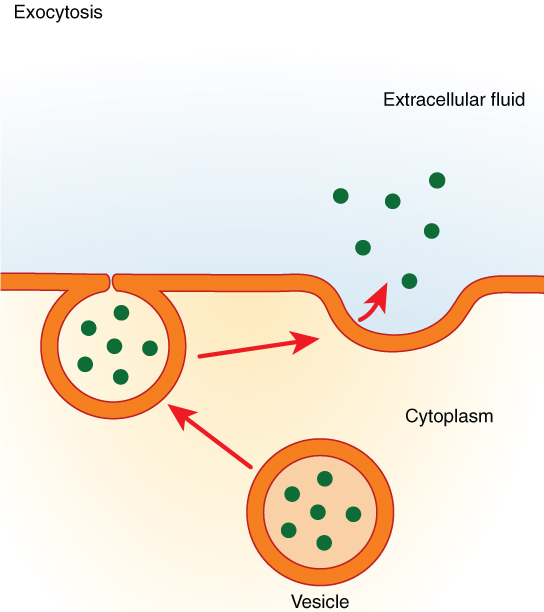
I begge tilfeller tilfører vesikkelfusjonen ikke bare innhold til utsiden av cellen, men også nytt membranmateriale til plasmamembranen. Det betyr at eksocytose bidrar til å regulere membranens areal og sammensetning, i tillegg til sin rolle i kommunikasjon og utskillelse.
Til sammen gir endocytose og eksocytose cellen en dynamisk forbindelse med omverdenen. Ikke bare kan cellen ta inn informasjon og næringsstoffer, den kan også forme miljøet rundt seg, sende signaler og regulere sin egen størrelse og membranstruktur. Dette gjør vesikkeltransporten til et levende, fleksibelt grensesnitt mellom cellens indre og resten av kroppen.
Transmembran transport til mitokondrier og endoplasmatisk retikulum
Når et protein skal fraktes inn i et organelle som mitokondriene eller det endoplasmatiske retikulum (ER), krever det spesifikke signaler og spesialiserte transportmekanismer. Disse systemene er nøye tilpasset hver sin organelle og gjør det mulig å plassere hvert protein nøyaktig der det trengs.
Import til mitokondriene
Mange av mitokondrienes proteiner blir faktisk syntetisert i cytoplasma, selv om mitokondriene har sitt eget DNA.
For at disse proteinene skal havne i riktig mitokondrielt rom, må de først merkes med en signal-sekvens, en slags adressekode som gjenkjennes av importmaskineriet i mitokondriemembranen.
Først bindes proteinet til en importreseptor på den ytre membranen.
Derfra ledes det inn i et proteinkompleks kalt TOM-komplekset (Translocase of the Outer Membrane), som åpner en kanal inn gjennom membranen. Hvis proteinet skal helt inn i mitokondriematrixen, sendes det videre gjennom TIM-komplekset (Translocase of the Inner Membrane), som finnes i den indre mitokondriemembranen.
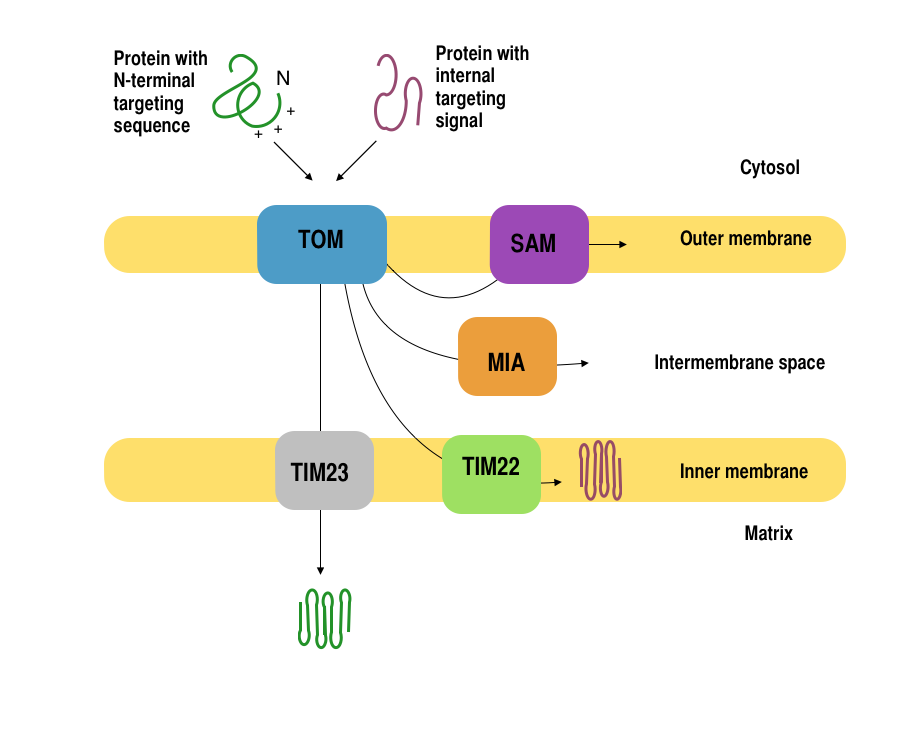
Proteinet holdes ufoldet underveis ved hjelp av chaperoner og trekkes aktivt inn, ofte drevet av ATP og membranpotensial. Når det når frem til sin destinasjon, blir signal-sekvensen vanligvis klippet av, og proteinet kan folde seg til sin aktive form.
Noen proteiner skal ikke helt inn i matriksen, men stoppes halvveis og integreres i den indre mitokondriemembranen, takket være en såkalt stop-transfer-sekvens. Andre skal tilbakeføres til membranen etter å ha blitt fullstendig importert, og dette skjer via OXA-komplekset, som er ansvarlig for å sette inn visse proteiner i den indre membranen – ofte proteiner som er produsert inne i mitokondriene selv.
Proteiner som skal havne i intermembranrommet – mellom de to membranene – kan også følge TOM-ruten, men blir delvis kløyvd slik at de frigjøres til rommet mellom membranene. Og til slutt finnes det også en egen vei for proteiner som skal til den ytre mitokondriemembranen, hvor SAM-komplekset sørger for at de foldes riktig og forankres i membranen.
Ko-translasjonell import til endoplasmatisk retikulum (ER)
Mens proteiner til mitokondriene fraktes post-translasjonelt (etter at de er laget), skjer transport til ER mens proteinet lages – det vi kaller ko-translasjonell transport.
Det hele begynner med at ribosomet starter å syntetisere et protein som har en ER-signal-sekvens i starten. Denne sekvensen gjenkjennes av et molekyl som flyter fritt i cytosol, kalt signal recognition particle (SRP). Når SRP binder til signal-sekvensen, stopper det midlertidig proteinsyntesen, og fører ribosomet til en SRP-reseptor på ER-membranen. Her dockes ribosomet, og SRP frigjøres.
Samtidig åpnes en kanal i ER-membranen, kalt translokon (oftest dannet av proteinkomplekset Sec61), og ribosomet fortsetter å lage proteinet – som da føres rett inn i ER-lumen mens det syntetiseres. Dette gjør at proteiner kan foldes, modifiseres og glykosyleres mens de fraktes inn.
Proteiner som er ment å sitte fast i ER- eller plasmamembranen, inneholder egne stop-transfer-sekvenser som stopper translasjonen og lar delen av proteinet bli værende i membranen.
Feilfolding og degradering – cellens kvalitetskontroll
Proteiner må foldes riktig for å kunne fungere. Strukturen deres – og ikke bare aminosyrerekkefølgen – avgjør hva de kan gjøre i cellen. Dersom et protein ikke klarer å foldes korrekt, risikerer det å bli ubrukelig eller til og med skadelig. Akkurat som en nøkkel som er bøyd eller deformert, vil et feilfoldet protein ofte ikke passe i de «låsene» det skal virke på – og i noen tilfeller kan det klumpe seg sammen og forstyrre hele cellens indre balanse.
For å unngå dette har cellen et avansert system for kvalitetskontroll, som begynner allerede i det endoplasmatiske retikulum (ER). Her overvåker egne proteiner – kalt chaperoner – om nylig syntetiserte proteiner folder seg riktig. Chaperonene fungerer som små molekylære hjelpere som kan binde seg til ustabile proteiner, beskytte dem, og hjelpe dem med å finne riktig tredimensjonal form. Dersom foldingen lykkes, får proteinet fortsette sin vei i cellen. Men dersom det fortsatt er ustabilt, kan chaperonene forsøke å rette det opp igjen – ofte gjennom flere forsøk.
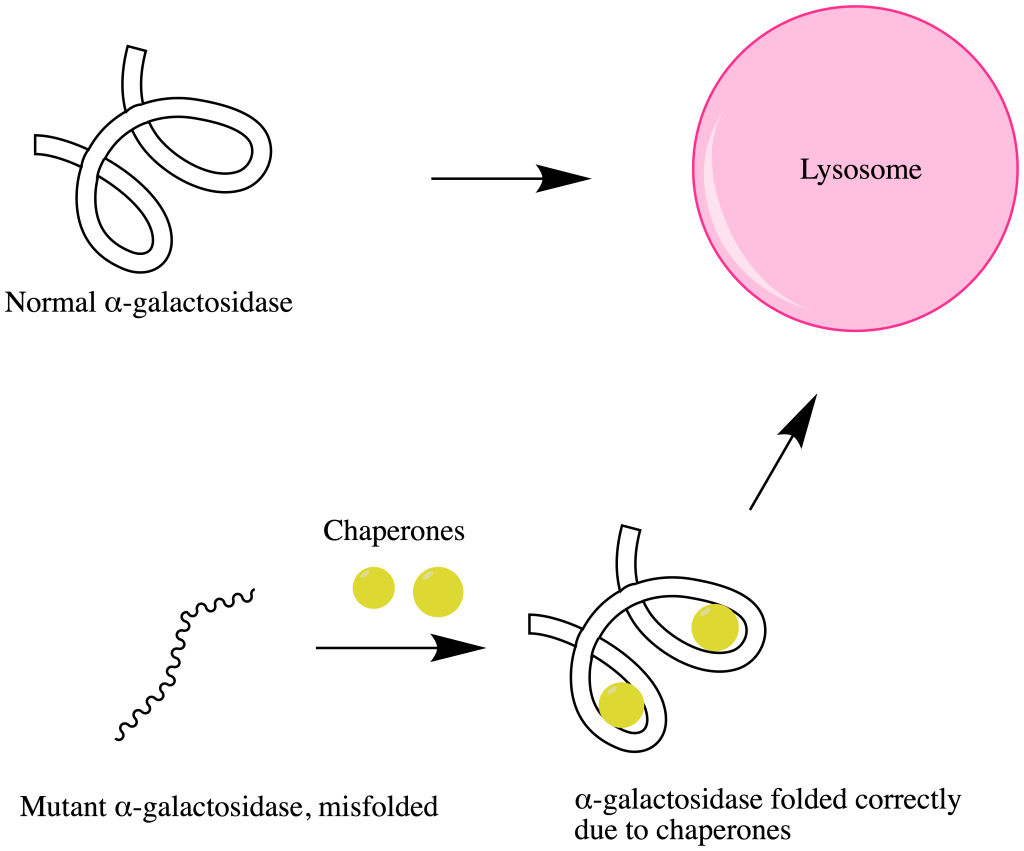
Når det blir klart at et protein ikke kan reddes, blir det sendt tilbake ut av ER og inn i cytosol. Der merkes det med et lite signalmolekyl kalt ubiquitin – et slags molekylært «klistrelapp» som sier: «dette skal ødelegges». Selve prosessen der ubiquitin festes til målet kalles ubiquitinering, og involverer flere spesialiserte enzymer. Når proteinet har fått nok ubiquitin-merker på seg, blir det gjenkjent av et stort nedbrytningskompleks kalt proteasomet.
Proteasomet er som en sylindrisk søppelkvern: det trekker proteinet inn, fjerner og resirkulerer ubiquitin, og bryter proteinet ned til små peptider. Dette hindrer opphopning av ødelagte eller potensielt toksiske proteiner, og gir samtidig cellen byggesteiner tilbake som kan brukes på nytt.
Men proteasomet er ikke den eneste veien til nedbrytning. Dersom et protein er for stort, aggregert, eller hvis det er mange skadede proteiner samtidig, kan cellen i stedet bruke autofagi – en annen nedbrytningsvei. Her pakkes skadede proteiner inn i en dobbel membran, kalt et autofagosom, som deretter smelter sammen med et lysosom. Inne i lysosomet finnes det sterke enzymer som bryter ned innholdet fullstendig.
Tilsammen sørger disse mekanismene – chaperoner, ubiquitin-proteasomet og autofagi – for at cellen hele tiden rydder opp i egne feil. Det er som et automatisert kontroll- og vedlikeholdssystem som sikrer at bare funksjonelle proteiner får lov til å bli. Når disse systemene svikter, kan det føre til alvorlige sykdommer, som nevrodegenerative tilstander (f.eks. Alzheimers) der feilfoldede proteiner hoper seg opp i hjernen.
Klinisk relevans – viktig
Intracellulær proteintransport er ikke bare en fascinerende biologisk prosess – den er også klinisk høyst relevant. Når transportveiene svikter, eller når proteiner ikke blir korrekt foldet og sortert, kan det få alvorlige konsekvenser for hele organismen.
Et tydelig eksempel er sykdommen cystisk fibrose (husk dette), som skyldes en mutasjon i genet for CFTR-proteinet – en kloridkanal som skal transporteres til plasmamembranen i epitelceller.
Mutasjonen fører til at proteinet foldes feil, selv om det egentlig kunne ha fungert dersom det nådde frem. I stedet holdes det tilbake i endoplasmatisk retikulum, og blir til slutt degradert via proteasomet. Resultatet er at cellene mangler CFTR-kanalen i membranen, og det oppstår problemer med væske- og saltbalanse i luftveiene, noe som fører til seigt slim, kroniske infeksjoner og redusert lungefunksjon.
Ikke glem cystisk fibrose, det er et erke-spørsmål på eksamener.
Et annet eksempel er Alzheimers sykdom, der feilfoldede proteiner som beta-amyloid og tau ikke blir fjernet effektivt. Disse danner aggregater som hoper seg opp i hjernen og forstyrrer nevronenes funksjon. Her spiller både proteasomets kapasitet og autofagisystemets effektivitet en rolle – og når disse systemene overbelastes eller svikter, kan det være starten på nevrodegenerasjon.
Flere virus, inkludert HIV og influensa, har også utviklet evner til å kapre cellens eget transportsystem for å komme seg inn, spre seg og unngå immunforsvaret. Noen virus bruker endocytose for å entre cellen, mens andre manipulerer vesikkeltransport for å eksportere sine egne proteiner og bygge viruspartikler.
I immunmedisin brukes kunnskap om proteintransport målrettet. For eksempel hemmer legemidler som cyklosporin A og FK506 enzymet calcineurin i T-celler. Dette hindrer defosforylering og kjerneimport av transkripsjonsfaktoren NF-AT, og demper dermed aktiveringen av T-celler. Det gjør disse legemidlene svært nyttige ved organtransplantasjoner, hvor man ønsker å undertrykke immunforsvaret og forhindre avstøting.
Selv kreft er i noen tilfeller knyttet til feil i proteindistribusjon og -nedbrytning. Dersom en celle unngår degradering av muterte eller skadelige proteiner, kan den begynne å vokse ukontrollert. Derfor forskes det stadig mer på hvordan man kan påvirke proteasomets aktivitet i kreftbehandling – for eksempel med proteasomhemmere i behandling av myelomatose.
Begrepsliste
Sorteringssignal / signal-sekvens
En kort aminosyresekvens som fungerer som proteinets «adressekode» og avgjør hvor i cellen det skal transporteres.
Gated transport
Transport mellom cytosol og cellekjernen gjennom kjerneporer. Krever spesifikke import- eller eksport-signaler.
Kjerneporekomplekset
Et stort proteinrikt kompleks i den nukleære membranen som regulerer trafikk inn og ut av cellekjernen.
Importin / exportin
Transportproteiner som frakter molekyler inn i (importin) eller ut av (exportin) cellekjernen via kjerneporer.
Transmembran transport
Transport gjennom en membran og inn i organeller som mitokondrier eller ER, vanligvis via egne kanalproteiner.
Chaperoner
Hjelpeproteiner som forhindrer feilfolding og holder proteiner i ufoldet tilstand under transport.
TOM-komplekset
Translocase of the Outer Membrane. Kanal i ytre mitokondriemembran som slipper proteiner inn i mitokondriet.
TIM-komplekset
Translocase of the Inner Membrane. Transportkanal i den indre mitokondriemembranen som fører proteiner inn i matriksen.
OXA-komplekset
Et transportkompleks som setter inn proteiner i den indre mitokondriemembranen, ofte proteiner som er syntetisert inne i mitokondriet selv.
SAM-komplekset
Kompleks i ytre mitokondriemembran som hjelper visse proteiner å integreres korrekt i membranen.
Signal Recognition Particle (SRP)
Et molekyl som gjenkjenner signal-sekvensen på proteiner som skal til ER og stopper proteinsyntesen midlertidig.
Translokon (Sec61-komplekset)
En kanal i ER-membranen som lar proteiner komme inn i ER mens de fortsatt blir laget av ribosomet.
Vesikkel
En liten membranblære som frakter proteiner mellom organeller eller til celleoverflaten.
Clathrin, COPI, COPII
Forskjellige coat-proteiner som former og stabiliserer vesikler ved vesikkeldannelse.
SNARE-proteiner
Proteiner som sikrer at vesikkelen smelter sammen med riktig målmembran.
Endocytose
Prosess der cellen tar opp materiale fra utsiden ved å omslutte det med plasmamembranen.
Eksocytose
Prosess der cellen skiller ut stoffer ved at vesikler smelter sammen med plasmamembranen.
Ubiquitin
Et lite protein som festes til feilfoldede eller uønskede proteiner for å merke dem for nedbrytning.
Proteasomet
Et stort proteinkompleks i cytosol som bryter ned ubiquitin-merkede proteiner.
Autofagi
En prosess der cellen pakker inn skadet materiale i en membranstruktur (autofagosom) og sender det til lysosomet for nedbrytning.
NF-AT
En transkripsjonsfaktor som aktiveres i T-celler ved økt Ca²⁺ og fraktes inn i kjernen for å aktivere immunrelaterte gener.
Calcineurin
Et enzym som aktiveres av kalsium og defosforylerer NF-AT, slik at det kan fraktes inn i cellekjernen.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3