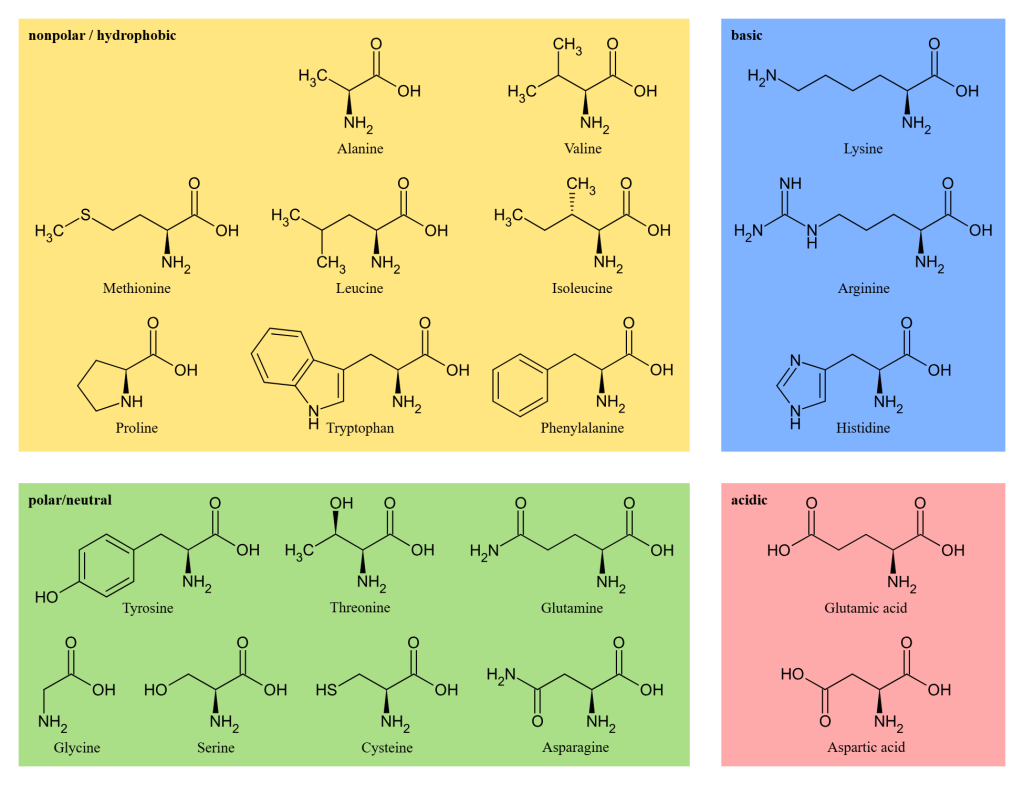
Aminosyrer – byggesteinene i proteinene
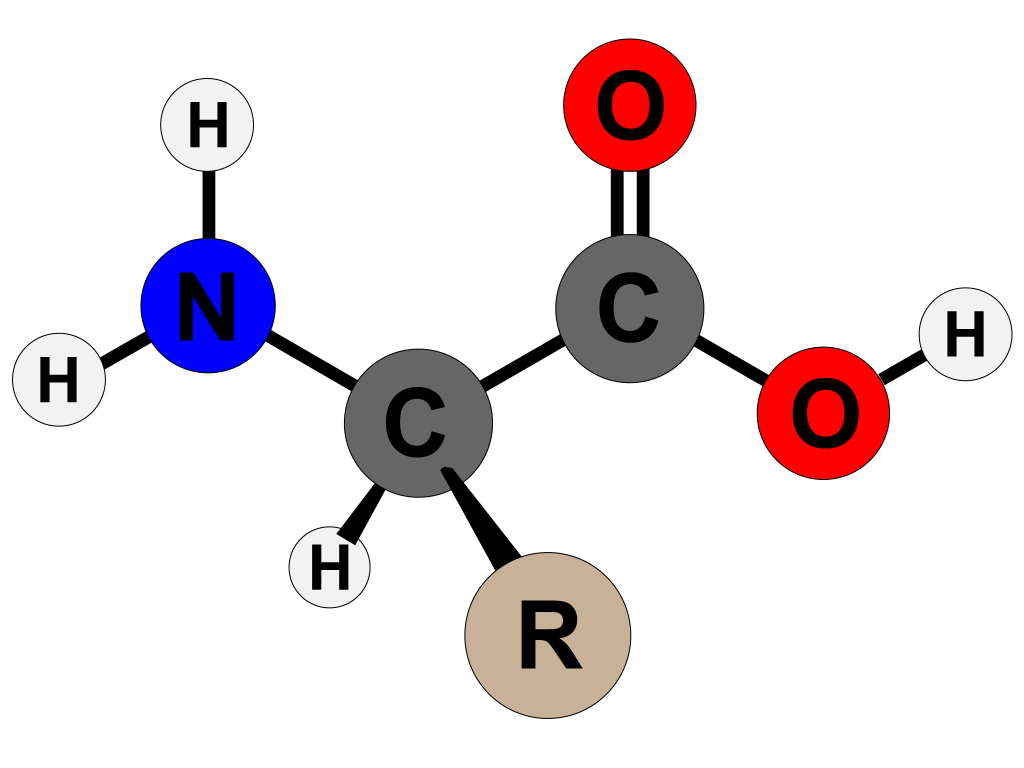
Alle proteiner i kroppen vår er bygd opp av aminosyrer, små organiske molekyler med en struktur som gjør dem unike. Hver aminosyre består av en sentral karbonatom, kalt alfa-karbonet, som danner kjernen i molekylet. Til dette karbonatomet er det festet fire grupper:
- En aminogruppe (-NH₂)
- En karboksylsyregruppe (-COOH)
- Et hydrogenatom
- En sidekjede (R-gruppe), som varierer mellom ulike aminosyrer
Det er denne sidekjeden som bestemmer aminosyrens individuelle egenskaper. Noen sidekjeder er polare og vannløselige, mens andre er upolare og hydrofobe. Noen bærer elektrisk ladning – og dette har stor betydning for proteinets struktur og funksjon.
De fleste naturlig forekommende aminosyrene i kroppen finnes i det som kalles L-konfigurasjon, som handler om hvordan atomene er orientert i rommet. Dette er viktig for hvordan proteinene brettes og fungerer.
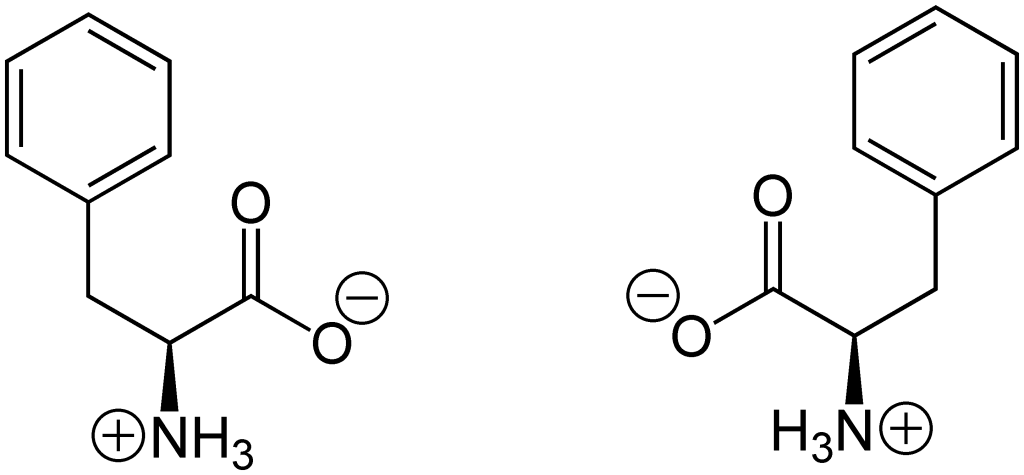
Ionisering
Aminosyrer har ioniseringsegenskaper, altså evne til å bære elektrisk ladning, og dette påvirkes av pH i omgivelsene. Både aminogruppen og karboksylsyregruppen kan ta opp eller avgi protoner (H⁺), og på den måten bli ladet.
- Aminogruppen har en pKa på ca. 9,5, og vil vanligvis være positivt ladet ved fysiologisk pH (rundt 7,4)
- Karboksylgruppen har en pKa på ca. 2,2, og vil være negativt ladet ved samme pH
Ved pH mellom 4 og 8 er begge gruppene ladet – men med motsatt ladning. Dette gjør at aminosyren opptrer som et zwitterion – et molekyl som samtidig har både en positiv og en negativ ladning, men som totalt sett er elektrisk nøytralt.
Når aminosyrene kobles sammen i en polypeptidkjede (et protein), forsvinner disse ladningene for de fleste aminosyrene – fordi aminogruppen og karboksylgruppen danner peptidbindinger. Det er bare de frie endene – N-terminalen (aminosiden) og C-terminalen (karboksylsiden) – som fortsatt kan være ionisert.
Proteiners ladning – surt eller basisk?
Proteiners totale ladning i en gitt løsning bestemmes av hvilke aminosyrer de inneholder:
- Hvis et protein inneholder mange sure aminosyrer, som glutaminsyre og asparaginsyre, vil det ha en negativ ladning og være surt.
- Hvis det derimot inneholder mange basiske aminosyrer, som arginin, lysin, og til en viss grad histidin, vil det være positivt ladet og basisk.
Disse ladningsegenskapene påvirker hvordan proteinet folder seg, hvor det lokaliseres i cellen, og hvordan det interagerer med andre molekyler.
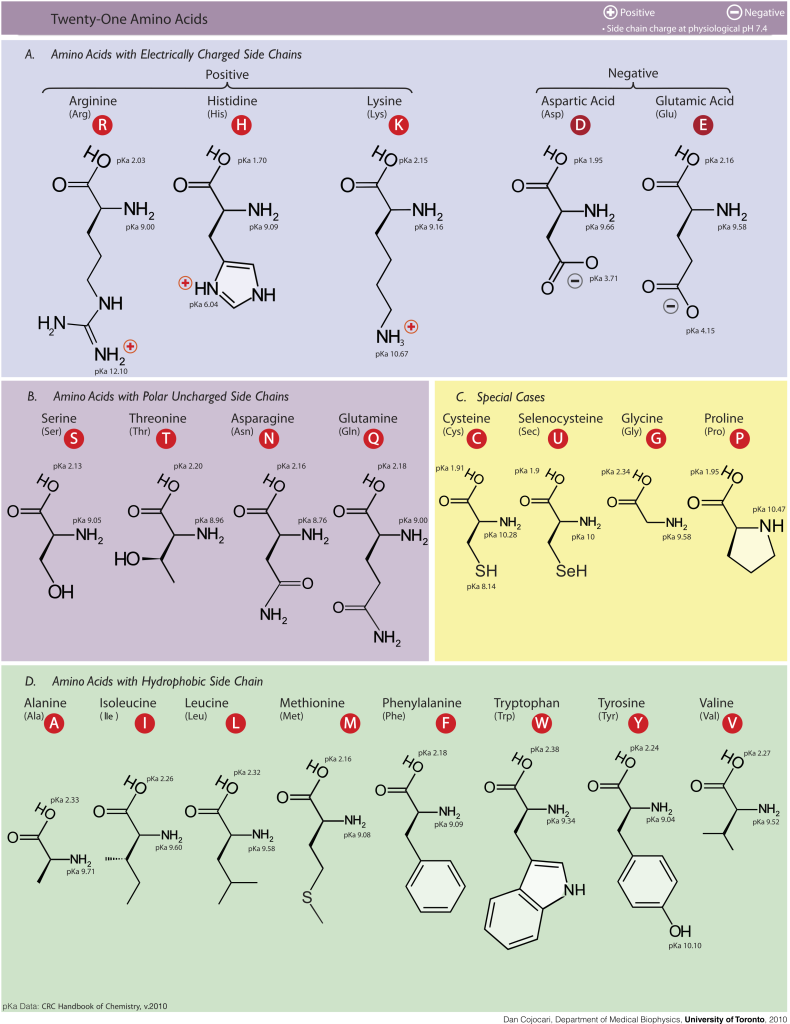
Aminosyrenes inndeling
Alle proteiner, uansett om de finnes i muskel, hud eller enzymer i leveren, er satt sammen av de samme 20 aminosyrene. Det som skiller dem fra hverandre er sidekjeden.
Disse sidekjedene varierer i kjemisk struktur og bestemmer hvordan aminosyren vil oppføre seg: om den vil søke seg mot vann eller bort fra det, om den vil tiltrekke eller frastøte andre ladninger, eller om den kanskje foretrekker å inngå spesielle bindinger med naboene sine.
Vi deler derfor aminosyrene inn i fire hovedkategorier, ut fra hva slags sidekjede de har.
Apolære og hydrofobe
Noen aminosyrer har sidekjeder som rett og slett er redde for vann. De foretrekker å gjemme seg vekk inne i proteinets kjerne, der det er tørt og trygt.
Disse kalles apolære eller hydrofobe. De er ikke ladet, og kan ikke danne hydrogenbindinger.
I stedet holder de seg sammen med sine egne ved hjelp av svake van der Waals-krefter.
Blant disse finner vi glycin – den minste av dem alle – og alanin, som bare har en liten metylgruppe som hale.
Valin, leucin og isoleucin er mer robuste, med forgrenede kjeder som bygger opp proteinkjernens indre.
Metionin har et svovelatom i kjeden sin og er alltid først i rekken under proteinsyntesen.
Fenylalanin og tryptofan har store aromatiske ringer, som gjør dem stabile og delvis stive.
Og så har vi prolin, den litt sære i gjengen, som bøyer ryggen tilbake mot seg selv og lager en skarp knekk i polypeptidkjeden.
Polare og hydrofile
Andre aminosyrer bærer på sidekjeder som trekker til seg vannmolekyler. Disse kalles polare, og de trives godt på proteinets overflate.
Der kan de danne hydrogenbindinger med vannet rundt eller med andre molekyler. De kan også være aktive deltakere i enzymer, der binding og kjemiske reaksjoner skjer.
Serin og treonin har små hydroksylgrupper (-OH) som er glade i vann.
Cystein, på sin side, bærer et svovelatom og kan danne disulfidbroer med en annen cystein – et slags molekylært håndtrykk som binder to deler av proteinet sammen. Tyrosin er både polar og delvis hydrofob, og kan delta i signaloverføring.
Asparagin og glutamin har sidekjeder som inneholder amidgrupper, som gjør dem polare uten å være ladet.
Disse aminosyrene er som små kontaktpunkter som tillater kommunikasjon mellom proteinet og omgivelsene.
Basiske aminosyrer – de med positiv ladning
Noen aminosyrer bærer med seg en positiv ladning, og de er derfor basiske.
Ved fysiologisk pH (rundt 7,4) vil de være protonert og klare for å tiltrekke seg negativt ladede molekyler.
Disse finnes ofte i proteiner som samhandler med DNA, som jo selv er negativt ladet, eller i aktive områder i enzymer.
Lysin har en lang sidekjede med en aminogruppe ytterst, arginin har en guanidiniumgruppe som er permanent positiv, og histidin har en spesiell ring som kan veksle mellom ladet og uladet form – dette gjør histidin særlig nyttig i enzymer som må være følsomme for små pH-endringer.
Sure aminosyrer – de med negativ ladning
Aspartat og glutamat er de to sure aminosyrene.
Begge har en karboksylgruppe i sidekjeden, som lett gir fra seg et proton og blir negativt ladet. De er de rake motsetningene til de basiske aminosyrene, og tiltrekker seg derfor positiv ladning.
De finnes ofte i bindingslommer, eller der proteinet trenger å samhandle med metallioner eller andre ladde grupper.
De kan også være med på å forme ionekanaler eller bidra til å skape elektrisk ladning over membraner.
Peptidbindinger
Hver av aminosyrene bærer to grupper som gjør dem i stand til å knyttes sammen – en karboksylgruppe (-COOH) i den ene enden, og en aminogruppe (-NH₂) i den andre.
Når disse gruppene møtes, reagerer de med hverandre i en kondensasjonsreaksjon: et vannmolekyl fjernes, og en sterk kjemisk binding dannes. Dette er peptidbindingen.
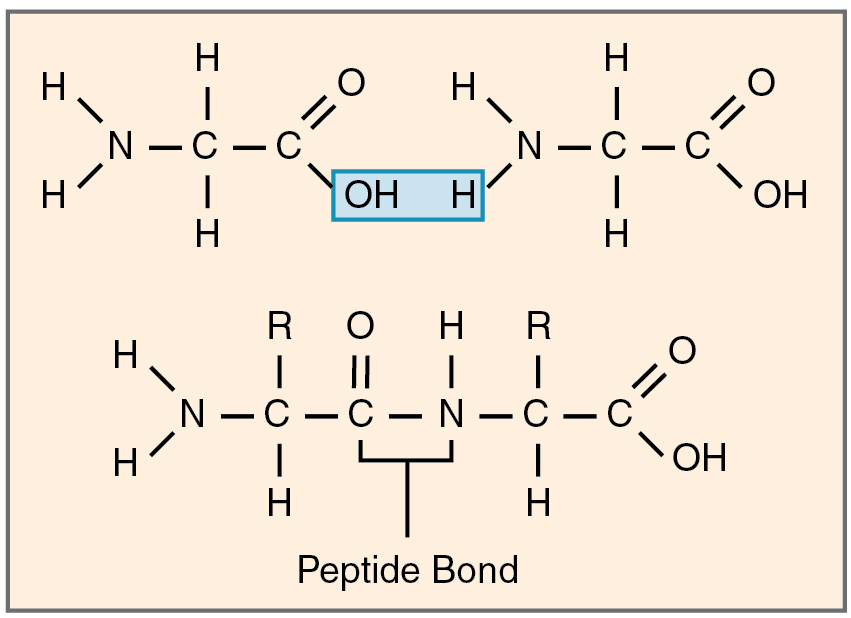
Det er karbonet i karboksylgruppen som binder seg til nitrogenet i aminogruppen – og resultatet er en ny kjemisk enhet: et dipeptid.
Når denne prosessen gjentas igjen og igjen, dannes lengre kjeder av aminosyrer, kjent som polypeptider – og når disse kjedene folder seg riktig, får vi proteiner.
Peptidbindingen i seg selv er bemerkelsesverdig stabil og plan.
Dette skyldes at elektroner deles mellom karbonet, oksygenet og nitrogenet i bindingen, noe som gir den delvis dobbeltbindingsegenskaper.
Det betyr at selve bindingen ikke kan rotere fritt.
Den er som et stivt ledd mellom to fleksible armer – de nærliggende bindingene kan rotere, men selve peptidbindingen holder formen.
Denne stivheten bidrar til hvordan proteinet til slutt folder seg.
For selv om kjeden kan bøyes og vris på mange måter, er det ikke tilfeldig hvordan den ender opp.
Hver aminosyre påvirker de omkringliggende, og hele kjeden søker en struktur som krever minst mulig energi.
Hydrogenbindinger, hydrofobe interaksjoner, ionebindinger og disulfidbroer samarbeider for å trekke proteinet inn i en spesifikk tredimensjonal form – en form som er avgjørende for proteinets funksjon.
Enzymet som hjelper til med å danne peptidbindinger i kroppen, finnes i ribosomet – det er der proteinsyntesen skjer. Og hver gang en ny aminosyre legges til kjeden, er det gjennom akkurat denne reaksjonen: en peptidbinding dannes, og et vannmolekyl slippes fri.
Dette er grunnen til at proteiner kan være både lange, komplekse og spesialiserte. Alt starter med enkle, små molekyler som kobles sammen – og det hele holdes sammen av peptidbindingens usynlige styrke.
Kjemiske bindinger som former proteinet
For at et protein skal fungere slik det skal, må det ikke bare bestå av riktig rekkefølge av aminosyrer – det må også ha riktig tredimensjonal form.
Og det er her de kjemiske kreftene i proteinet spiller sin avgjørende rolle. Flere typer bindinger og interaksjoner samarbeider for å stabilisere proteinets struktur. La oss se nærmere på de viktigste:
Hydrogenbindinger
Hydrogenbindinger er blant de mest sentrale kreftene som holder proteiner sammen. De oppstår når et hydrogenatom som er bundet til et elektronegativt atom (som nitrogen eller oksygen), trekkes mot et annet elektronegativt atom i nærheten.
Disse bindingene er avgjørende for å danne og stabilisere sekundærstrukturer, som alfa-helikser og beta-sheets.
I en alfa-heliks holder hydrogenbindingene kjeden snodd som en spiral, mens i en beta-sheet sørger de for at proteintråder legger seg flatt og tett ved siden av hverandre.
Hydrogenbindinger er ikke spesielt sterke hver for seg, men fordi det er så mange av dem, har de en samlet effekt som er helt avgjørende for proteinets struktur.
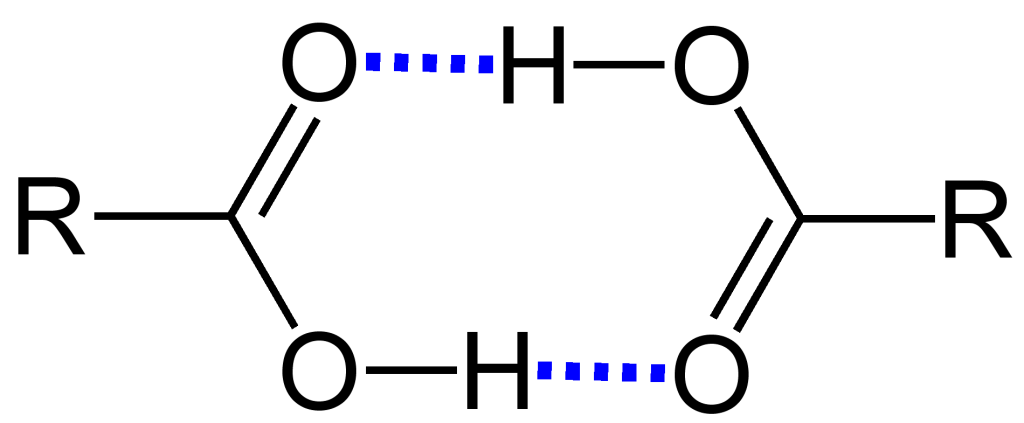
Elektrostatiske interaksjoner
Disse interaksjonene skjer mellom ladde grupper på aminosyrene.
Positive og negative ladninger tiltrekker hverandre – som når en positivt ladet sidekjede fra lysin, arginin eller histidin binder seg til en negativt ladet gruppe fra aspartat eller glutamat.
Dette kalles også for ionebindinger eller saltbroer, og bidrar til å stabilisere proteinets struktur, spesielt i områder der det er lite vann (som i proteinkjernene eller inne i cellemembraner).
Men ladninger kan også frastøte hverandre. To like ladninger i nærheten kan skape repulsjon, og dette kan bidra til at deler av proteinet skyver hverandre bort og folder seg annerledes.
Van der Waals-krefter
Van der Waals-interaksjoner er svake, men viktige. Disse kreftene oppstår når atomer er tett på hverandre og danner en slags balanse mellom tiltrekning og frastøting.
Hver atomtype har sin van der Waals-radius, og når to atomer ligger akkurat i riktig avstand fra hverandre, oppnås et energi-minimum. Det betyr at systemet er mest stabilt – og det koster minst energi å holde det slik.
Selv om én slik interaksjon er svak, kan mange sammen bidra betydelig til stabilisering – spesielt inne i proteinet der atomene ligger tettpakket.
Hydrofobe interaksjoner
Dette er en av de viktigste drivkreftene bak hvordan et protein folder seg.
Noen sidekjeder – som de fra aminosyrene valin, leucin, isoleucin, fenylalanin og metionin – liker ikke vann.
I en vandig løsning vil disse hydrofobe (vannskyende) delene trekke seg bort fra vann og samles i midten av proteinet – omtrent som oljedråper som klumper seg sammen i vann.
På denne måten danner proteinet en indre, vannavvisende kjerne, mens de hydrofile (vannelskende) delene vender utover mot det omkringliggende vannet. Dette bidrar sterkt til proteinets endelige form.
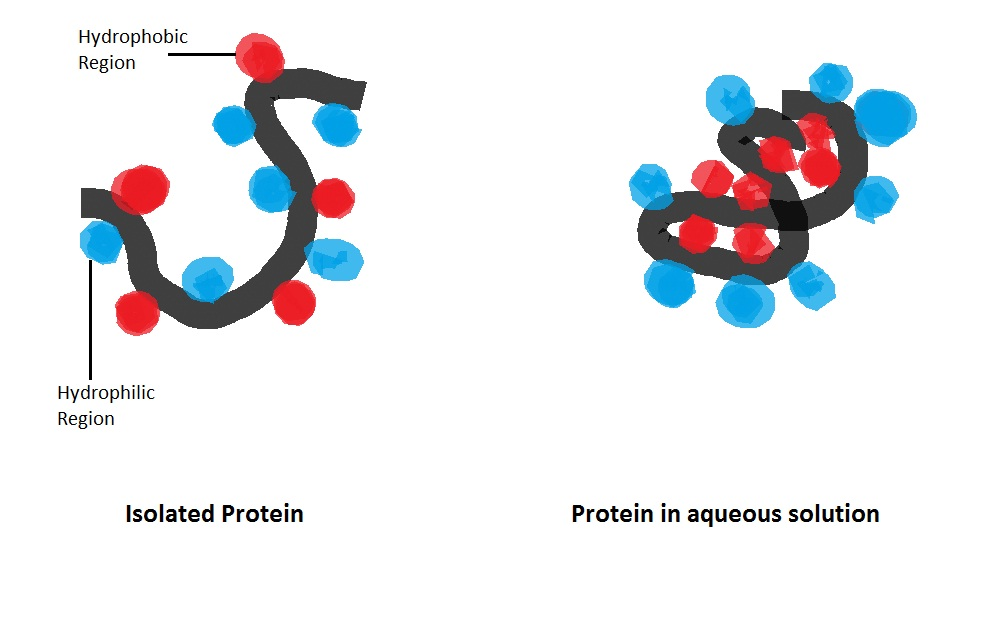
Proteinstruktur
Proteiner er lange kjeder av aminosyrer som folder seg til bestemte tredimensjonale former. Disse formene er avgjørende for proteinets funksjon, og foldingen skjer spontant basert på egenskapene til hver aminosyre i kjeden. Når et protein folder seg riktig, frigjøres energi i form av varme. Dette betyr at den foldede strukturen er mer stabil og har lavere energi enn den ufoldede kjeden. Samtidig øker entropien i omgivelsene – det vil si at det blir mer uorden rundt, selv om selve proteinet blir mer ordnet.
Proteinets tredimensjonale struktur er forhåndsprogrammert av rekkefølgen på aminosyrene – altså dens primærstruktur.
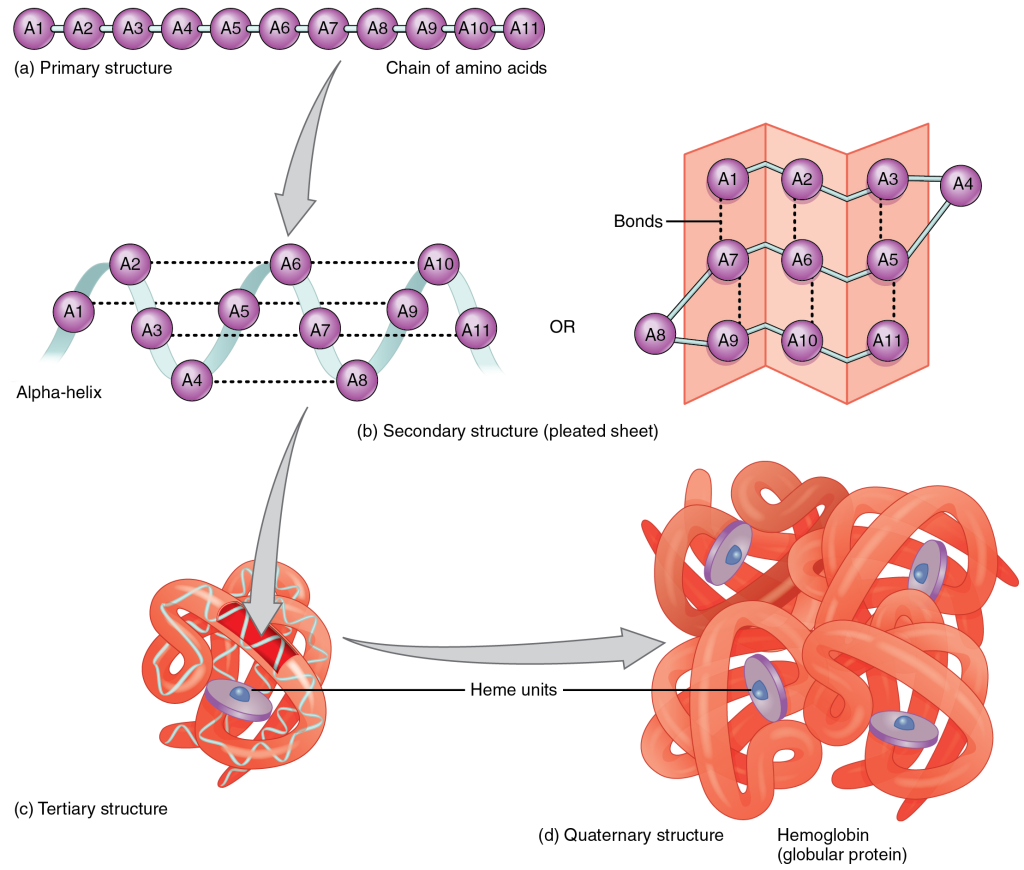
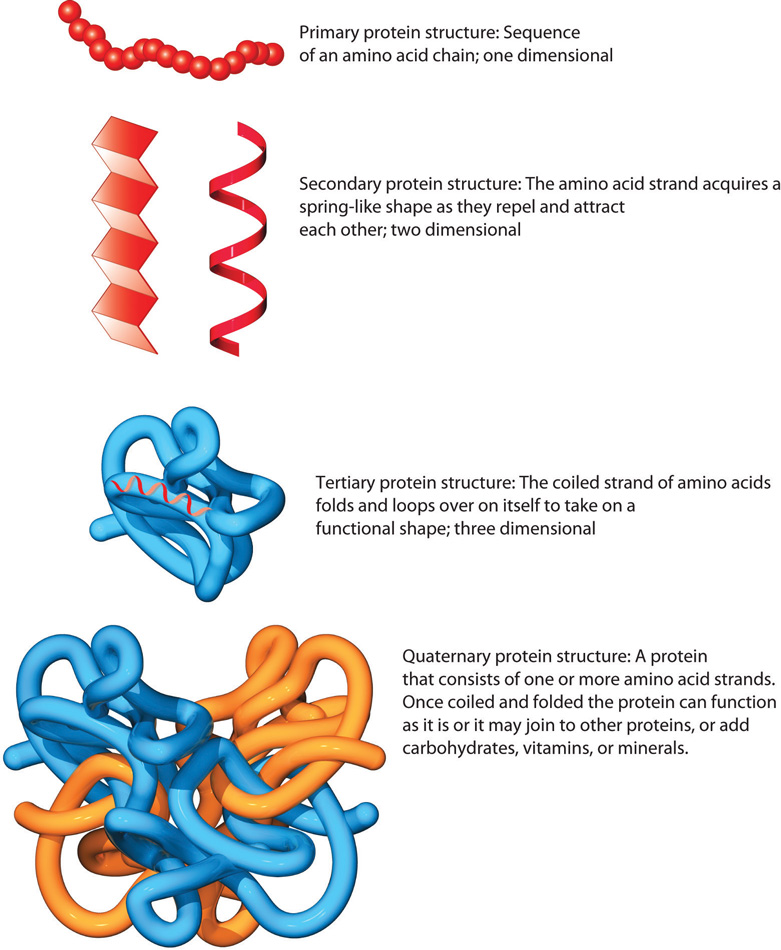
Primærstruktur
Primærstrukturen er den lineære rekkefølgen av aminosyrer i et protein. Denne sekvensen starter ved N-terminalen (enden med en fri aminogruppe) og slutter ved C-terminalen (enden med en fri karboksylgruppe). Rekkefølgen er spesifikk og bestemt av genetisk informasjon i DNA. Hver aminosyre i sekvensen representeres ofte med en forkortelse, for eksempel:
Met-Gly-Thr-Ser-Ala-Lys-Pro
Selv små endringer i primærstrukturen – som én enkelt aminosyre – kan ha stor innvirkning. For eksempel skyldes sigdcelleanemi en eneste mutasjon i hemoglobinmolekylet.

Sekundærstruktur
– proteinets indre organisering
Når en lang polypeptidkjede folder seg til et funksjonelt protein, skjer det ikke tilfeldig. Proteiner folder seg nemlig alltid mot den strukturen som gir lavest mulig energi – og det skjer spontant. Når et protein folder seg, frigjøres det varme, og systemet rundt får økt entropi – altså mer uorden – mens selve proteinet stabiliseres i sin bestemte tredimensjonale form. Og denne formen er ikke tilfeldig valgt: Den er forhåndsbestemt av aminosyresammensetningen i primærstrukturen.
Den hydrofobe kjernen og den hydrofile overflaten
I vannløselige proteiner finner vi et mønster: de hydrofobe (vannavstøtende) aminosyrene pakker seg sammen innerst, i kjernen, mens de hydrofile (vannelskende) aminosyrene vender ut mot overflaten.
Dette skjer fordi det er energimessig gunstig i et vannholdig miljø som cytoplasma.
❓ Denise lurer: Hvorfor er kjernen hydrofob og utsiden hydrofil?
Det er fordi vann er et polart molekyl, og hydrofobe grupper ikke liker å være i kontakt med det. Ved å skjule de hydrofobe sidene inne i proteinet og la de hydrofile være på utsiden, senker proteinet sin frie energi og blir stabilt.
Dette er en drivkraft for proteinfolding og forklarer hvorfor mange vannløselige proteiner ser ut slik de gjør.
Sekundærstruktur refererer til lokal folding av deler av polypeptidkjeden til stabile mønstre.
Disse mønstrene stabiliseres ved hydrogenbindinger mellom NH- og C=O-grupper i peptidbindingene – altså ikke mellom sidekjedene, men i selve ryggraden.
To hovedtyper dominerer:
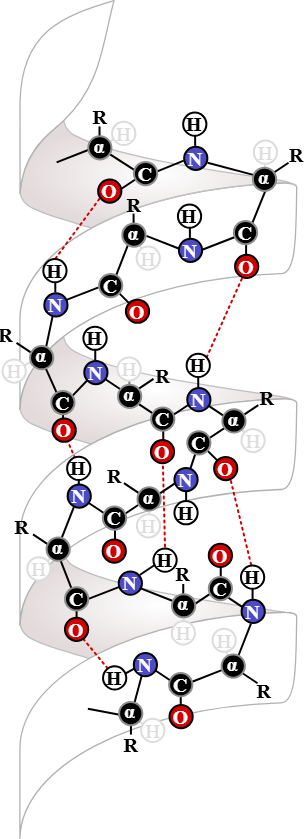
α-heliks (alfa-heliks)
Alfa-heliksen er som en stram spiralfjær der kjeden snurrer rundt seg selv. Strukturen stabiliseres av hydrogenbindinger mellom hver fjerde aminosyre langs kjeden. Sidekjedene peker utover fra spiralen, og heliksen får et dipolmoment – én ende blir delvis positiv og den andre delvis negativ.
Alfa-heliksen er svært vanlig i mange proteiner:
- Hemoglobin har flere alfa-helikser som holder oksygenmolekylet på plass.
- Keratin, proteinet i hår og negler, består av mange spiraler tvinnet sammen.
- Myosin i musklene har lange helikser som gjør det mulig å trekke seg sammen.
- DNA-bindende proteiner bruker ofte alfa-helikser som «nøkler» som passer inn i DNA-ets struktur.
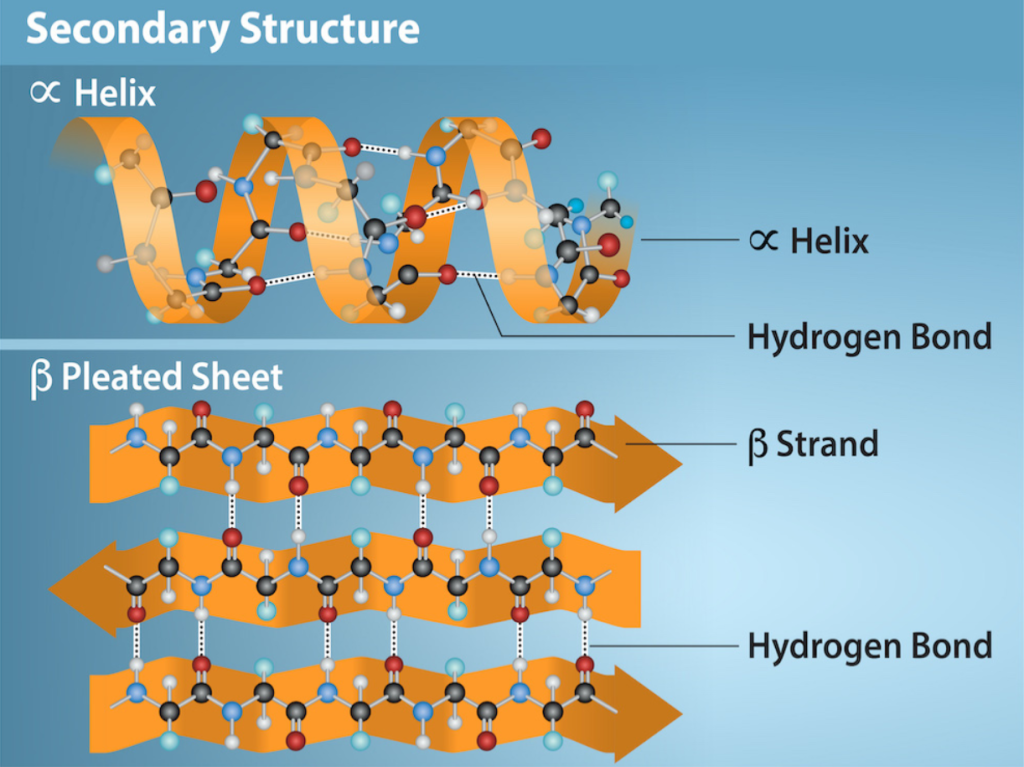
β-flak (beta-sheets)
Beta-strukturene dannes når kjeden folder seg ut i rette segmenter – kalt beta-tråder – som legger seg parallelt eller antiparallelt med hverandre og bindes sammen av hydrogenbindinger.
Resultatet er flate, båndformede områder – ofte litt vridde – som gir proteinet stivhet og styrke.
I illustrasjoner vises beta-tråder gjerne som piler som peker fra N-terminal til C-terminal. Og når flere tråder bindes sammen, danner de et β-sheet – et slags molekylært flak.
Beta-strukturer finnes i mange viktige proteiner:
- Antistoffer bruker beta-sheets for å danne stabile bindingslommer.
- Enzymer bruker dem som plattformer der kjemiske reaksjoner skjer.
Loops og turns – fleksible koblinger
Ikke all struktur er så ordnet. Mellom helikser og flak finner vi ofte fleksible områder kalt loops eller turns. Disse er ikke tilfeldige, men gir proteinet mulighet til å binde seg til andre molekyler eller endre form ved behov.
❓ Denise lurer: Hva betyr det at loops er mindre konservative?
Det betyr at disse områdene lettere kan endre seg gjennom evolusjon uten å ødelegge proteinets funksjon.
De er mer «tolerante» for mutasjoner fordi de ikke er like kritiske for proteinets struktur som helikser og flak ofte er.
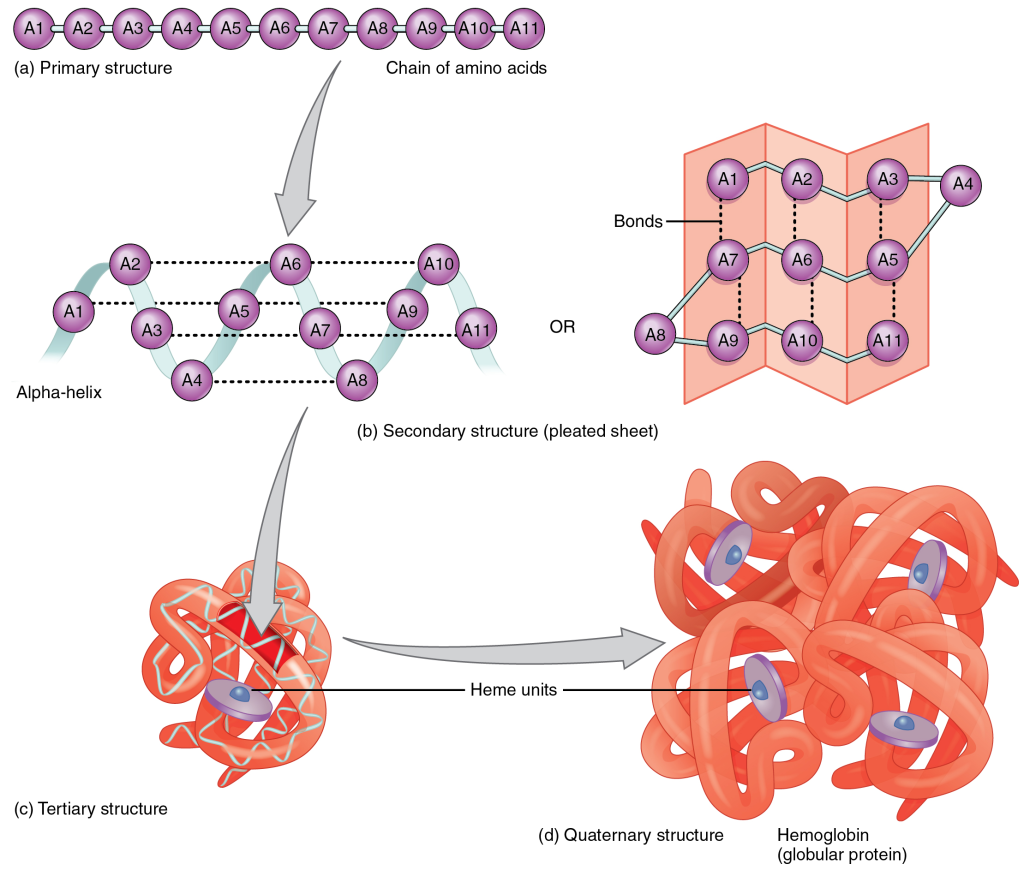
Tertiærstruktur
– proteinets tredimensjonale form
Et protein er ikke ferdig så snart det har dannet spiraler og flak. De ulike delene – alfa-helikser, beta-sheets og løkker – må også finne sin plass i forhold til hverandre i rommet.
Det er dette som kalles tertærstruktur: proteinets endelige tredimensjonale form. Det er her proteinet går fra å være en fleksibel tråd med strukturelle innslag – til å bli et funksjonelt, romlig tilpasset molekyl.
Tertiærstrukturen bestemmes av hvordan de ulike sekundærstrukturelementene pakker seg sammen og organiserer seg rundt den hydrofobe kjernen.
Denne formen er unik for hvert protein, og den er helt avgjørende for at proteinet skal kunne utføre sine spesifikke oppgaver i cellen – enten det er å katalysere reaksjoner, binde til andre molekyler, eller fungere som en transportør.
Hva holder strukturen sammen?
Foldingen til tertiærstrukturen skjer gjennom et komplekst samspill av kjemiske bindinger og fysiske krefter mellom aminosyrene – spesielt mellom sidekjedene deres. Noen trekker mot hverandre, andre skyver hverandre bort. Noen danner sterke broer, andre danner svake, men viktige forbindelser. Sammen sørger de for at proteinet foldes på en presis måte og forblir stabilt.
De viktigste kreftene er:
- Hydrogenbindinger, mellom NH- og CO-grupper eller sidekjeder som kan danne slike bånd
- Ioniske interaksjoner, mellom positivt og negativt ladede aminosyrer
- Van der Waals-krefter, som oppstår når atomer ligger tett, men i perfekt balanse
- Hydrofobe interaksjoner, der vannskyende grupper trekker seg mot proteinets indre
- Disulfidbindinger, sterke kovalente broer mellom cysteinrester, som «låser» strukturen
I tillegg kan tertiærstrukturen påvirkes av eksterne forhold som pH, temperatur og saltkonsentrasjon. Dette er grunnen til at proteiner kan denaturere – altså miste sin struktur og funksjon – hvis miljøet blir for ekstremt.
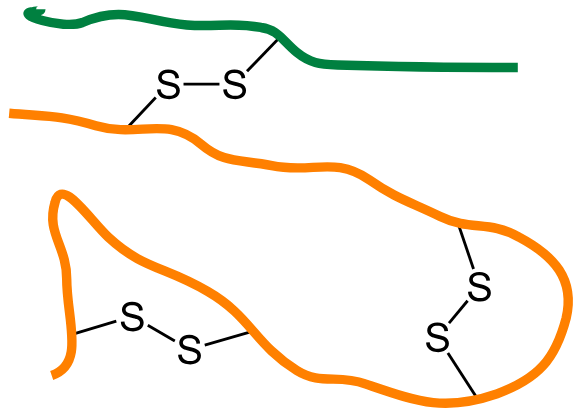
Disulfidbindinger – kjemiske låser i strukturen
Blant de mest avgjørende strukturelle elementene i tertiærstruktur finner vi disulfidbindingene. Disse oppstår mellom to cystein-rester som ligger i nærheten av hverandre i det foldede proteinet. Når svovelatomene i deres sidekjeder oksideres, dannes det en sterk kovalent binding – en disulfidbro – som holder proteinet sammen.
Disulfidbroene virker som kjemiske låser og er spesielt viktige i proteiner som finnes utenfor cellen, der miljøet er mer oksidativt. Der bidrar de til å gjøre proteinet mer robust og motstandsdyktig mot denaturering.
Post-translasjonelle modifikasjoner
– finjustering etter produksjon
Etter at et protein er syntetisert i ribosomet, er det fortsatt ikke nødvendigvis klart til bruk. Mange proteiner gjennomgår kjemiske endringer etter translasjonen – såkalte post-translasjonelle modifikasjoner (PTM). Disse kan være midlertidige eller permanente, og de regulerer blant annet proteinets funksjon, stabilitet, lokalisering og interaksjoner.
Det er identifisert over 400 typer PTM, og mange av dem skjer spesifikt i bestemte celletyper eller som respons på signaler.
De viktigste typene du bør kjenne til er:
Fosforylering
Fosforylering skjer når en fosfatgruppe festes til en OH-gruppe på aminosyrene serin, treonin eller tyrosin. Dette skjer ved hjelp av spesifikke enzymer kalt kinaser, og fosfatgruppen kan fjernes igjen av fosfataser.
Fosforylering fungerer ofte som en på- eller av-knapp for enzymer og signalproteiner.
Eksempel: I muskelceller aktiveres enzymet glykogenfosforylase ved fosforylering. Dette starter nedbrytningen av glykogen, slik at cellen får tilgang på energi.
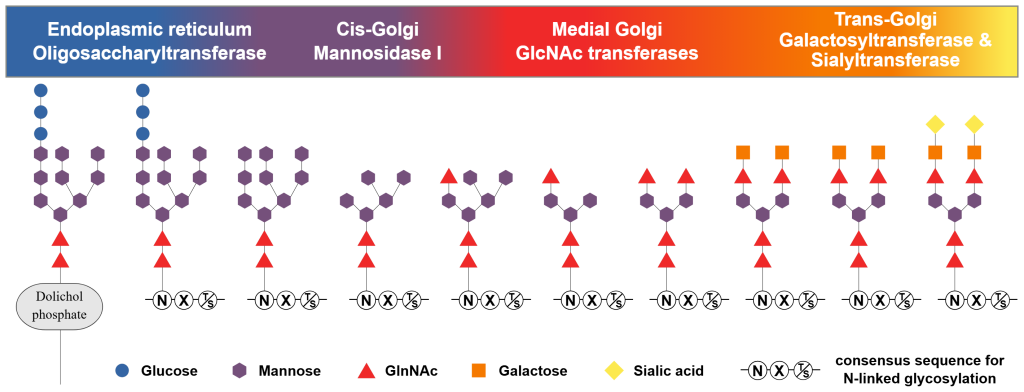
Glykosylering
Her festes sukkerkjeder (oligosakkarider) til proteinet – ofte til sidekjeden på asparagin. Glykosylering er avgjørende for at proteinet skal sorteres riktig inne i cellen og fraktes dit det skal – ofte til cellemembranen.
Sukkerrestene fungerer som identitetsmerker som hjelper cellen å gjenkjenne og kommunisere med andre celler.
Acetylering og metylering
Ved acetylering og metylering festes små kjemiske grupper til spesifikke aminosyrer – ofte på histoner eller transkripsjonsfaktorer – og dette påvirker genregulering, proteinets interaksjoner og dets levetid.
Kvartærstruktur
– når flere proteiner danner ett
Et protein trenger ikke alltid være én sammenhengende kjede. Mange av kroppens viktigste proteiner består faktisk av flere polypeptidkjeder, som sammen danner ett fungerende kompleks. Når disse kjedene – kalt subenheter – kommer sammen og samarbeider, kaller vi det kvartærstruktur. Dette er det høyeste nivået av proteinstruktur.
Hver subenhet kan folde seg og fungere for seg selv, men sammen kan de gjøre noe større. De holdes sammen av svake ikke-kovalente krefter, som hydrogenbindinger, ioniske interaksjoner og van der Waals-krefter – og noen ganger av disulfidbindinger, som danner sterke broer mellom subenheter.
Strukturen kan være symmetrisk, med subenheter arrangert som et mønster, eller asymmetrisk, der hver del har sin helt spesifikke rolle.
Kvartærstruktur gjør det mulig å:
- Koordinere funksjon mellom flere enheter
- Regulere aktivitet dynamisk
- Øke effektiviteten i komplekse prosesser
Eksempler du bør kjenne til:
- Hemoglobin: Består av fire subenheter – to alfa- og to beta-kjeder – som samarbeider om å binde og frakte oksygen. Bindingen til én oksygen påvirker de andre.
- Antistoffer (immunoglobuliner): Har fire kjeder i en Y-form – to lette og to tunge. De binder til inntrengere med den ene enden og signaliserer med den andre.
- Pyruvat dehydrogenase-komplekset: Et stort enzymsamarbeid som omdanner pyruvat til acetyl-CoA, en avgjørende overgang mellom glykolyse og sitronsyresyklus. Her finner vi tre ulike enzymaktiviteter samlet i én funksjonell struktur.
Motiver og domener
– proteinets funksjonelle byggesteiner
Når man ser på et protein i tredimensjonal form, oppdager man at det ikke bare er en tilfeldig formet klump. Det er mønstre, gjentagelser og gjenkjennelige former. Disse kalles motiver og domener – og de er nøkkelen til å forstå hvordan proteiner fungerer.
Motiv
Et motiv er et lite strukturmønster – gjerne bare noen få alfa-helikser og beta-tråder – som er satt sammen på en måte som gir dem en spesiell funksjon. Motiver er ikke selvstendige enheter, men del av større strukturer, og de dukker ofte opp i mange ulike proteiner som trenger å gjøre lignende ting.
🧠 Forklaring for dummies – av Denise
Tenk deg et protein som en avansert maskin. Et motiv er som en ferdigbygd komponent – et tannhjul, en gripearm eller en sensor – som kan settes inn i ulike maskiner. Det gjør ikke alt alene, men er avgjørende for spesifikke oppgaver.
Eksempler:
- Helix-turn-helix: To spiraler koblet med en liten sving – brukes til å kjenne igjen DNA.
- Zinc finger: En liten struktur stabilisert av et sinkatom – fungerer som en presis DNA-grepsmekanisme.
Disse finnes i mange proteiner, som transkripsjonsfaktorer, og gir dem evne til å binde seg til spesifikke DNA-sekvenser.
Domener – selvstendige moduler
Et domene er noe større enn et motiv. Det er en del av et protein som kan folde seg selvstendig, og som ofte har en spesifikk funksjon. Mens et motiv er som en komponent, er et domene mer som en ferdig modul med et tydelig formål.
Proteiner kan ha ett eller flere domener, og hvert domene kan utføre en oppgave. Det er vanlig at:
- Ett domene binder et substrat
- Et annet katalyserer en reaksjon
- Et tredje regulerer aktiviteten
Eksempel: Antistoffets to domener
- Antigenbindende domene: Som en hånd som kjenner igjen og binder fremmede molekyler (antigener)
- Konstant domene: Som en signalstang som aktiverer resten av immunsystemet
Disse to domenene samarbeider i samme protein – og gir det både gjenkjennende og kommuniserende evner.
📚 Anki-kort
Obs, tomt! Kommer etterhvert <3
📝 Eksamensoppgaver
Obs, tomt! Kommer etterhvert <3
👨⚕️ Klinisk case
Obs, tomt! Kommer etterhvert <3
Legg igjen en kommentar